Clear Sky Science · ru
Ndfip2 в сенсорных нейронах, экспрессирующих TrkA, регулирует болевую механоощущаемость через контроль сигналинга и уровней белка TrkA
Почему болевую систему нужно тонко настраивать
Боль может казаться раздражающей, но это одна из важнейших сигнальных систем организма. Когда этот сигнал даёт сбой — либо становится слишком громким при хронической боли, либо слишком тихим у людей, почти не ощущающих повреждения — последствия могут быть тяжёлыми. В этом исследовании выявлена ранее неизвестная молекула, названная Ndfip2, которая помогает задавать чувствительность определённых нервных клеток, воспринимающих боль. Поняв, как работает этот внутриклеточный регулятор, учёные надеются на пути к новым методам лечения, которые ослабляют боль, не отключая при этом жизненно важную защиту.
Ключевые участники болевого «тревожного звонка»
Нервные клетки, обнаруживающие боль и известные как ноцицепторы, располагаются скоплениями у спинного мозга и посылают в мозг сигналы при вредных воздействиях — например уколе булавкой или сильном нагреве. Большая часть этих клеток зависит от сигнала роста, называемого фактором роста нервов (NGF), и его партнёра на поверхности клетки — рецептора TrkA. Когда NGF связывается с TrkA, запускается каскад сигналов, которые помогают этим нейронам развиваться и затем определяют их чувствительность к болевым стимулям. Чрезмерная активность TrkA может усилить боль, а её нехватка — ослабить. Поскольку прямое блокирование NGF в клинических испытаниях вызывало побочные эффекты, учёные сейчас ищут более безопасные способы тонкой настройки этого пути изнутри клетки.
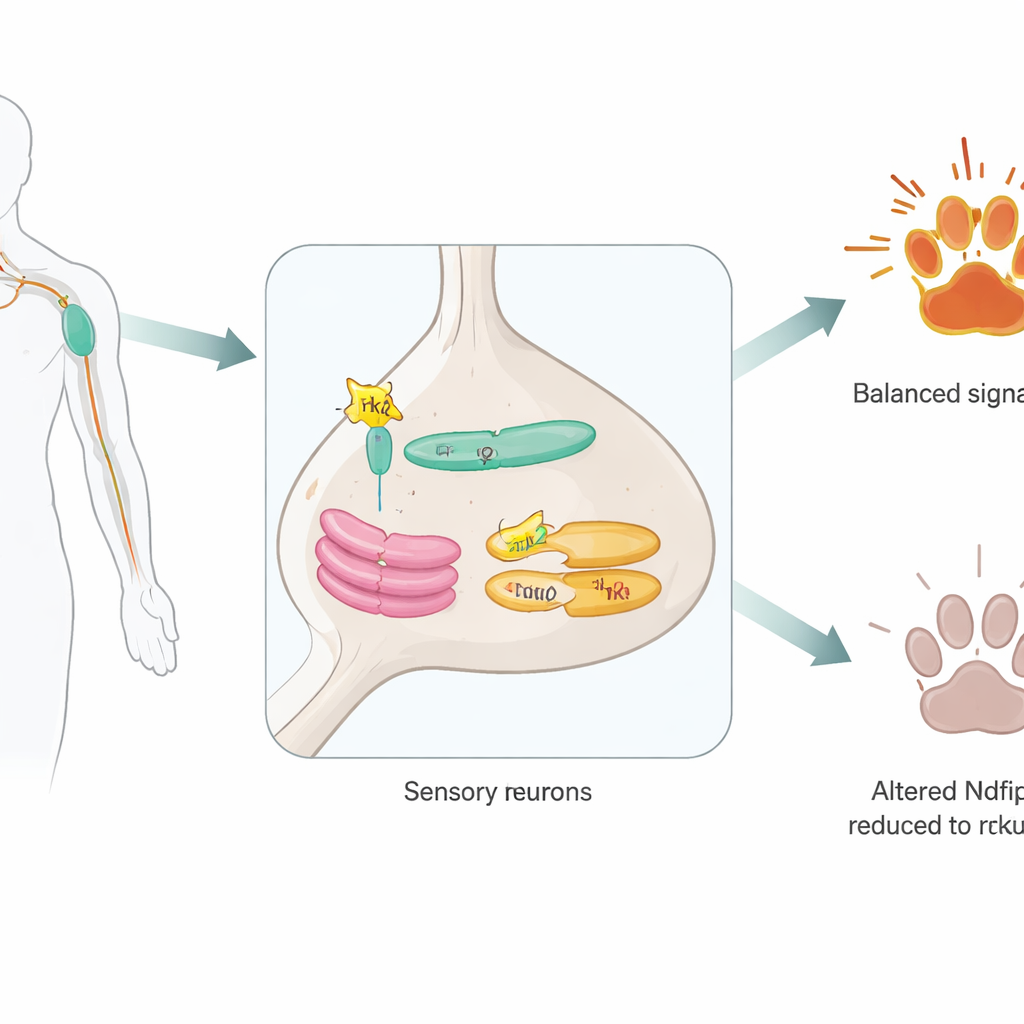
Скрытый помощник внутри сенсорных нейронов
Исследователи сосредоточились на Ndfip2 — белке, ранее известном как помощник ферментов, маркирующих другие белки для разрушения. Они сначала подтвердили, что Ndfip2 присутствует в зрелых болевых нейронах дорсальных корешковых ганглиев и особенно обогащён в клетках, несущих TrkA. Внутри этих нейронов Ndfip2 локализуется в внутриклеточных «логистических центрах» — эндоплазматическом ретикулуме и аппарате Гольджи, а не на поверхности клетки. Там он физически ассоциируется с самим TrkA. Интригующе, у самцов мышей наблюдались более высокие базовые уровни Ndfip2 в этих нейронах, чем у самок, что указывает на возможный вклад этой молекулы в известные половые различия восприятия боли.
Ослабление механической боли без «онемения» всего
Чтобы выяснить роль Ndfip2 в живых организмах, команда создала мышей, у которых Ndfip2 удалён только в клетках, экспрессирующих TrkA. Эти животные росли нормально и не демонстрировали отличий в движениях или поведении, связанном с тревожностью, по сравнению с их сиблингами. Но при тестировании лап с помощью калиброванного механического давления как самцам, так и самкам мутантных мышей требовалась более сильная сила для рефлекторного отдергивания — это указывает на избирательное снижение чувствительности к болевым механическим стимулам. Напротив, реакции на тепло и большинство холодовых тестов не изменились, а поведение при воспалительной боли было лишь незначительно усилено у самок в первые минуты после инъекции формалина. Такая картина указывает на то, что Ndfip2 тонко регулирует специфический канал боли — вредное давление — а не притупляет все формы ощущения.
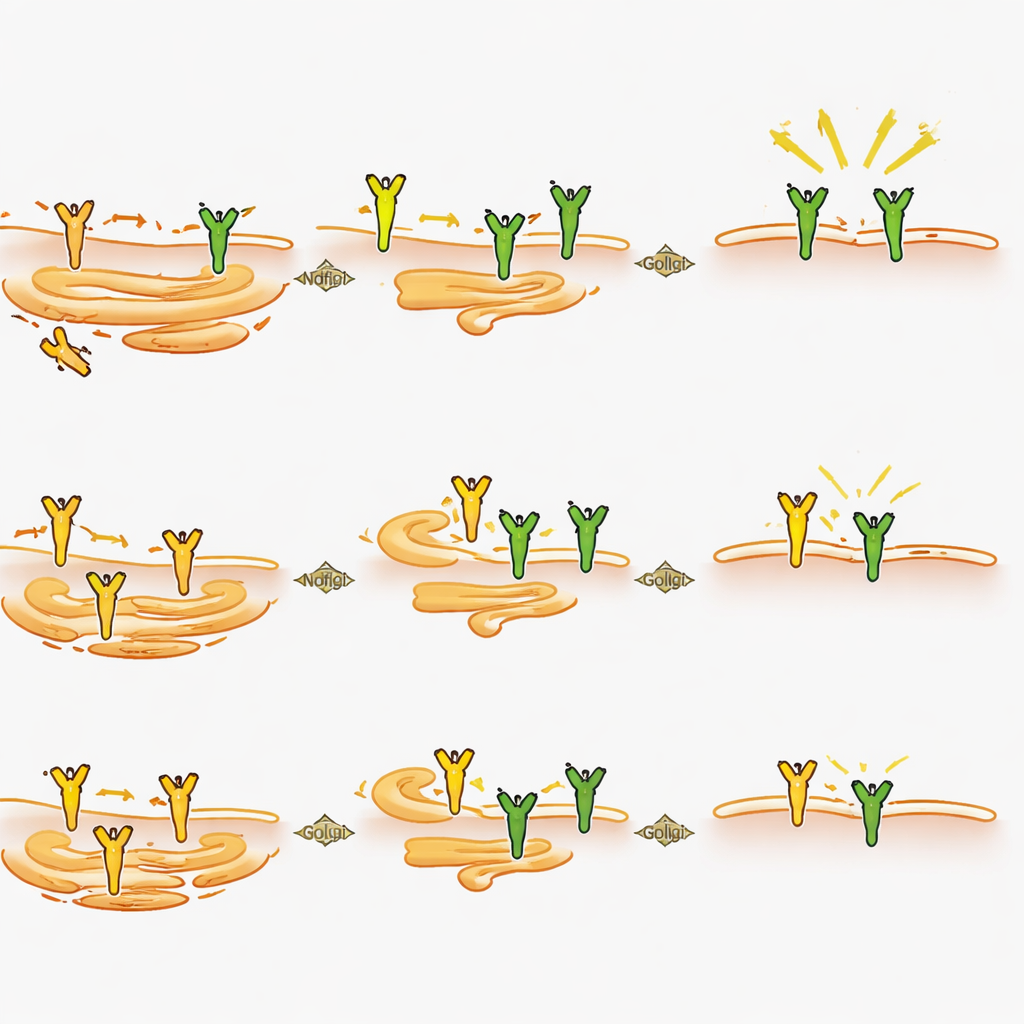
Как Ndfip2 формирует болевой сигнал изнутри клетки
При более детальном изучении нейронов учёные обнаружили, что удаление Ndfip2 снижает общий уровень белка TrkA в дорсальных корешковых ганглиях взрослых животных, особенно у самцов, хотя экспрессия гена TrkA оставалась нормальной. В культивируемых нейронах потеря Ndfip2 уменьшала как уровни TrkA, так и силу сигнала, вызванного NGF, снова более выраженно у самцов. Удивительно, что этот эффект не был связан с изменениями в привычном тегировании TrkA для деградации. Вместо этого эксперименты в клетках показали, что избыток Ndfip2 приводит к накоплению TrkA в незрелой, негликозилированной форме и к уменьшению полностью обработанных вариантов, которые обычно попадают на поверхность клетки. Согласуясь с этим, снижение уровня Ndfip2 в нейронах увеличивало долю TrkA, присутствующего в мембране у самцов. В совокупности эти данные указывают на роль Ndfip2 как регулятора химической зрелости и маршрутизации TrkA внутри клетки, а следовательно — контроля количества функционального рецептора, доступного для восприятия NGF.
Что это значит для будущих методов лечения боли
Описав Ndfip2 как внутриклеточный регулятор системы NGF–TrkA, эта работа добавляет новый уровень понимания того, как организм калибрует чувствительность к боли, особенно к вредным механическим стимулам. Вместо полного блокирования NGF вмешательство в работу Ndfip2 или сопутствующих этапов созревания TrkA может позволить врачам тонко снизить избыточный сигнал в конкретных болевых путях, сохранив при этом защитную функцию боли. Наблюдаемые половые различия в уровнях и эффектах Ndfip2 также подчёркивают необходимость учитывать биологический контекст при разработке будущих терапий, а не полагаться на универсальные решения.
Цитирование: Cañada-García, D., Hernández-García, A., Vicente-García, C. et al. Ndfip2 in TrkA-expressing sensory neurons regulates noxious mechanosensation through control of TrkA signaling and protein levels. Cell Death Dis 17, 437 (2026). https://doi.org/10.1038/s41419-026-08670-9
Ключевые слова: механическая боль, сенсорные нейроны, фактор роста нервов, рецептор TrkA, посттрансляционная регуляция