Clear Sky Science · it
Ndfip2 nei neuroni sensoriali che esprimono TrkA regola la mechano-sensazione nociva attraverso il controllo della segnalazione e dei livelli di proteina TrkA
Perché il dolore richiede una regolazione accurata
Il dolore può sembrare un fastidio, ma è uno dei sistemi di allarme più importanti del corpo. Quando questo allarme funziona male — o troppo forte nel dolore cronico, o troppo debole in persone che percepiscono poco le lesioni — le conseguenze possono essere devastanti. Questo studio individua una molecola finora sconosciuta, chiamata Ndfip2, che contribuisce a impostare la sensibilità di particolari cellule nervose che rilevano il dolore. Capire come opera questo regolatore interno potrebbe indicare nuove strade terapeutiche per alleviare il dolore senza spegnere difese vitali.
Attori chiave dell’allarme del dolore
I neuroni che rilevano il dolore, detti nocicettori, si trovano in aggregati vicino al midollo spinale e inviano segnali al cervello quando incontrano stimoli dannosi come una puntura o un calore estremo. Molti di questi neuroni dipendono da un segnale di crescita chiamato fattore di crescita nervoso (NGF) e dal suo partner sulla superficie cellulare, un recettore chiamato TrkA. Quando NGF si lega a TrkA, avvia una cascata di segnali che aiuta questi neuroni a svilupparsi e successivamente determina quanto reagiscono agli stimoli dolorosi. Troppa attività di TrkA può amplificare il dolore, mentre troppo poca può attenuarlo. Poiché bloccare direttamente NGF ha causato effetti indesiderati nei trial clinici, gli scienziati cercano ora modi più sicuri per modulare questa via dall’interno della cellula.
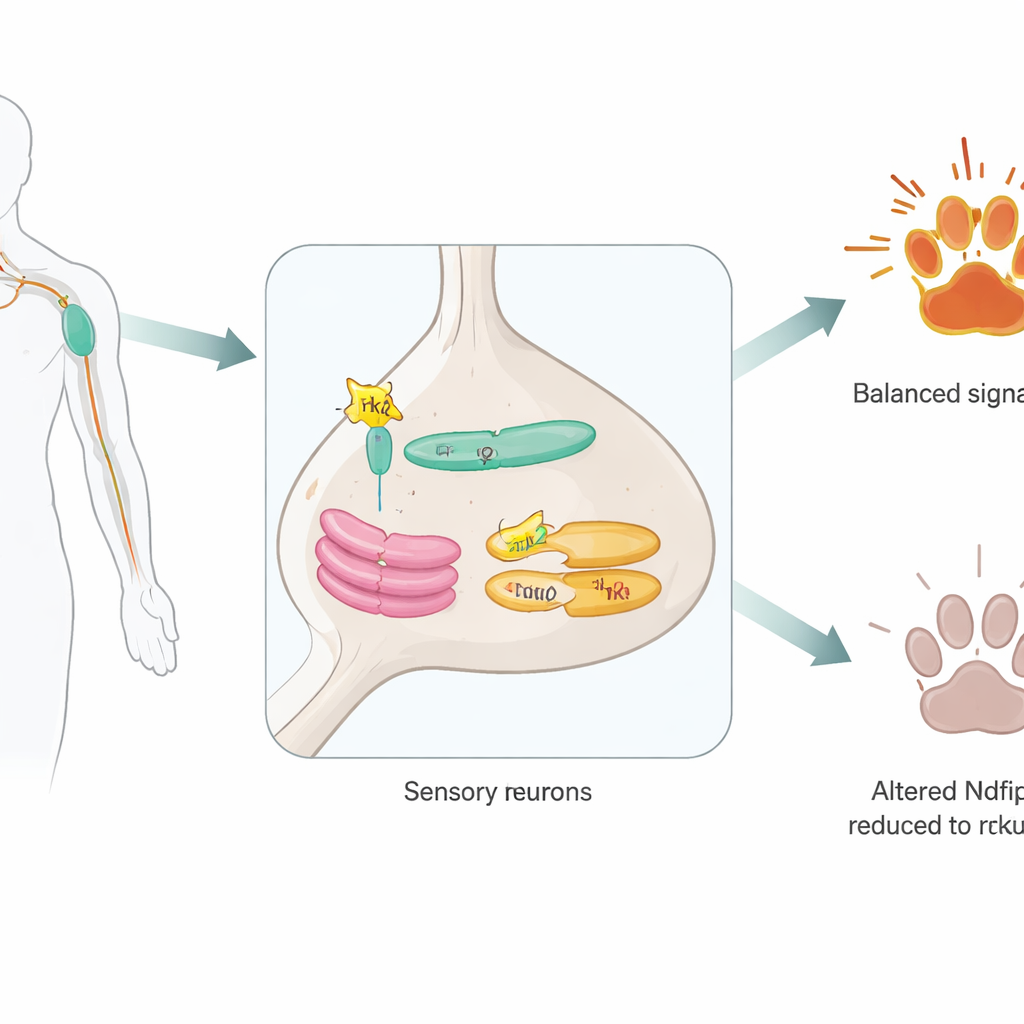
Un aiuto nascosto all’interno dei neuroni sensoriali
I ricercatori si sono concentrati su Ndfip2, una proteina nota in precedenza per assistere enzimi che marcano altre proteine per la degradazione. Hanno innanzitutto confermato che Ndfip2 è presente nei neuroni adulti che percepiscono il dolore nei gangli della radice dorsale ed è particolarmente arricchita nelle cellule che esprimono TrkA. All’interno di questi neuroni, Ndfip2 si raggruppa nei centri di smistamento interni della cellula — il reticolo endoplasmatico e l’apparato del Golgi — piuttosto che sulla superficie cellulare. Lì si associa fisicamente allo stesso TrkA. È interessante che nei topi maschi i livelli basali di Ndfip2 in questi neuroni risultino più alti rispetto alle femmine, suggerendo che questa molecola possa contribuire a differenze di genere già note nella percezione del dolore.
Ridurre il dolore meccanico senza intorpidire tutto
Per sondare il ruolo di Ndfip2 negli animali, il team ha ingegnerizzato topi in cui Ndfip2 è stata rimossa solo dalle cellule che esprimono TrkA. Questi animali sono cresciuti normalmente e non hanno mostrato differenze nel movimento o in comportamenti simili all’ansia rispetto ai consanguinei. Ma quando le loro zampe sono state testate con pressione meccanica calibrata, sia i topi mutanti maschi sia femmina hanno richiesto una forza maggiore prima di ritirare la zampa, rivelando una riduzione selettiva della sensibilità agli stimoli meccanici nocivi. Al contrario, le risposte al calore e alla maggior parte dei test al freddo non sono cambiate, e il comportamento legato al dolore infiammatorio è risultato solo moderatamente aumentato nelle femmine nei primi minuti dopo un’iniezione di formalina. Questo quadro suggerisce che Ndfip2 affina un canale specifico del dolore — la pressione nociva — piuttosto che smorzare in modo generalizzato tutte le forme di sensazione.
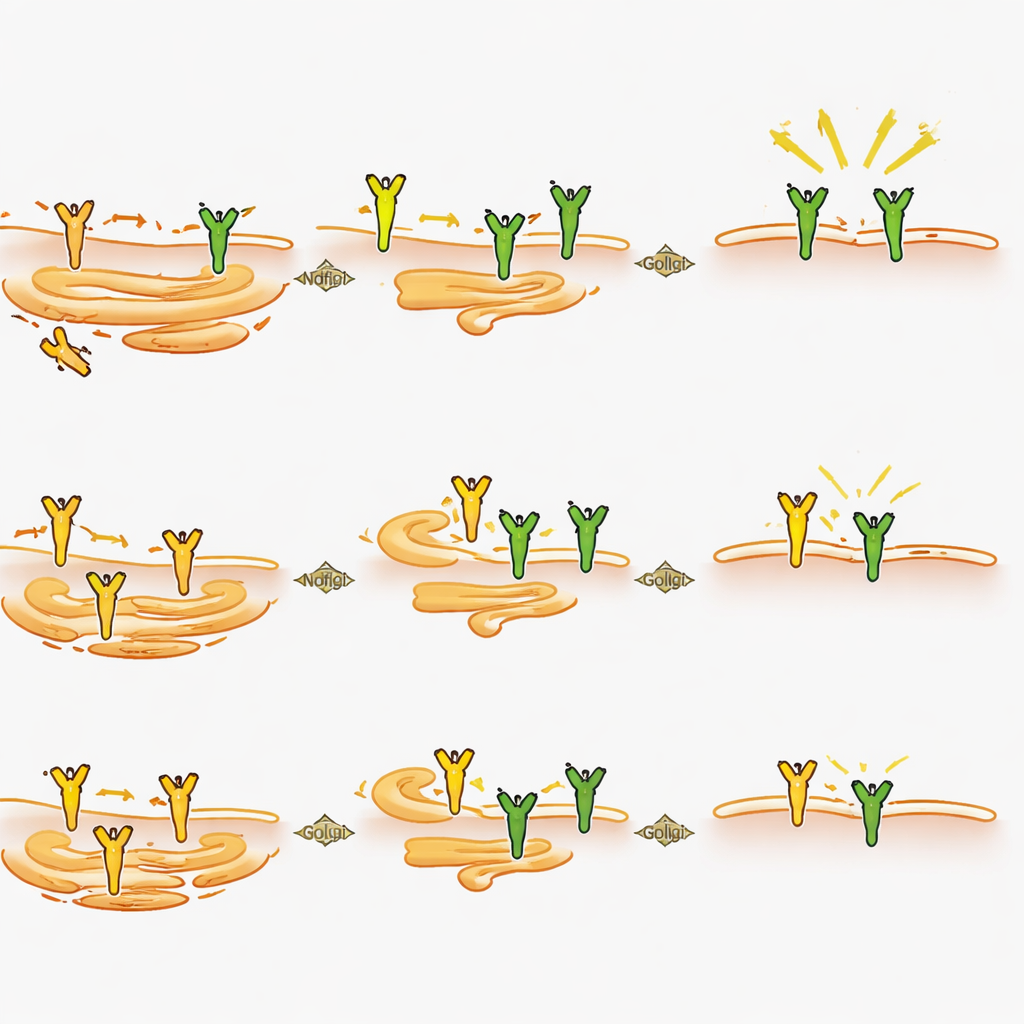
Come Ndfip2 modella il segnale del dolore dall’interno della cellula
Esaminando più da vicino i neuroni, gli scienziati hanno scoperto che la rimozione di Ndfip2 riduceva la quantità complessiva di proteina TrkA nei gangli della radice dorsale adulta, in particolare nei maschi, nonostante il gene di TrkA fosse ancora espresso a livelli normali. Nei neuroni in coltura, la perdita di Ndfip2 riduceva sia i livelli di TrkA sia l’intensità della segnalazione indotta da NGF, ancora una volta in modo più marcato nei maschi. Sorprendentemente, questo effetto non derivava da cambiamenti nel consueto meccanismo di marcatura di TrkA per la degradazione. Al contrario, esperimenti in cellule hanno rivelato che l’eccesso di Ndfip2 provoca l’accumulo di TrkA in una forma immatura non glicosilata, diminuendo nel contempo le versioni completamente processate che normalmente raggiungono la membrana cellulare. Coerentemente, l’abbattimento di Ndfip2 nei neuroni aumentava la frazione di TrkA presente alla membrana nei maschi. Nel complesso, questi risultati indicano Ndfip2 come regolatore della maturazione chimica e del traffico intracellulare di TrkA, controllando così quanto recettore funzionale è disponibile per rilevare NGF.
Cosa significa per le terapie del dolore future
Scoprire Ndfip2 come controllore interno del sistema NGF–TrkA aggiunge un nuovo livello di comprensione a come il corpo calibra la sensibilità al dolore, specialmente per gli stimoli meccanici nocivi. Piuttosto che bloccare NGF in modo netto, intervenire su Ndfip2 o su passaggi correlati nella maturazione di TrkA potrebbe permettere di ridurre sottilmente l’eccessiva segnalazione in specifiche vie del dolore preservando la funzione protettiva complessiva del dolore. Le differenze di genere osservate nei livelli ed effetti di Ndfip2 sottolineano inoltre l’importanza di adattare le future terapie del dolore al contesto biologico, invece di assumere soluzioni universali per tutti.
Citazione: Cañada-García, D., Hernández-García, A., Vicente-García, C. et al. Ndfip2 in TrkA-expressing sensory neurons regulates noxious mechanosensation through control of TrkA signaling and protein levels. Cell Death Dis 17, 437 (2026). https://doi.org/10.1038/s41419-026-08670-9
Parole chiave: dolore meccanico, neuroni sensoriali, fattore di crescita nervoso, recettore TrkA, regolazione post-traduzionale