Clear Sky Science · zh
BAP1 失调损害滋养层细胞分化并促成先兆子痫中的胎盘功能障碍
当妊娠的支持器官出错时
先兆子痫是一种危险的妊娠并发症,表现为高血压并可损害肝脏、肾脏等器官。该病的核心在于胎盘——这个临时器官为胎儿提供营养。本研究揭示了单一调控蛋白 BAP1 的失调如何扰乱关键胎盘细胞的发育,并助长严重的早发型先兆子痫的发生。
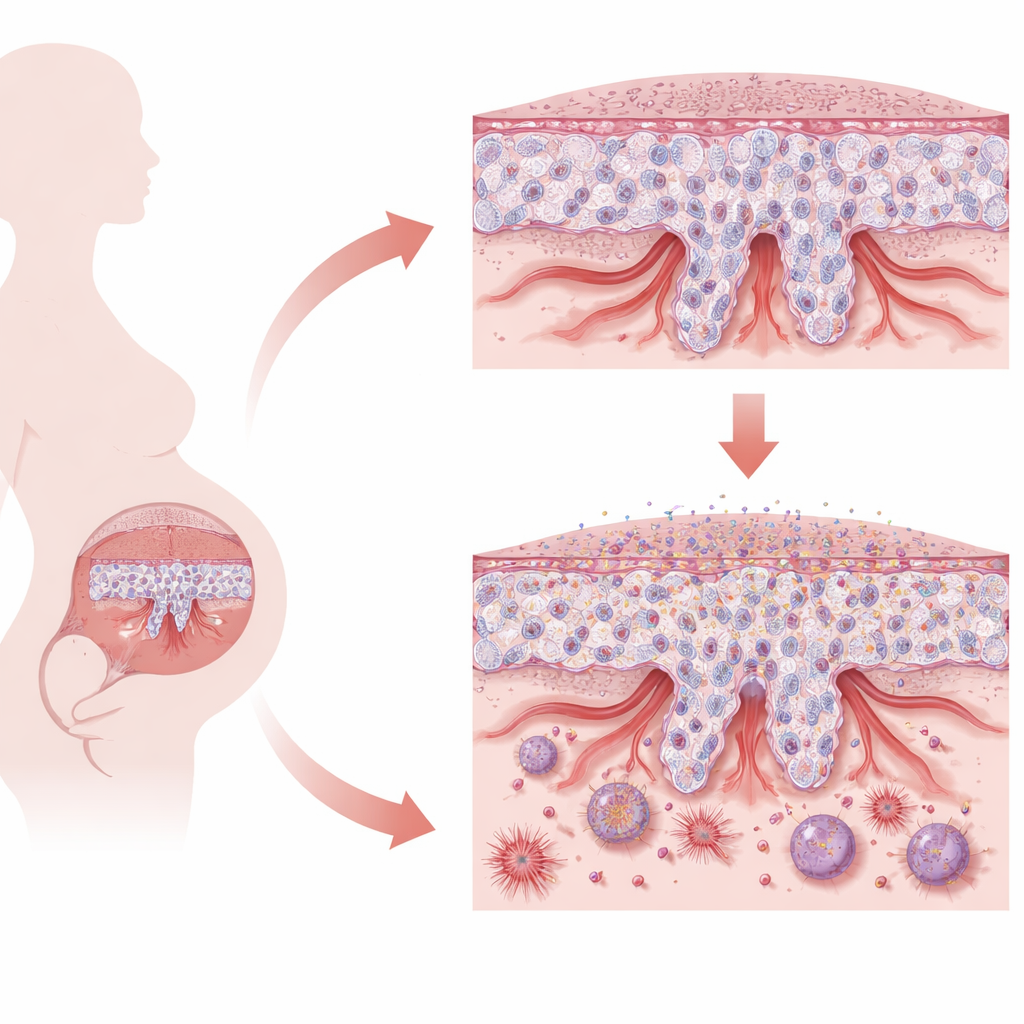
胎盘的精细平衡
胎盘由称为滋养层细胞的专门细胞构成。怀孕早期,类干性的滋养层细胞必须在两种主要功能间作出选择。一部分细胞融合形成连续的表面层,负责营养和气体交换;另一部分则转化为具有侵袭性的细胞,侵入母体子宫并改建螺旋动脉,扩张血管以向发育中的胎儿输送充足血液。这种在维持干性状态、改变细胞身份与适度侵袭之间的微妙平衡至关重要。若该过程失败,如早发型先兆子痫中所见,胎盘将变得浅薄、承受压力,难以维持健康妊娠。
胎盘中被调高的蛋白
研究者将注意力集中在 BAP1——一种在癌症生物学中更为人所知的蛋白。在健康妊娠早期的胎盘中,BAP1 在类干性滋养层细胞中含量高,但随着这些细胞分化成熟,BAP1 通常会下降。研究团队使用有无妊娠并发症的妇女胎盘样本发现,BAP1 及其伴侣蛋白 ASXL2 和 ASXL3 在早发型先兆子痫的胎盘中特异性升高,而在更晚发、以母体因素为主的疾病形式中则未见此变化。该模式提示,过度的 BAP1 活性与胎盘起因的疾病密切相关,而非纯粹的母体因素造成的病变。
将胎盘细胞“冻结”在未成熟状态
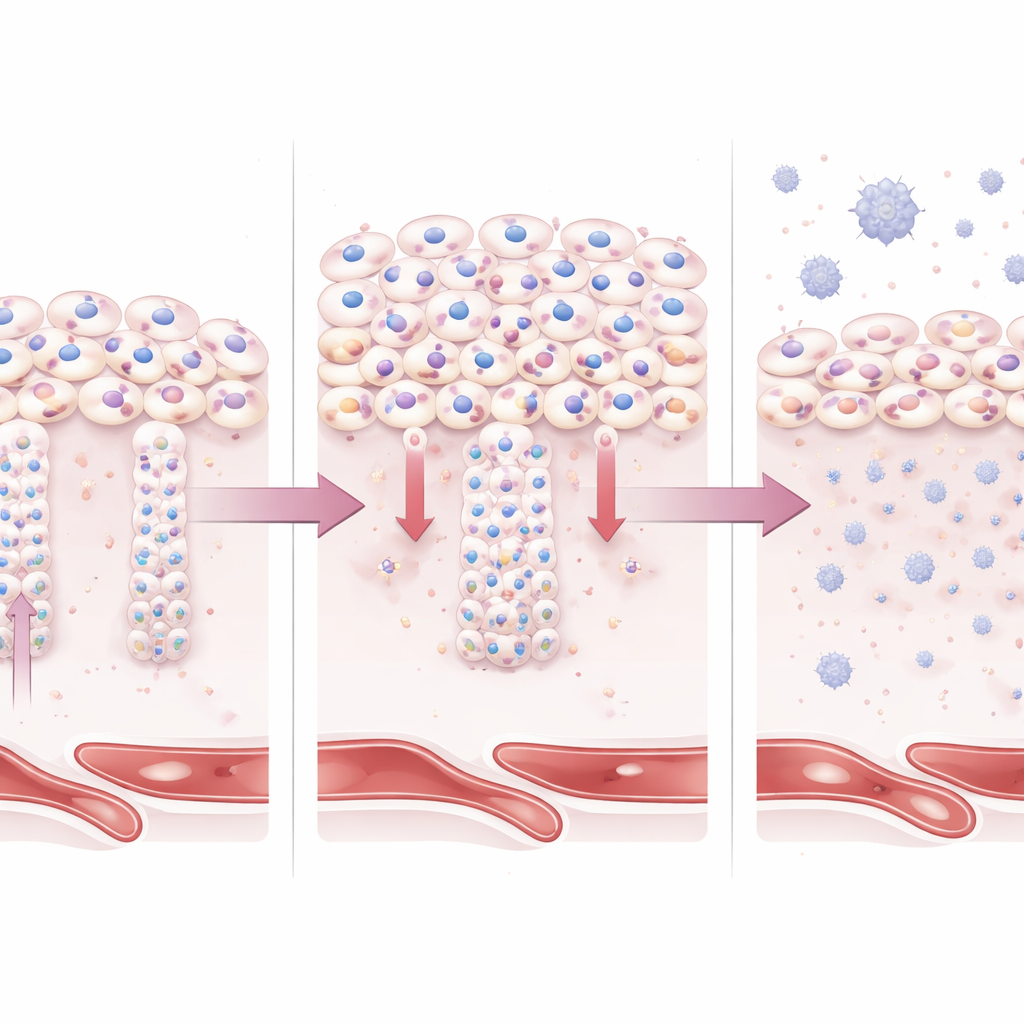
为探明 BAP1 在人类胎盘细胞内的功能,科学家们在体外使用了人类滋养层干细胞和三维胎盘类器官。当他们人为提高 BAP1 水平时,细胞相互紧密粘附并强烈维持上皮或片状的表型。这些细胞降低了向侵袭性滋养层细胞转化的能力,因此减少了改建母体血管所需的酶类产生。同样,本应融合形成分泌激素的表面层细胞反而保持为独立、未融合的单元。分子分析显示,与细胞粘附和结构连接相关的基因与蛋白上调,而与侵袭、激素生成、代谢及应激适应相关的基因则被下调。
从错误的细胞选择到胎盘应激
在模拟早期人类胎盘组织的类器官模型中,过量的 BAP1 导致融合表面细胞区域变小或形成不良,同时类干性滋养层细胞过度增多。与此同时,这些类器官激活了先天免疫和炎性通路,包括与干扰素相关的信号,这些信号在早发型先兆子痫胎盘中也可见。通过结合 RNA 测序与蛋白质测量,研究者建立了一个由 BAP1 驱动的分子“特征谱”,并显示其与早发型先兆子痫中特异的模式高度一致,而在其它妊娠并发症如妊娠期糖尿病或 COVID-19 引起的胎盘改变中则不明显。这将 BAP1 过度活性与病变胎盘的结构功能障碍和炎性环境联系起来。
这对母婴意味着什么
总体来看,该研究将 BAP1 描绘为妊娠期间需要精细调控的“守门人”。当 BAP1 持续偏高时,滋养层细胞无法分化为深度侵入子宫的特化细胞和强有力的激素分泌表面层,结果是胎盘浅薄、压力增大并伴随炎症——这些都是早发型先兆子痫的标志。尽管仍需更多研究以确定 BAP1 的变化是触发因素还是对早期应激的反应,这项研究提供了胎盘细胞身份程序失调与威胁生命的妊娠疾病之间的明确机制联系,开启了寻找新型生物标志物并最终实现靶向治疗的可能性。
引用: Doria-Borrell, P., Ferrero-Micó, A., Navarro-Serna, S. et al. BAP1 dysregulation impairs trophoblast differentiation and contributes to placental dysfunction in preeclampsia. Cell Death Dis 17, 410 (2026). https://doi.org/10.1038/s41419-026-08650-z
关键词: 先兆子痫, 胎盘, 滋养层细胞, BAP1, 妊娠并发症