Clear Sky Science · sv
BAP1-dysregulation försämrar trophoblastdifferentiering och bidrar till placentafunktionstörning vid preeklampsi
När graviditetens stödorgan går fel
Preeklampsi är en farlig graviditetskomplikation som kännetecknas av högt blodtryck och skador på organ som lever och njurar. I centrum för detta tillstånd finns placentan, det temporära organ som närar fostret. Denna studie avslöjar hur felreglering av ett enda reglerande protein, kallat BAP1, kan sabotera utvecklingen av viktiga placentaceller och bidra till den allvarliga, tidigt insjuknande formen av preeklampsi.
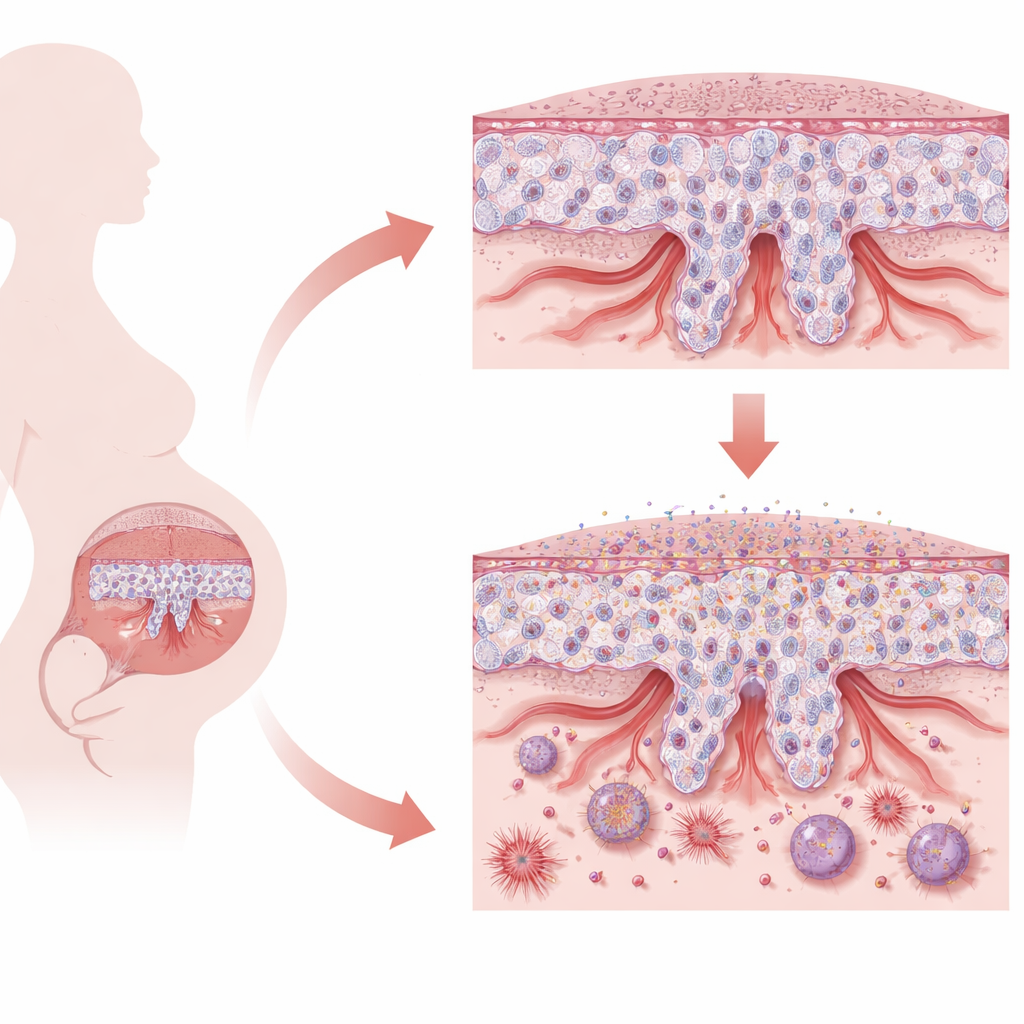
Placentans känsliga balansakt
Placentan är uppbyggd av specialiserade celler som kallas trophoblaster. Tidigt i graviditeten måste stamliknande trophoblaster välja mellan två huvuduppgifter. Några smälter samman för att bilda ett kontinuerligt ytskikt som ansvarar för närings- och gasutbyte. Andra omvandlas till invasiva celler som borrar sig in i moderns livmodervägg och omformar spiralartärerna, vidgar dem för att förse det växande fostret med tillräckligt med blod. Denna noggranna balans mellan att förbli stamlik, byta identitet och invadera lagom långt är avgörande. När processen misslyckas, som vid tidigt insjuknande preeklampsi, blir placentan grund, stressad och mindre kapabel att stödja en frisk graviditet.
Ett placentaprotein som går på för högvarv
Forskarna fokuserade på BAP1, ett protein som är bättre känt för sin roll i cancerbiologi. I friska placentor tidigt i graviditeten är BAP1 rikligt förekommande i stamliknande trophoblaster men sjunker normalt när dessa celler mognar. Genom att använda placentaprover från kvinnor med och utan graviditetskomplikationer fann teamet att BAP1 och dess partnerproteiner ASXL2 och ASXL3 var specifikt förhöjda i placentor från tidigt insjuknande preeklampsi, men inte i den senare insjuknande, mer moderdrivna formen av sjukdomen. Detta mönster tyder på att överaktivitet av BAP1 är nära kopplat till placentabaserade, snarare än rent maternella, orsaker till sjukdomen.
Fryser placentaceller i ett omoget tillstånd
För att se vad BAP1 gör inne i humana placentaceller använde forskarna mänskliga trophoblaststamceller och 3D-placentaorganoider odlade i laboratoriet. När de konstgjort ökade BAP1-nivåerna höll sig cellerna tätt samman och bibehöll starkt en epitelial, eller skivlik, identitet. Dessa celler hade svårare att omvandlas till de invasiva trophoblaster som normalt tränger in i livmodern, och de producerade färre av de enzymer som behövs för att omforma moderns blodkärl. Likaså förblev celler som borde ha smält samman till det hormonproducerande ytskiktet istället separata, osammansmälta enheter. Molekylära analyser visade att gener och proteiner kopplade till celladhesion och strukturella fogar var uppreglerade, medan de som är förenade med invasion, hormonproduktion, metabolism och stressanpassning var nedreglerade.
Från felaktiga cellval till placentastress
I organoidmodeller som efterliknar tidig mänsklig placentavävnad ledde överskott av BAP1 till mindre eller dåligt formade områden av sammansmälta ytceller och en överrepresentation av stamliknande trophoblaster. Samtidigt aktiverade organoiderna medfödda immun- och inflammatoriska vägar, inklusive interferonrelaterade signaler som också ses i placentor från tidigt insjuknande preeklampsi. Genom att kombinera RNA-sekvensering och proteinmätningar byggde forskarna en BAP1-driven molekylär ”signatur” och visade att den starkt överensstämde med mönster som hittades specifikt i tidigt insjuknande preeklampsi, men inte i andra graviditetskomplikationer såsom graviditetsdiabetes eller placentapåverkan av COVID-19. Detta kopplar BAP1-överaktivitet till både den strukturella funktionsstörningen och den inflammatoriska miljön i den sjuka placentan.
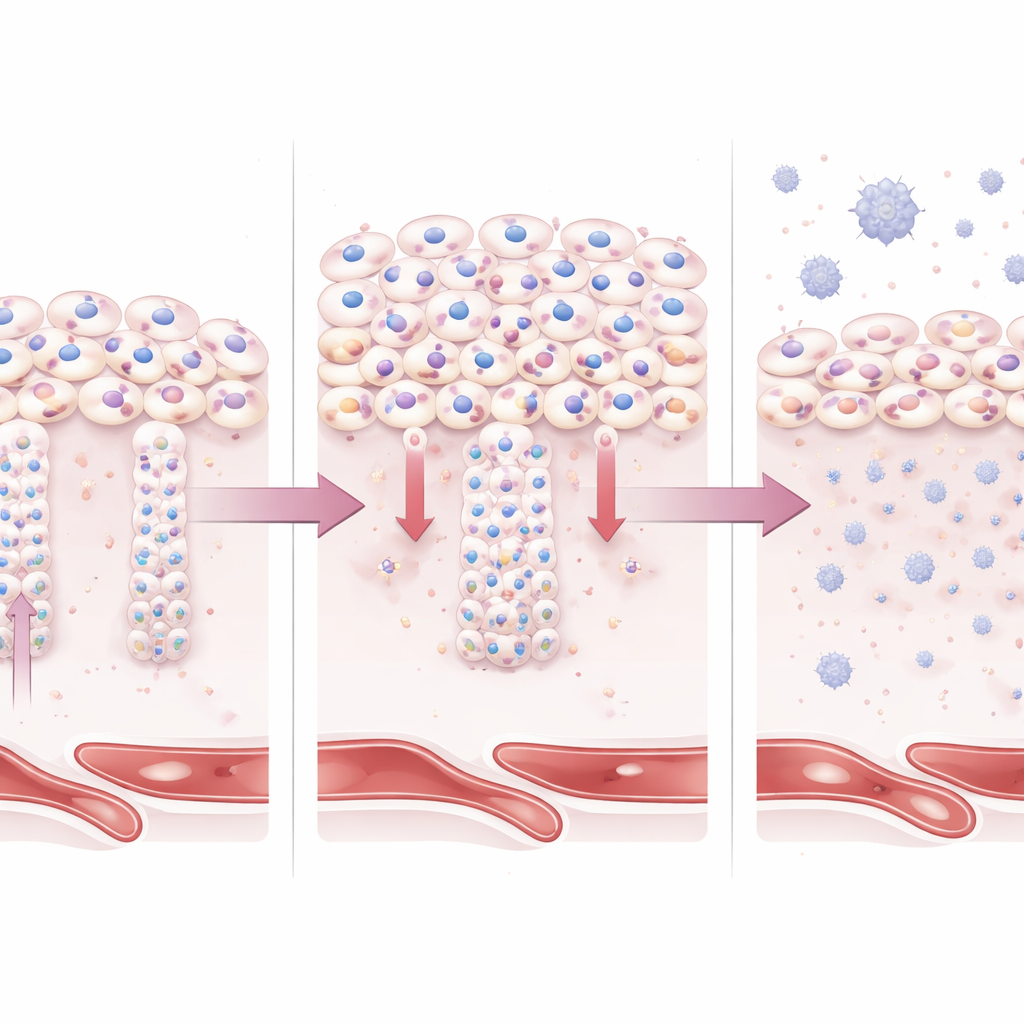
Vad detta betyder för mödrar och barn
Tillsammans framställer arbetet BAP1 som en grindvakt som måste vara noggrant reglerad under graviditeten. När BAP1 förblir för högt misslyckas trophoblaster med att utvecklas till de specialiserade celltyper som behövs för djup uterininvasion och robusta hormonutsöndrande ytskikt. Resultatet blir en placenta som är grund, stressad och inflammerad—kännetecken för tidigt insjuknande preeklampsi. Även om mer forskning behövs för att avgöra om förändringar i BAP1 är en utlösare eller en följd av tidig stress, ger denna studie en tydlig mekanistisk koppling mellan felreglerade cellidentitetsprogram i placentan och en livshotande graviditetsstörning, vilket öppnar dörren för nya biomarkörer och så småningom riktade terapier.
Citering: Doria-Borrell, P., Ferrero-Micó, A., Navarro-Serna, S. et al. BAP1 dysregulation impairs trophoblast differentiation and contributes to placental dysfunction in preeclampsia. Cell Death Dis 17, 410 (2026). https://doi.org/10.1038/s41419-026-08650-z
Nyckelord: preeklampsi, placenta, trofoblast, BAP1, graviditetskomplikationer