Clear Sky Science · es
La desregulación de BAP1 altera la diferenciación del trofoblasto y contribuye al funcionamiento anómalo de la placenta en la preeclampsia
Cuando el órgano de sostén del embarazo falla
La preeclampsia es una complicación peligrosa del embarazo caracterizada por hipertensión y daño en órganos como el hígado y los riñones. En el centro de esta afección está la placenta, el órgano temporal que nutre al bebé. Este estudio revela cómo la mala regulación de una única proteína reguladora, llamada BAP1, puede descarrilar el desarrollo de células placentarias clave y contribuir a la forma severa y de inicio precoz de la preeclampsia.
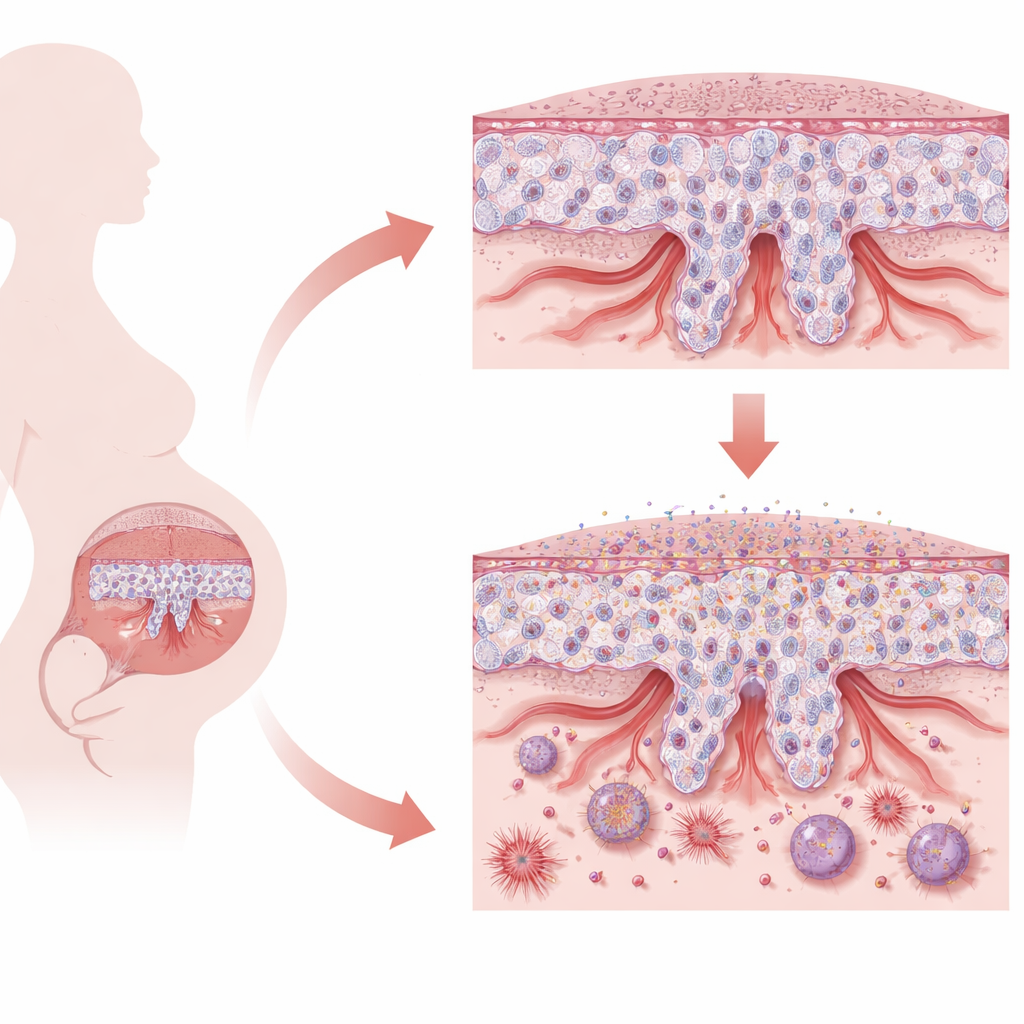
El delicado equilibrio de la placenta
La placenta se construye a partir de células especializadas conocidas como trofoblastos. Al inicio del embarazo, los trofoblastos con cualidades de células madre deben elegir entre dos funciones principales. Algunos se fusionan para formar una capa continua que se encarga del intercambio de nutrientes y gases. Otros se transforman en células invasivas que perforan el útero materno y remodelan las arterias espirales, ensanchándolas para aportar suficiente sangre al feto en crecimiento. Este equilibrio entre permanecer en un estado similar al de las células madre, cambiar de identidad e invadir lo justo es esencial. Cuando el proceso falla, como ocurre en la preeclampsia de inicio precoz, la placenta queda superficial, estresada y menos capaz de sostener un embarazo sano.
Una proteína placentaria elevada en exceso
Los investigadores se centraron en BAP1, una proteína más conocida por su papel en la biología del cáncer. En placentas sanas al inicio del embarazo, BAP1 es abundante en los trofoblastos de tipo stem, pero normalmente disminuye a medida que estas células maduran. Usando muestras placentarias de mujeres con y sin complicaciones gestacionales, el equipo observó que BAP1 y sus proteínas asociadas ASXL2 y ASXL3 estaban específicamente aumentadas en placentas de preeclampsia de inicio precoz, pero no en la forma de aparición más tardía, más impulsada por factores maternos. Este patrón sugiere que la actividad excesiva de BAP1 está estrechamente ligada a causas placentarias, más que puramente maternas, del trastorno.
Congelando las células placentarias en un estado inmaduro
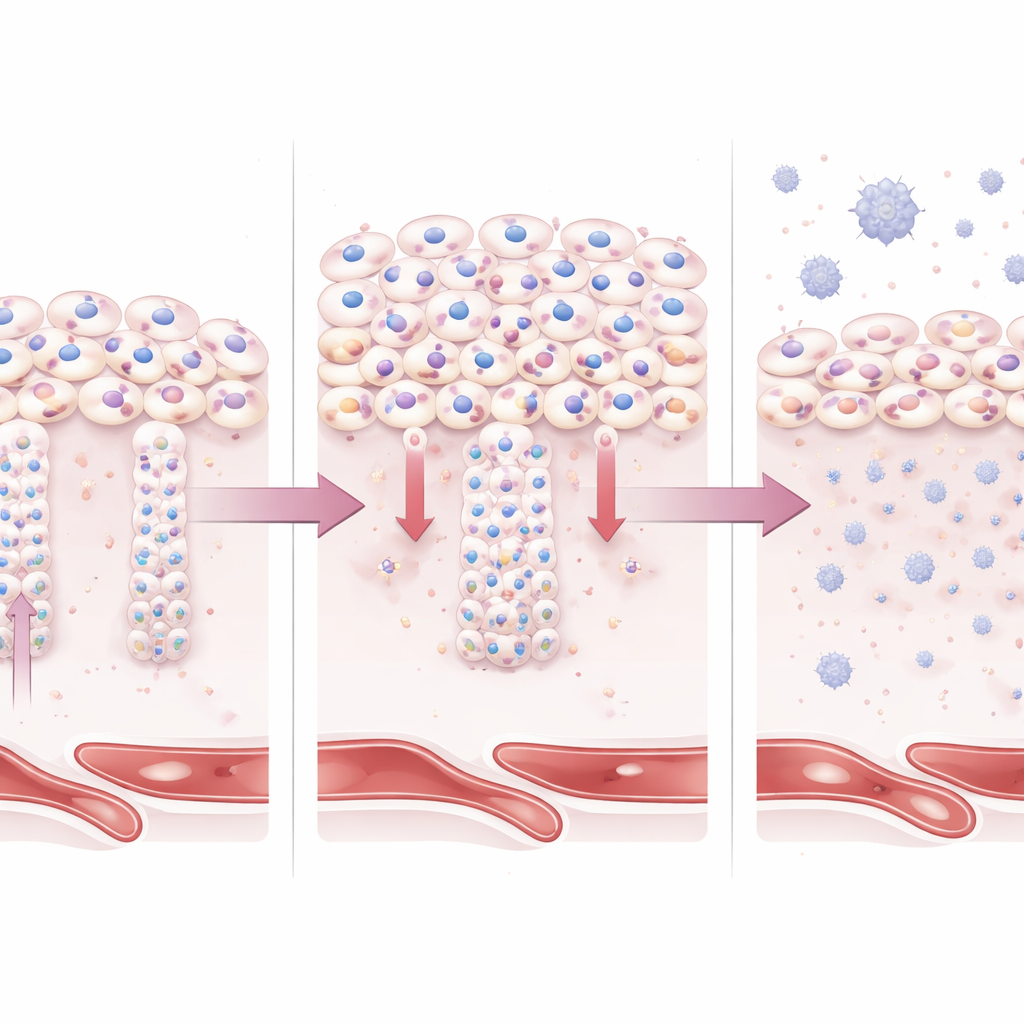
Para ver qué hace BAP1 dentro de las células placentarias humanas, los científicos emplearon células madre trofoblásticas humanas y organoides placentarios 3D cultivados en el laboratorio. Cuando aumentaron artificialmente los niveles de BAP1, las células se mantuvieron fuertemente adheridas entre sí y conservaron con intensidad una identidad epitelial, o en forma de capa. Estas células fueron menos capaces de transformarse en los trofoblastos invasivos que normalmente penetran el útero, y produjeron menos de las enzimas necesarias para remodelar los vasos sanguíneos maternos. De igual modo, las células que deberían haberse fusionado para formar la capa superficial productora de hormonas permanecieron separadas y sin fusionar. Los análisis moleculares mostraron que los genes y proteínas asociados a la adhesión celular y las uniones estructurales se activaron, mientras que los ligados a la invasión, la producción hormonal, el metabolismo y la adaptación al estrés se redujeron.
De decisiones celulares defectuosas al estrés placentario
En modelos de organoides que imitan el tejido placentario humano temprano, el exceso de BAP1 condujo a regiones más pequeñas o mal formadas de células superficiales fusionadas y a una sobrerrepresentación de trofoblastos con rasgos de células madre. Al mismo tiempo, los organoides activaron vías inmunitarias innatas e inflamatorias, incluidas señales relacionadas con interferón que también se observan en placentas de preeclampsia de inicio precoz. Combinando secuenciación de ARN y mediciones proteicas, los investigadores construyeron una “firma” molecular impulsada por BAP1 y mostraron que ésta coincidía fuertemente con los patrones hallados específicamente en la preeclampsia de inicio precoz, pero no en otras complicaciones del embarazo como la diabetes gestacional o los efectos placentarios de la COVID-19. Esto vincula la sobreactividad de BAP1 tanto con el fallo estructural como con la atmósfera inflamatoria de la placenta enferma.
Qué significa esto para madres y bebés
En conjunto, el trabajo dibuja a BAP1 como un guardián que debe ajustarse con precisión durante el embarazo. Cuando BAP1 permanece demasiado elevado, los trofoblastos no se diferencian en los tipos celulares especializados necesarios para una invasión uterina profunda y para superficies secretoras de hormonas robustas. El resultado es una placenta superficial, estresada e inflamada: rasgos distintivos de la preeclampsia de inicio precoz. Si bien hacen falta más investigaciones para determinar si los cambios en BAP1 son un desencadenante o una respuesta al estrés temprano, este estudio proporciona un vínculo mecanicista claro entre programas de identidad celular mal regulados en la placenta y un trastorno del embarazo potencialmente mortal, abriendo la puerta a nuevos biomarcadores y, eventualmente, a terapias dirigidas.
Cita: Doria-Borrell, P., Ferrero-Micó, A., Navarro-Serna, S. et al. BAP1 dysregulation impairs trophoblast differentiation and contributes to placental dysfunction in preeclampsia. Cell Death Dis 17, 410 (2026). https://doi.org/10.1038/s41419-026-08650-z
Palabras clave: preeclampsia, placenta, trofoblasto, BAP1, complicaciones del embarazo