Clear Sky Science · it
La disregolazione di BAP1 compromette la differenziazione dei trofoblasti e contribuisce alla disfunzione placentare nella preeclampsia
Quando l’organo di supporto della gravidanza si guasta
La preeclampsia è una complicanza pericolosa della gravidanza caratterizzata da ipertensione e danni ad organi come fegato e reni. Al centro di questa condizione c’è la placenta, l’organo temporaneo che nutre il bambino. Questo studio rivela come la cattiva regolazione di una singola proteina regolatrice, chiamata BAP1, possa mandare fuori strada lo sviluppo di popolazioni chiave di cellule placentari e contribuire alla forma grave e a insorgenza precoce della preeclampsia.
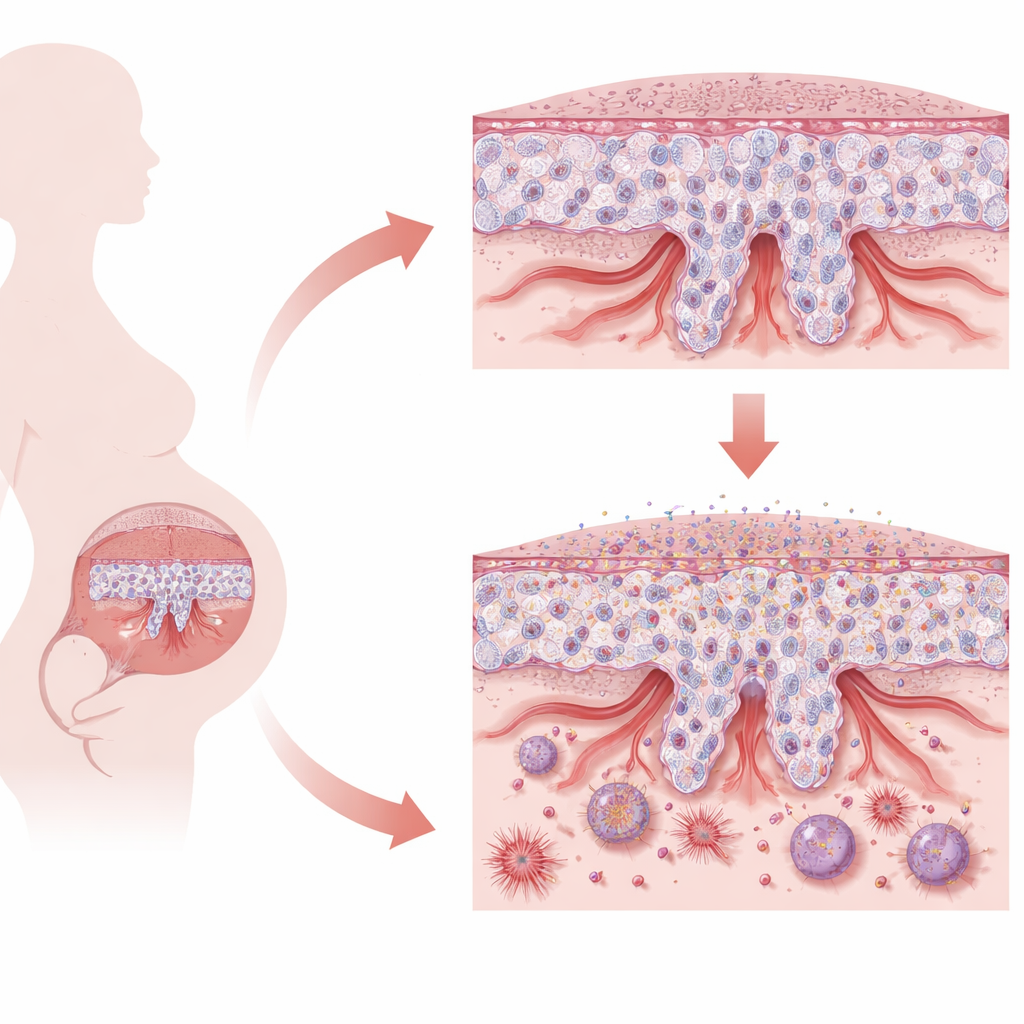
Il delicato equilibrio della placenta
La placenta è composta da cellule specializzate note come trofoblasti. All’inizio della gravidanza, i trofoblasti con proprietà staminali devono scegliere tra due compiti principali. Alcuni si fondono per formare uno strato di superficie continuo che gestisce lo scambio di nutrienti e gas. Altri si trasformano in cellule invasive che penetrano nell’utero materno e rimodellano le arterie spirali, allargandole per portare un flusso sanguigno adeguato al bambino in crescita. Questo equilibrio tra mantenersi in uno stato simile a quello staminale, cambiare identità e invadere nella giusta misura è essenziale. Quando il processo fallisce, come nella preeclampsia a insorgenza precoce, la placenta rimane poco profonda, sotto stress e meno in grado di sostenere una gravidanza sana.
Una proteina placentare troppo attiva
I ricercatori si sono concentrati su BAP1, una proteina più nota per il suo ruolo nella biologia del cancro. Nelle placente sane all’inizio della gravidanza, BAP1 è abbondante nei trofoblasti con caratteristiche staminali ma normalmente diminuisce quando queste cellule maturano. Analizzando campioni placentari di donne con e senza complicazioni della gravidanza, il team ha scoperto che BAP1 e le sue proteine partner ASXL2 e ASXL3 erano specificamente aumentate nelle placente della preeclampsia a insorgenza precoce, ma non nella forma a insorgenza tardiva, più legata a fattori materni. Questo schema suggerisce che un’eccessiva attività di BAP1 sia strettamente collegata a cause placentari, piuttosto che puramente materne, del disturbo.
Congelare le cellule placentari in uno stato immaturo
Per capire cosa fa BAP1 all’interno delle cellule placentari umane, gli scienziati hanno usato cellule staminali trofoblastiche umane e organoidi placentari 3D coltivati in laboratorio. Quando hanno aumentato artificialmente i livelli di BAP1, le cellule hanno mantenuto stretti legami tra loro e hanno conservato fortemente un’identità epiteliale, a “superficie”. Queste cellule erano meno capaci di trasformarsi nei trofoblasti invasivi che normalmente penetrano nell’utero e producevano meno degli enzimi necessari a rimodellare i vasi sanguigni materni. Allo stesso modo, le cellule che avrebbero dovuto fondersi nello strato di superficie produttrice di ormoni rimasero invece come unità separate, non fuse. Le analisi molecolari hanno mostrato che geni e proteine legati all’adesione cellulare e alle giunzioni strutturali erano aumentati, mentre quelli associati all’invasione, alla produzione ormonale, al metabolismo e all’adattamento allo stress risultavano ridotti.
Da scelte cellulari difettose allo stress placentare
Nei modelli di organoidi che imitano il tessuto placentare umano precoce, l’eccesso di BAP1 ha portato a regioni di cellule di superficie fuse più piccole o mal formate e a una sovrarappresentazione di trofoblasti con caratteristiche staminali. Contemporaneamente, gli organoidi hanno attivato vie innate immunitarie e infiammatorie, incluse le vie correlate all’interferone che si osservano anche nelle placente affette da preeclampsia a insorgenza precoce. Combinando il sequenziamento dell’RNA con misure proteiche, i ricercatori hanno costruito una “firma” molecolare guidata da BAP1 e hanno mostrato che corrispondeva fortemente ai modelli riscontrati specificamente nella preeclampsia a insorgenza precoce, ma non in altre complicazioni della gravidanza come il diabete gestazionale o gli effetti placentari del COVID-19. Questo collega l’eccessiva attività di BAP1 sia al malfunzionamento strutturale sia all’atmosfera infiammatoria della placenta malata.
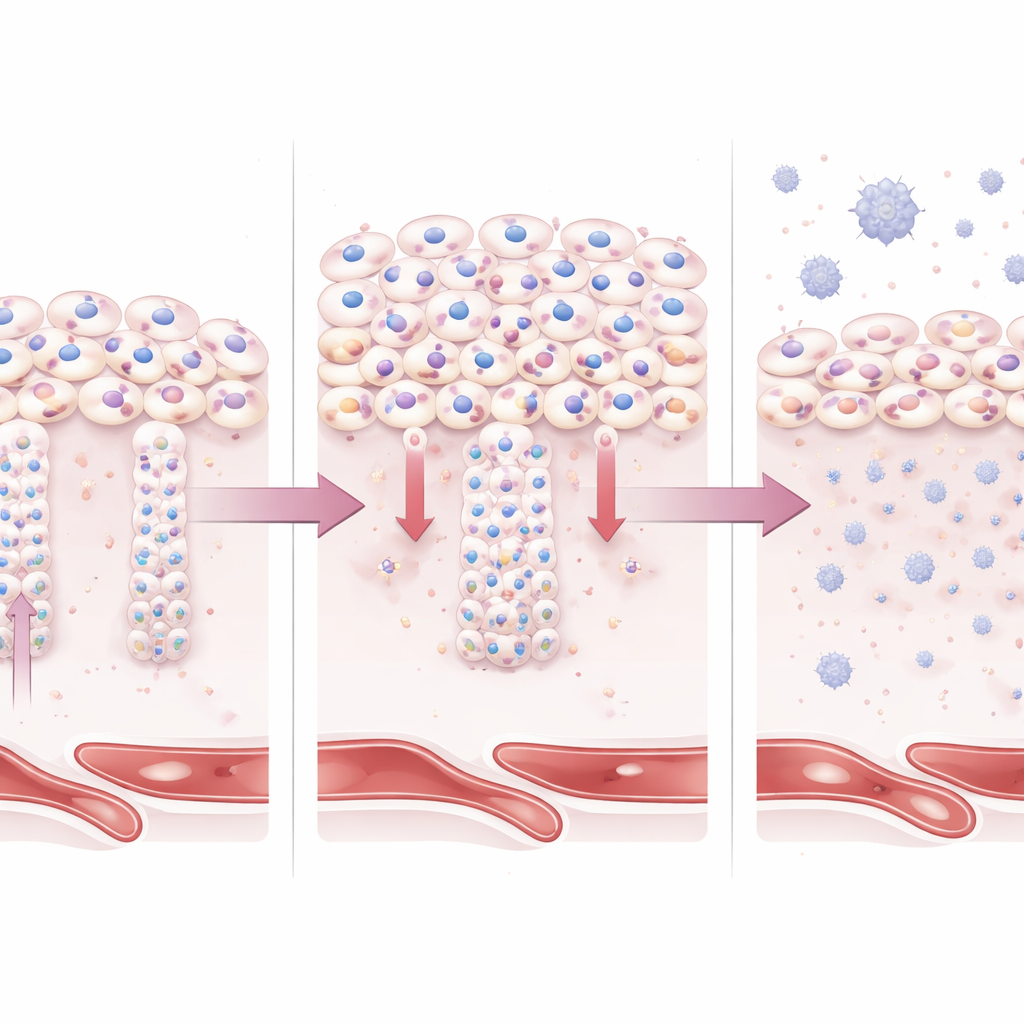
Cosa significa per madri e bambini
Nel complesso, il lavoro descrive BAP1 come un guardiano che deve essere finemente regolato durante la gravidanza. Quando BAP1 rimane troppo alto, i trofoblasti non si differenziano nei tipi cellulari specializzati necessari per un’invasione uterina profonda e per superfici secernenti ormoni ben funzionanti. Il risultato è una placenta poco profonda, sotto stress e infiammata—segni distintivi della preeclampsia a insorgenza precoce. Pur servendo ulteriore ricerca per capire se i cambiamenti di BAP1 siano una causa scatenante o una risposta allo stress precoce, questo studio fornisce un chiaro collegamento meccanicistico tra la disregolazione dei programmi di identità cellulare nella placenta e un disturbo della gravidanza che può mettere a rischio la vita, aprendo la strada a nuovi biomarcatori e, in prospettiva, a terapie mirate.
Citazione: Doria-Borrell, P., Ferrero-Micó, A., Navarro-Serna, S. et al. BAP1 dysregulation impairs trophoblast differentiation and contributes to placental dysfunction in preeclampsia. Cell Death Dis 17, 410 (2026). https://doi.org/10.1038/s41419-026-08650-z
Parole chiave: preeclampsia, placenta, trofoblasto, BAP1, complicazioni della gravidanza