Clear Sky Science · nl
BAP1-dysregulatie belemmert differentiatie van trophoblasten en draagt bij aan placentaire disfunctie bij pre-eclampsie
Wanneer het ondersteunende orgaan van de zwangerschap ontspoort
Pre-eclampsie is een gevaarlijke zwangerschapscomplicatie die wordt gekenmerkt door hoge bloeddruk en schade aan organen zoals de lever en de nieren. Centraal in deze aandoening staat de placenta, het tijdelijke orgaan dat de baby voedt. Deze studie onthult hoe ontregeling van één regulerend eiwit, BAP1 genaamd, de ontwikkeling van sleutelcellen in de placenta kan ontsporen en kan bijdragen aan de ernstige, vroeg optredende vorm van pre-eclampsie.
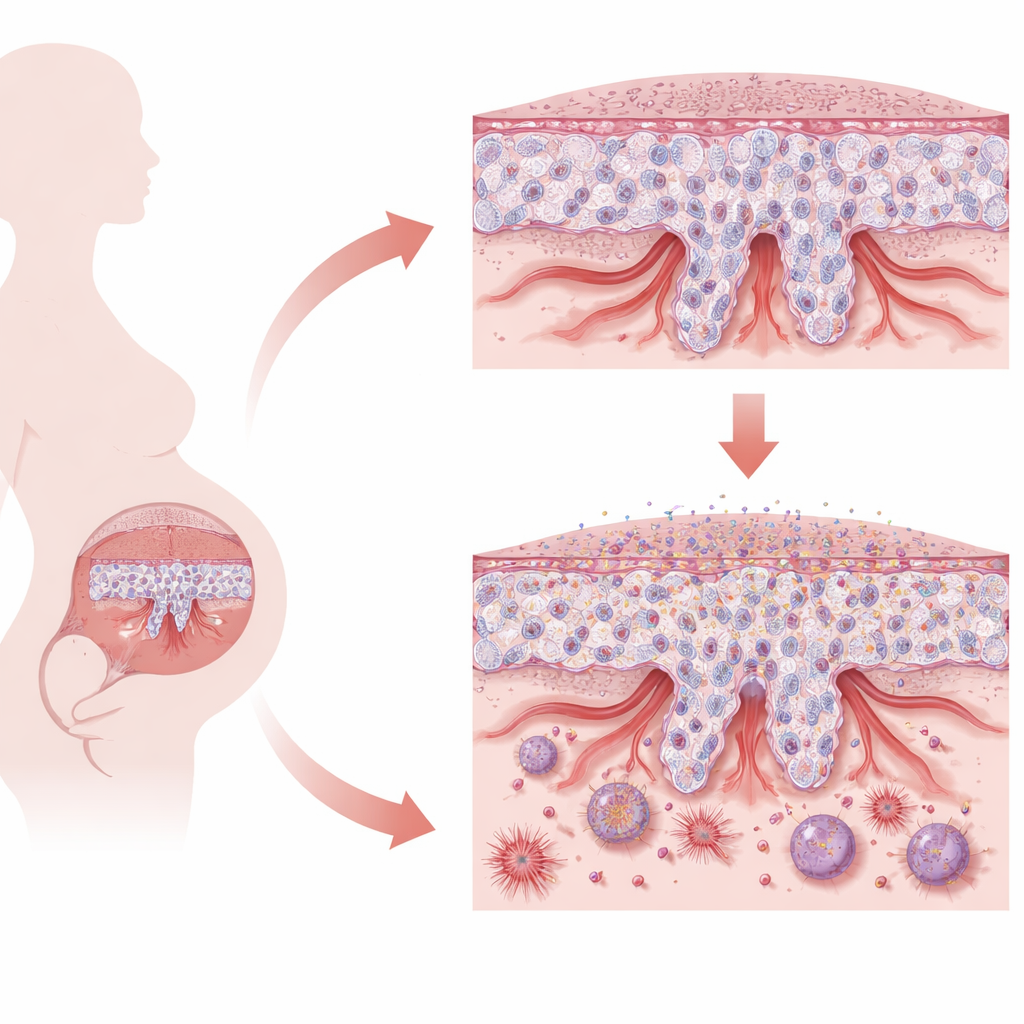
Het fijne evenwicht van de placenta
De placenta is opgebouwd uit gespecialiseerde cellen die trophoblasten worden genoemd. Vroeg in de zwangerschap moeten stamachtige trophoblasten kiezen tussen twee hoofdrollen. Sommige versmelten tot een continue oppervlaktelaag die instaat voor de uitwisseling van voedingsstoffen en gassen. Andere veranderen in invasieve cellen die in de baarmoeder van de moeder binnendringen en de spiraalarteriën herstructureren, waardoor deze wijder worden en meer bloed naar de groeiende foetus brengen. Dit zorgvuldige evenwicht tussen het behouden van een stamachtige toestand, het veranderen van identiteit en het precies ver genoeg binnendringen is essentieel. Wanneer dit proces faalt, zoals bij vroeg optredende pre-eclampsie, wordt de placenta ondiep, gestrest en minder in staat een gezonde zwangerschap te ondersteunen.
Een placentaire eiwit dat te hoog wordt opgeregeld
De onderzoekers richtten zich op BAP1, een eiwit dat vooral bekend is om zijn rol in de kankerbiologie. In gezonde placenta’s vroeg in de zwangerschap is BAP1 overvloedig aanwezig in stamachtige trophoblasten, maar normaal gesproken daalt het wanneer deze cellen rijpen. Met placentasamples van vrouwen met en zonder zwangerschapscomplicaties vonden de onderzoekers dat BAP1 en zijn partner-eiwitten ASXL2 en ASXL3 specifiek verhoogd waren in placenta’s van vroeg optredende pre-eclampsie, maar niet in de later optredende, meer moedergerelateerde vorm van de ziekte. Dit patroon suggereert dat excessieve BAP1-activiteit nauw samenhangt met placentaire, en niet puur maternale, oorzaken van de aandoening.
Placentaire cellen bevroren in een onrijpe staat
Om te onderzoeken wat BAP1 doet in menselijke placentacellen, gebruikten de wetenschappers menselijke trophoblast-stamcellen en 3D-placentaorganoïden die in het laboratorium werden gekweekt. Toen ze kunstmatig het BAP1-niveau verhoogden, klampten de cellen zich stevig aan elkaar vast en behielden ze sterk een epitheliale, velachtige identiteit. Deze cellen waren minder in staat om zich te transformeren tot de invasieve trophoblasten die normaal in de baarmoeder doordringen, en produceerden minder van de enzymen die nodig zijn om de bloedvaten van de moeder te herstructureren. Evenzo bleven cellen die zich tot de hormoonproducerende oppervlaktelaag hadden moeten versmelten, als afzonderlijke, niet-gefuseerde eenheden bestaan. Moleculaire analyses toonden aan dat genen en eiwitten die verband houden met celadhesie en structurele verbindingen werden verhoogd, terwijl die gekoppeld aan invasie, hormoonproductie, metabolisme en stressadaptatie werden verlaagd.
Van foutieve celkeuzes naar placentaire stress
In organoïdemodellen die vroeg menselijk placentaweefsel nabootsen, leidde overtollig BAP1 tot kleinere of slecht gevormde regio’s van versmolten oppervlaktecellen en een oververtegenwoordiging van stamachtige trophoblasten. Tegelijkertijd activeerden de organoïden innate immuun- en ontstekingsroutes, inclusief interferon-gerelateerde signalen die ook worden gezien in placenta’s bij vroeg optredende pre-eclampsie. Door RNA-sequencing en eiwitmetingen te combineren, stelden de onderzoekers een door BAP1 gedreven moleculair “handtekening” op en toonden ze aan dat deze sterk overeenkwam met patronen die specifiek in vroeg optredende pre-eclampsie werden gevonden, maar niet bij andere zwangerschapscomplicaties zoals zwangerschapsdiabetes of placentaire effecten van COVID-19. Dit koppelt overactiviteit van BAP1 aan zowel de structurele disfunctie als de ontstekingsrijke omgeving van de zieke placenta.
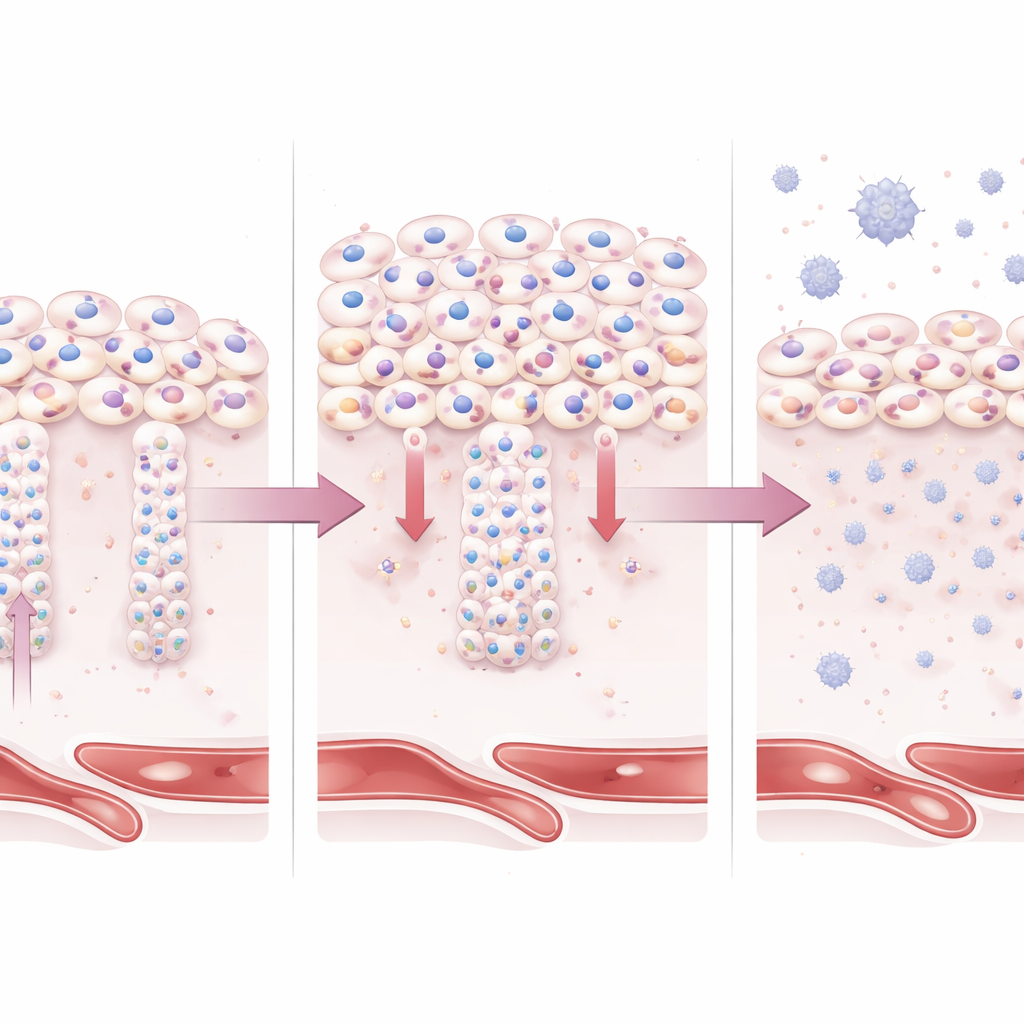
Wat dit betekent voor moeders en baby’s
Alles bij elkaar schetst dit werk BAP1 als een poortwachter die tijdens de zwangerschap zorgvuldig moet worden afgesteld. Wanneer BAP1 te hoog blijft, slagen trophoblasten er niet in om uit te groeien tot de gespecialiseerde celtypen die nodig zijn voor diepe uteriene invasie en robuuste, hormoon-secernerende oppervlakken. Het resultaat is een placenta die ondiep, gestrest en ontstoken is — kenmerkend voor vroeg optredende pre-eclampsie. Hoewel meer onderzoek nodig is om te bepalen of BAP1-veranderingen een trigger zijn of een reactie op vroege stress, levert deze studie een duidelijk mechanistisch verband tussen ontregelde celidentiteitsprogramma’s in de placenta en een levensbedreigende zwangerschapsstoornis, en opent ze de deur naar nieuwe biomarkers en uiteindelijk gerichte behandelingen.
Bronvermelding: Doria-Borrell, P., Ferrero-Micó, A., Navarro-Serna, S. et al. BAP1 dysregulation impairs trophoblast differentiation and contributes to placental dysfunction in preeclampsia. Cell Death Dis 17, 410 (2026). https://doi.org/10.1038/s41419-026-08650-z
Trefwoorden: pre-eclampsie, placenta, trophoblast, BAP1, zwangerschapscomplicaties