Clear Sky Science · pt
Desregulação de BAP1 prejudica a diferenciação de trofoblastos e contribui para a disfunção placentária na pré-eclâmpsia
Quando o órgão de suporte da gravidez sai dos trilhos
A pré-eclâmpsia é uma complicação perigosa da gravidez caracterizada por pressão alta e lesão a órgãos como fígado e rins. No cerne dessa condição está a placenta, o órgão temporário que nutre o bebê. Este estudo revela como a desregulação de uma única proteína reguladora, chamada BAP1, pode atrapalhar o desenvolvimento de células placentárias-chave e contribuir para a forma grave e de início precoce da pré-eclâmpsia.
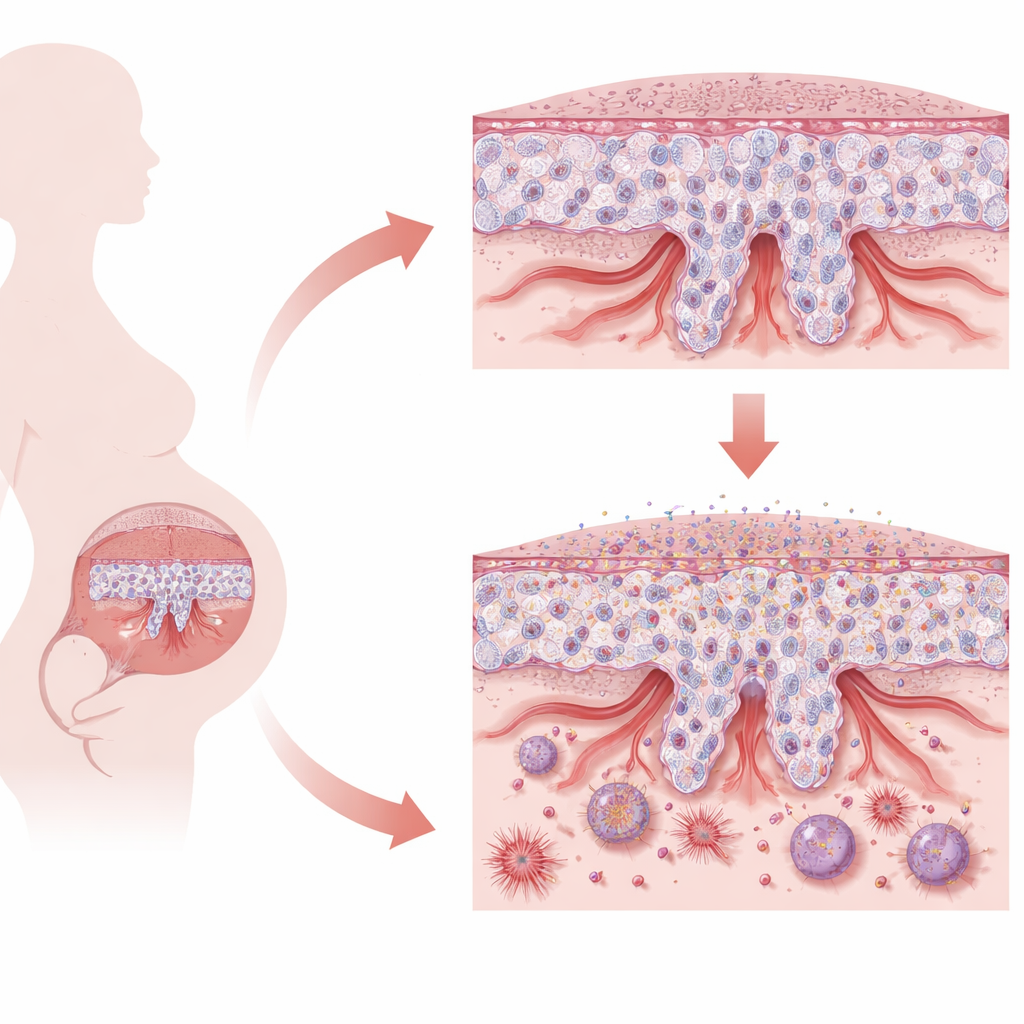
O delicado jogo de equilíbrio da placenta
A placenta é formada por células especializadas conhecidas como trofoblastos. No início da gravidez, trofoblastos com características de células-tronco devem escolher entre duas funções principais. Alguns se fundem para formar uma camada contínua que lida com a troca de nutrientes e gases. Outros se transformam em células invasivas que penetram o útero materno e remodelam as artérias espirais, alargando-as para fornecer sangue em quantidade suficiente ao feto em crescimento. Esse equilíbrio cuidadoso entre permanecer em um estado semelhante a células-tronco, mudar de identidade e invadir na medida certa é essencial. Quando o processo falha, como na pré-eclâmpsia de início precoce, a placenta fica superficial, estressada e menos capaz de sustentar uma gestação saudável.
Uma proteína placentária elevada além do normal
Os pesquisadores concentraram-se em BAP1, uma proteína mais conhecida por seu papel na biologia do câncer. Em placentas saudáveis no início da gestação, BAP1 é abundante em trofoblastos com caráter de células-tronco, mas normalmente diminui à medida que essas células amadurecem. Usando amostras placentárias de mulheres com e sem complicações gestacionais, a equipe constatou que BAP1 e suas proteínas parceiras ASXL2 e ASXL3 estavam especificamente aumentadas em placentas de pré-eclâmpsia de início precoce, mas não na forma de início tardio, mais dirigida por fatores maternos. Esse padrão sugere que a atividade excessiva de BAP1 está intimamente ligada a causas placentárias, em vez de serem puramente maternas, da doença.
Congelando células placentárias num estado imaturo
Para entender o papel de BAP1 dentro de células placentárias humanas, os cientistas usaram células-tronco de trofoblasto humano e organoides placentares 3D cultivados em laboratório. Quando elevaram artificialmente os níveis de BAP1, as células permaneceram fortemente aderidas umas às outras e mantiveram uma identidade epitelial, ou em forma de lâmina. Essas células tiveram menor capacidade de se transformar nos trofoblastos invasivos que normalmente penetram o útero, e produziram menos das enzimas necessárias para remodelar os vasos sanguíneos maternos. Da mesma forma, células que deveriam ter se fundido na camada superficial produtora de hormônios permaneceram separadas, sem fusão. Análises moleculares mostraram que genes e proteínas ligados à adesão celular e às junções estruturais estavam aumentados, enquanto aqueles associados à invasão, produção hormonal, metabolismo e adaptação ao estresse foram reduzidos.
De escolhas celulares defeituosas ao estresse placentário
Em modelos de organoide que imitam o tecido placentário humano precoce, o excesso de BAP1 levou a regiões menores ou mal formadas de células superficiais fundidas e a uma sobrerrepresentação de trofoblastos com características de células-tronco. Ao mesmo tempo, os organoides ativaram vias imunes inatas e inflamatórias, incluindo sinais relacionados a interferons que também são observados em placentas de pré-eclâmpsia de início precoce. Ao combinar sequenciamento de RNA e medições de proteínas, os pesquisadores construíram uma “assinatura” molecular dirigida por BAP1 e mostraram que ela correspondia fortemente a padrões encontrados especificamente na pré-eclâmpsia de início precoce, mas não em outras complicações gestacionais, como diabetes gestacional ou efeitos placentários da COVID-19. Isso liga a hiperatividade de BAP1 tanto à disfunção estrutural quanto ao ambiente inflamatório da placenta doente.
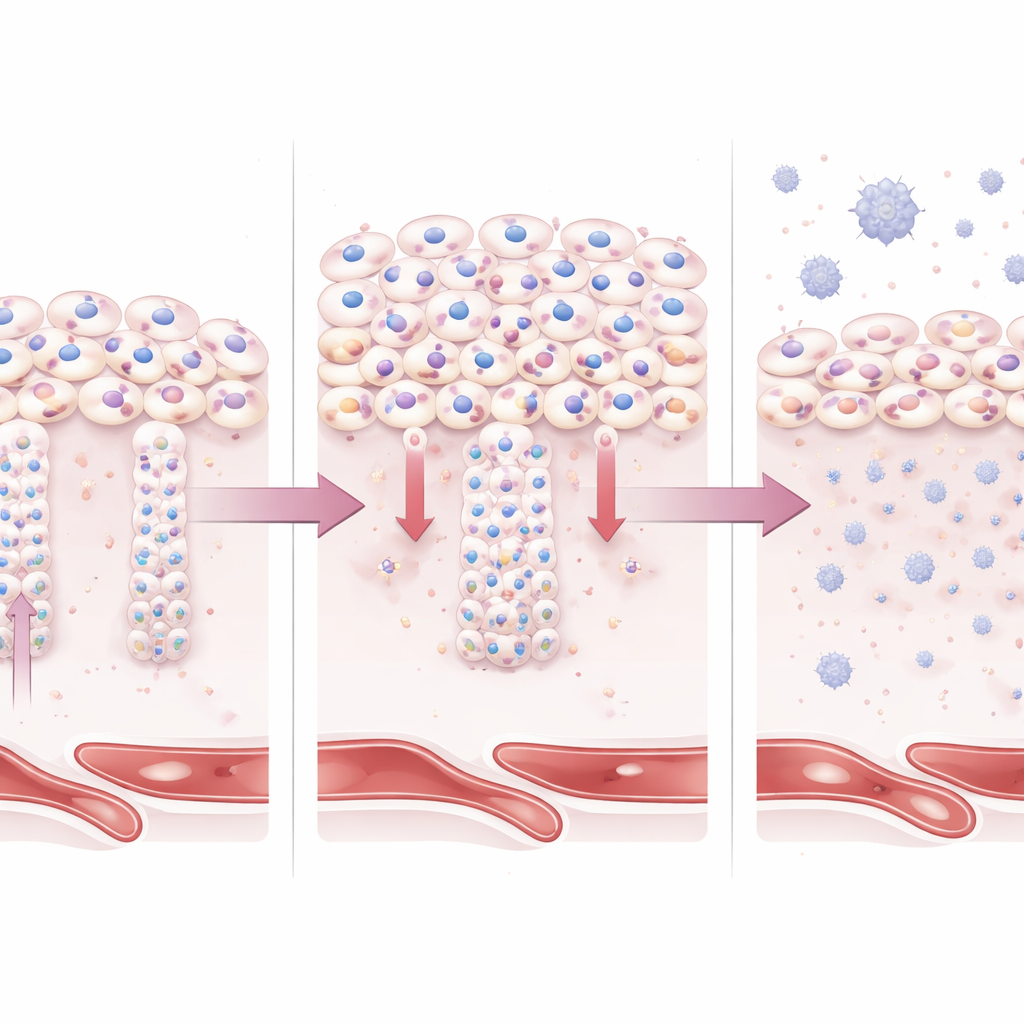
O que isso significa para mães e bebês
No conjunto, o trabalho pinta BAP1 como um guardião que precisa ser cuidadosamente calibrado durante a gravidez. Quando BAP1 permanece em níveis elevados, os trofoblastos não se diferenciam nos tipos celulares especializados necessários para a invasão uterina profunda e para a formação de superfícies secretoras de hormônios robustas. O resultado é uma placenta superficial, estressada e inflamada — marcas registradas da pré-eclâmpsia de início precoce. Embora sejam necessárias mais pesquisas para determinar se as alterações em BAP1 são um gatilho ou uma resposta ao estresse inicial, este estudo fornece um elo mecânico claro entre programas de identidade celular desregulados na placenta e um distúrbio gestacional potencialmente fatal, abrindo caminho para novos biomarcadores e, eventualmente, terapias direcionadas.
Citação: Doria-Borrell, P., Ferrero-Micó, A., Navarro-Serna, S. et al. BAP1 dysregulation impairs trophoblast differentiation and contributes to placental dysfunction in preeclampsia. Cell Death Dis 17, 410 (2026). https://doi.org/10.1038/s41419-026-08650-z
Palavras-chave: pré-eclâmpsia, placenta, trofoblasto, BAP1, complicações na gravidez