Clear Sky Science · pl
Dysregulacja BAP1 zaburza różnicowanie trofoblastów i przyczynia się do dysfunkcji łożyska w stanach rzucawkowych
Kiedy organ podtrzymujący ciążę zawodzi
Stan rzucawkowy (preeclampsia) to groźne powikłanie ciąży, charakteryzujące się wysokim ciśnieniem krwi i uszkodzeniem narządów takich jak wątroba i nerki. U podstaw tego schorzenia leży łożysko — tymczasowy organ odżywiający dziecko. W badaniu odkryto, jak zaburzenie regulacji jednego białka kontrolnego, nazwanego BAP1, może zniweczyć rozwój kluczowych komórek łożyska i przyczyniać się do ciężkiej postaci stanu rzucawkowego o wczesnym początku.
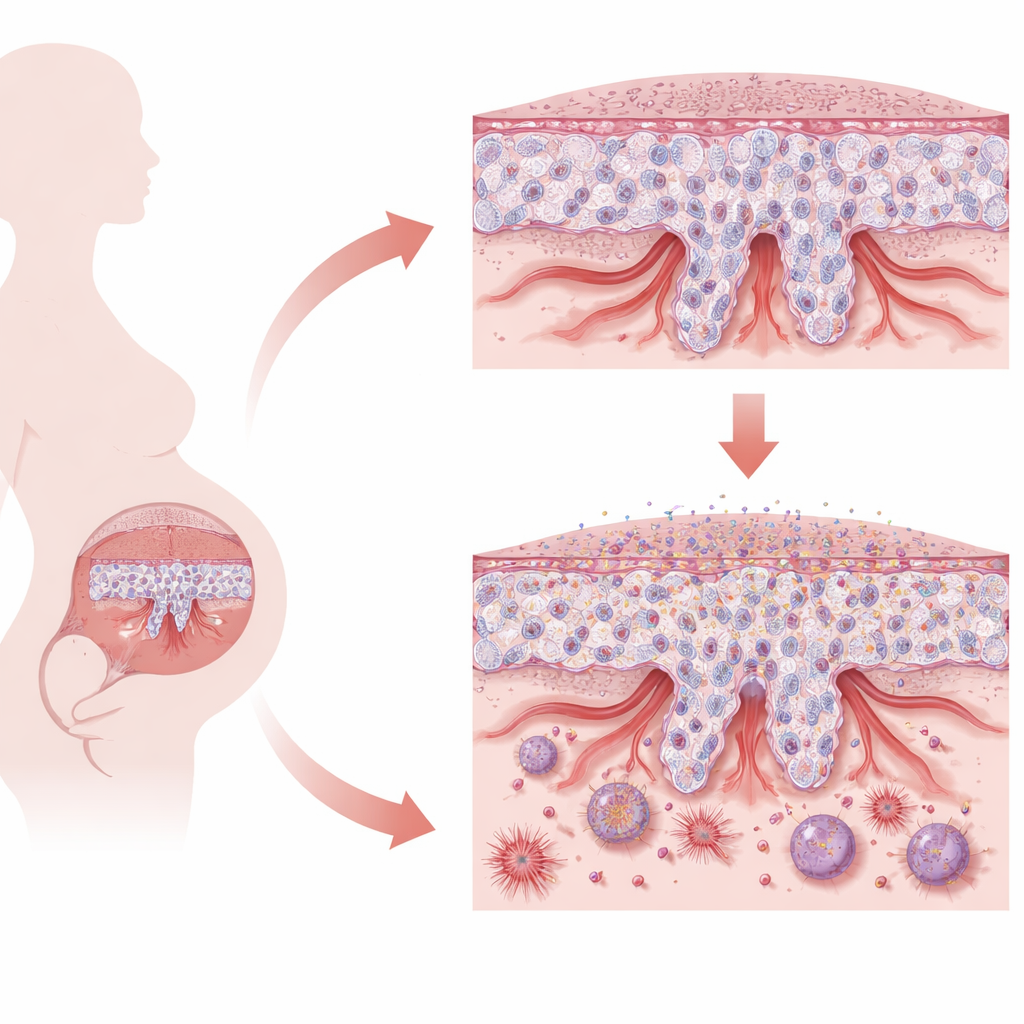
Delikatna równowaga łożyska
Łożysko zbudowane jest ze wyspecjalizowanych komórek zwanych trofoblastami. We wczesnej ciąży trofoblasty o cechach komórek macierzystych muszą dokonać wyboru między dwiema głównymi rolami. Niektóre z nich łączą się, tworząc ciągłą warstwę powierzchniową odpowiedzialną za wymianę substancji i gazów. Inne przekształcają się w inwazyjne komórki, które wnikają w macicę matki i przebudowują tętniczki spiralne, rozszerzając je, by dostarczyć rosnącemu płodowi wystarczającą ilość krwi. Ta ostrożna równowaga między zachowaniem stanu podobnego do komórek macierzystych, zmianą tożsamości a inwazją na odpowiednią głębokość jest kluczowa. Gdy proces zawodzi, jak w przypadku wczesnego rzucawkowego, łożysko staje się płytkie, zestresowane i gorzej wspiera prawidłowy przebieg ciąży.
Łożyskowe białko podkręcone za bardzo
Naukowcy skupili się na BAP1, białku lepiej znanym z badań nad nowotworami. W zdrowych łożyskach we wczesnej ciąży BAP1 jest obfity w trofoblastach o cechach komórek macierzystych, ale zazwyczaj spada w miarę dojrzewania tych komórek. Analiza próbek łożyska od kobiet z komplikacjami ciąży i bez nich wykazała, że BAP1 oraz jego białkowi partnerzy ASXL2 i ASXL3 były specyficznie podwyższone w łożyskach z wczesnym początkiem stanu rzucawkowego, lecz nie w późniejszej, bardziej zależnej od czynników matczynych postaci choroby. Ten wzorzec sugeruje, że nadmierna aktywność BAP1 jest ściśle związana z przyczynami łożyskowymi, a nie wyłącznie matczynymi, zaburzenia.
Zamrażanie komórek łożyska w stanie niedojrzałym
Aby sprawdzić, co BAP1 robi w ludzkich komórkach łożyska, badacze użyli ludzkich trofoblastycznych komórek macierzystych oraz trójwymiarowych organoidów łożyskowych hodowanych w laboratorium. Gdy sztucznie podnieśli poziom BAP1, komórki mocniej przylegały do siebie i wyraźnie utrzymywały epitelialną, czyli warstwową, tożsamość. Te komórki miały mniejszą zdolność przekształcenia się w inwazyjne trofoblasty, które normalnie penetrują macicę, i wytwarzały mniej enzymów niezbędnych do przebudowy naczyń krwionośnych matki. Podobnie komórki, które powinny zlać się w warstwę powierzchniową produkującą hormony, pozostawały jako oddzielne, niepołączone jednostki. Analizy molekularne wykazały, że geny i białka związane z adhezją komórek i połączeniami strukturalnymi były w górze, podczas gdy te związane z inwazją, produkcją hormonów, metabolizmem i adaptacją do stresu były wyciszone.
Z wadliwych wyborów komórkowych do stresu łożyska
W modelach organoidów naśladujących wczesną tkankę łożyskową u ludzi nadmiar BAP1 prowadził do mniejszych lub źle ukształtowanych obszarów zlanego nabłonka powierzchniowego i nadreprezentacji trofoblastów o cechach komórek macierzystych. Jednocześnie organoidy aktywowały wrodzone szlaki immunologiczne i zapalne, w tym sygnalizację związaną z interferonami, obserwowaną również w łożyskach z wczesnym początkiem stanu rzucawkowego. Łącząc sekwencjonowanie RNA i pomiary białek, badacze stworzyli molekularny „sygnaturę” napędzaną przez BAP1 i pokazali, że silnie odpowiada ona wzorcom występującym specyficznie we wczesnym rzucawkowym, ale nie w innych powikłaniach ciąży, takich jak cukrzyca ciężarnych czy wpływ COVID-19 na łożysko. To łączy nadaktywność BAP1 zarówno z dysfunkcją strukturalną, jak i zapalnym klimatem chorego łożyska.
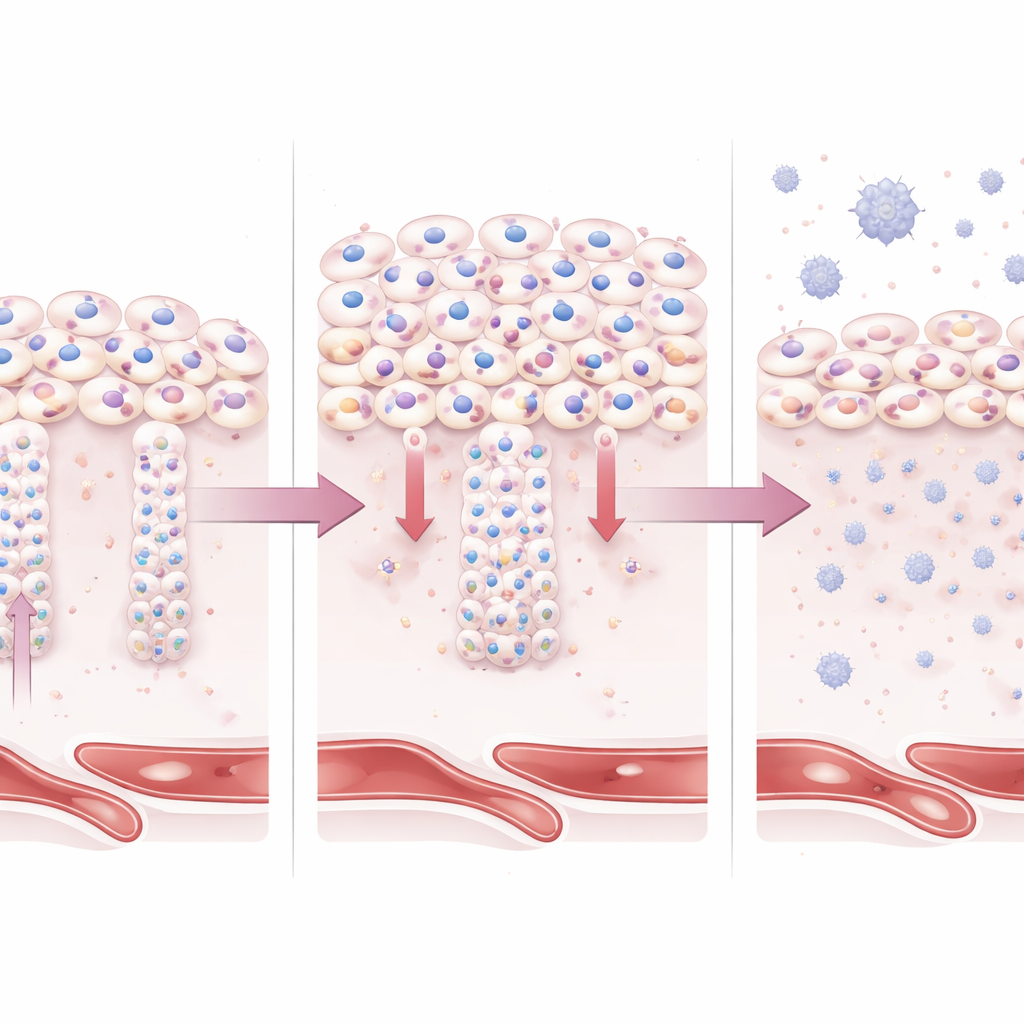
Co to oznacza dla matek i dzieci
Podsumowując, praca przedstawia BAP1 jako strażnika, którego trzeba precyzyjnie regulować podczas ciąży. Gdy poziom BAP1 pozostaje zbyt wysoki, trofoblasty nie rozwijają się w wyspecjalizowane typy komórek potrzebne do głębokiej inwazji macicznej i powstania wydajnych powierzchni wydzielających hormony. W efekcie łożysko jest płytkie, zestresowane i zapalne — cechy charakterystyczne wczesnego stanu rzucawkowego. Choć potrzebne są dalsze badania, aby ustalić, czy zmiany w BAP1 są przyczyną, czy odpowiedzią na wczesny stres, to badanie dostarcza wyraźnego mechanistycznego powiązania między zaburzeniem programów tożsamości komórkowej w łożysku a zagrażającym życiu zaburzeniem ciąży, otwierając drogę do nowych markerów i w przyszłości ukierunkowanych terapii.
Cytowanie: Doria-Borrell, P., Ferrero-Micó, A., Navarro-Serna, S. et al. BAP1 dysregulation impairs trophoblast differentiation and contributes to placental dysfunction in preeclampsia. Cell Death Dis 17, 410 (2026). https://doi.org/10.1038/s41419-026-08650-z
Słowa kluczowe: stan rzucawkowy, łożysko, trofoblast, BAP1, powikłania ciąży