Clear Sky Science · fr
La dysrégulation de BAP1 altère la différenciation des trophoblastes et contribue au dysfonctionnement placentaire dans la prééclampsie
Quand l’organe de soutien de la grossesse se dérègle
La prééclampsie est une complication grave de la grossesse caractérisée par une hypertension et des atteintes d’organes tels que le foie et les reins. Au cœur de cette pathologie se trouve le placenta, l’organe temporaire qui nourrit le fœtus. Cette étude révèle comment un mauvais contrôle d’une seule protéine régulatrice, nommée BAP1, peut perturber le développement de cellules placentaires clés et contribuer à la forme sévère et d’apparition précoce de la prééclampsie.
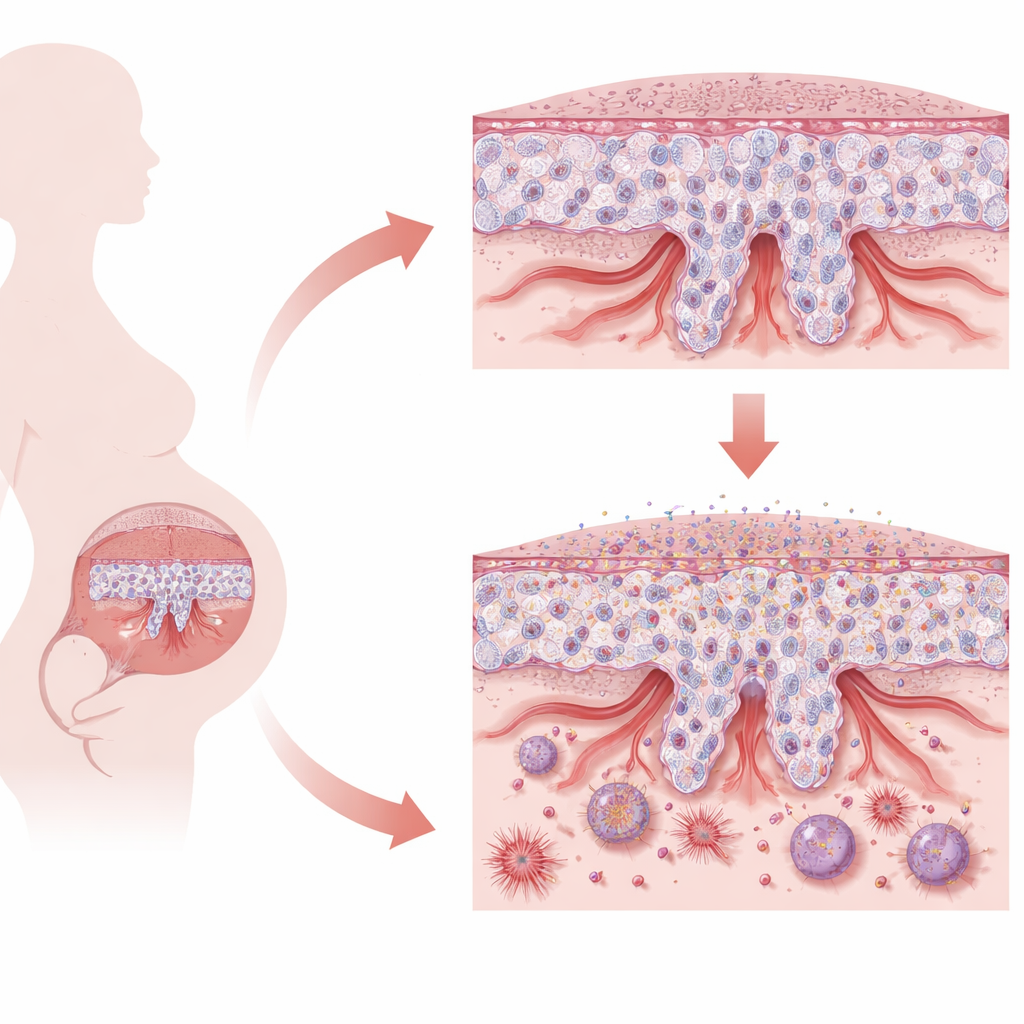
L’équilibre délicat du placenta
Le placenta est constitué de cellules spécialisées appelées trophoblastes. Au début de la grossesse, des trophoblastes de type souche doivent choisir entre deux fonctions principales. Certains fusionnent pour former une couche continue qui assure les échanges nutritifs et gazeux. D’autres se transforment en cellules invasives qui pénètrent dans l’utérus maternel et remodelent les artères spiralées, les élargissant pour fournir un flux sanguin suffisant au fœtus en croissance. Cet équilibre entre le maintien d’un état souche, le changement d’identité et une invasion limitée est essentiel. Lorsque ce processus échoue, comme dans la prééclampsie d’apparition précoce, le placenta devient superficiel, stressé et moins capable de soutenir une grossesse saine.
Une protéine placentaire trop active
Les chercheurs se sont intéressés à BAP1, une protéine mieux connue pour son rôle en cancérologie. Dans les placentas sains précoces, BAP1 est abondant dans les trophoblastes de type souche mais décroît normalement au fur et à mesure de la maturation cellulaire. En analysant des prélèvements placentaires de femmes avec et sans complications de grossesse, l’équipe a constaté que BAP1 et ses partenaires ASXL2 et ASXL3 étaient spécifiquement augmentés dans les placentas de la prééclampsie d’apparition précoce, et non dans la forme d’apparition plus tardive, davantage liée à des facteurs maternels. Ce schéma suggère qu’une activité excessive de BAP1 est étroitement liée à des causes placentaires, plutôt qu’à des causes purement maternelles, du trouble.
Geler les cellules placentaires dans un état immature
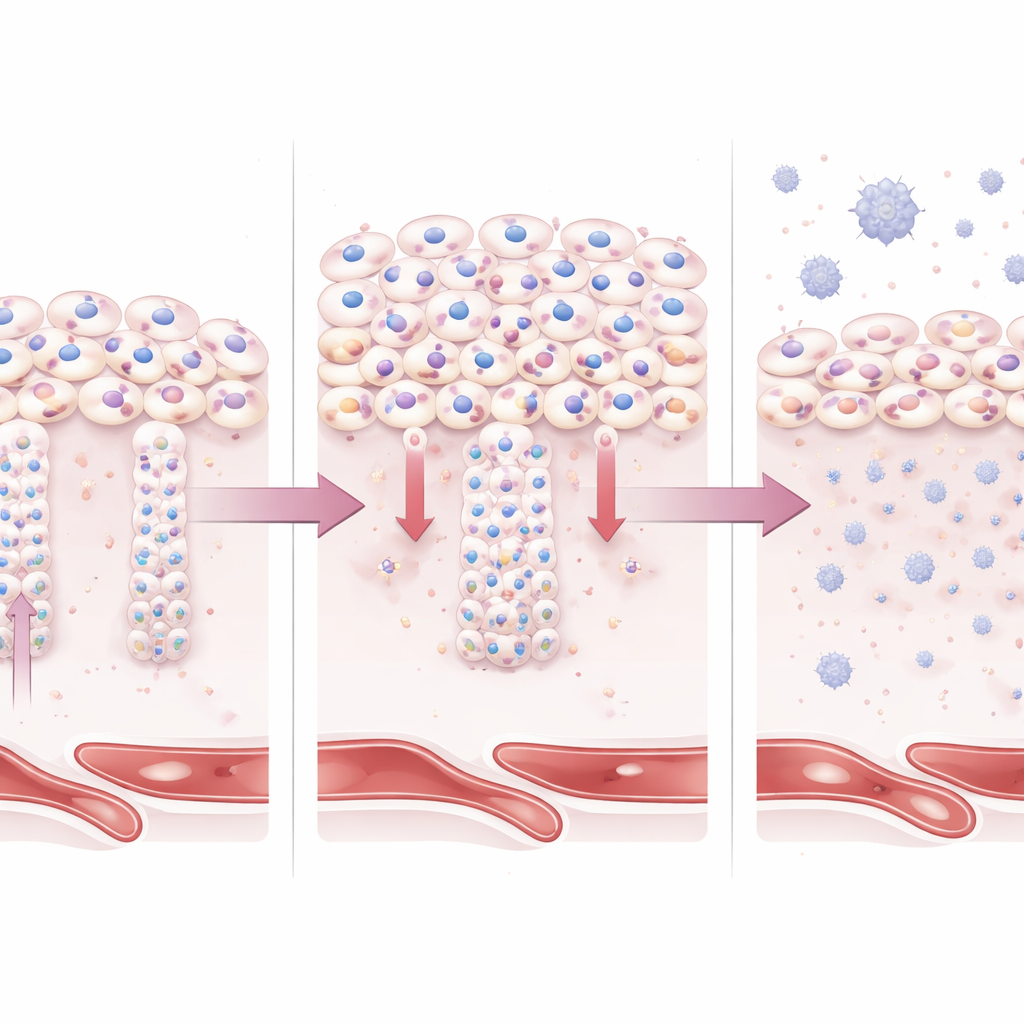
Pour comprendre le rôle de BAP1 dans les cellules placentaires humaines, les scientifiques ont utilisé des cellules souches trophoblastiques humaines et des organoïdes placentaires 3D cultivés en laboratoire. Lorsqu’ils ont artificiellement augmenté les niveaux de BAP1, les cellules sont restées fortement attachées les unes aux autres et ont conservé une identité épithéliale, en nappes. Ces cellules avaient une capacité réduite à se transformer en trophoblastes invasifs qui pénètrent normalement dans l’utérus, et elles produisaient moins des enzymes nécessaires au remodelage des vaisseaux maternels. De la même façon, des cellules qui auraient dû fusionner pour former la couche de surface productrice d’hormones sont restées séparées et non fusionnées. Les analyses moléculaires ont montré une augmentation des gènes et protéines liés à l’adhésion cellulaire et aux jonctions structurelles, tandis que ceux associés à l’invasion, à la production d’hormones, au métabolisme et à l’adaptation au stress étaient diminués.
De mauvais choix cellulaires au stress placentaire
Dans des organoïdes reproduisant les tissus placentaires précoces humains, l’excès de BAP1 a entraîné des régions de cellules de surface fusionnées plus petites ou mal formées et une surreprésentation de trophoblastes de type souche. Parallèlement, les organoïdes ont activé des voies immunitaires innées et inflammatoires, y compris des signaux liés aux interférons qui sont également observés dans les placentas de prééclampsie d’apparition précoce. En combinant séquençage de l’ARN et mesures protéiques, les chercheurs ont établi une « signature » moléculaire pilotée par BAP1 et montré qu’elle correspond fortement aux profils retrouvés spécifiquement dans la prééclampsie d’apparition précoce, mais pas dans d’autres complications de la grossesse comme le diabète gestationnel ou les effets placentaires du COVID-19. Cela relie la suractivité de BAP1 à la fois au dysfonctionnement structurel et à l’atmosphère inflammatoire du placenta malade.
Qu’est-ce que cela implique pour les mères et les bébés
Dans l’ensemble, ce travail peint BAP1 comme un garde-fou qui doit être finement régulé pendant la grossesse. Lorsque BAP1 reste trop élevé, les trophoblastes ne parviennent pas à se différencier en types cellulaires spécialisés nécessaires pour une invasion utérine profonde et des surfaces sécrétrices d’hormones robustes. Le résultat est un placenta superficiel, stressé et inflammatoire — des caractéristiques de la prééclampsie d’apparition précoce. Bien que des recherches supplémentaires soient nécessaires pour déterminer si les modifications de BAP1 sont une cause déclenchante ou une réponse à un stress précoce, cette étude fournit un lien mécaniste clair entre la dérégulation des programmes d’identité cellulaire dans le placenta et un trouble de grossesse potentiellement mortel, ouvrant la voie à de nouveaux biomarqueurs et, éventuellement, à des thérapies ciblées.
Citation: Doria-Borrell, P., Ferrero-Micó, A., Navarro-Serna, S. et al. BAP1 dysregulation impairs trophoblast differentiation and contributes to placental dysfunction in preeclampsia. Cell Death Dis 17, 410 (2026). https://doi.org/10.1038/s41419-026-08650-z
Mots-clés: prééclampsie, placenta, trophoblaste, BAP1, complications de la grossesse