Clear Sky Science · de
BAP1-Dysregulation beeinträchtigt die Differenzierung von Trophoblasten und trägt zur Plazentafunktionsstörung bei Präeklampsie bei
Wenn das Unterstützungsorgan der Schwangerschaft aus dem Gleichgewicht gerät
Präeklampsie ist eine gefährliche Schwangerschaftskomplikation, die durch Bluthochdruck und Organschäden, etwa an Leber und Nieren, gekennzeichnet ist. Im Zentrum dieser Erkrankung steht die Plazenta, das temporäre Organ, das das Baby ernährt. Diese Studie zeigt, wie die Fehlregulation eines einzelnen Steuerproteins, genannt BAP1, die Entwicklung zentraler plazentarer Zellen entgleisen lassen und die schwere, früh einsetzende Form der Präeklampsie fördern kann.
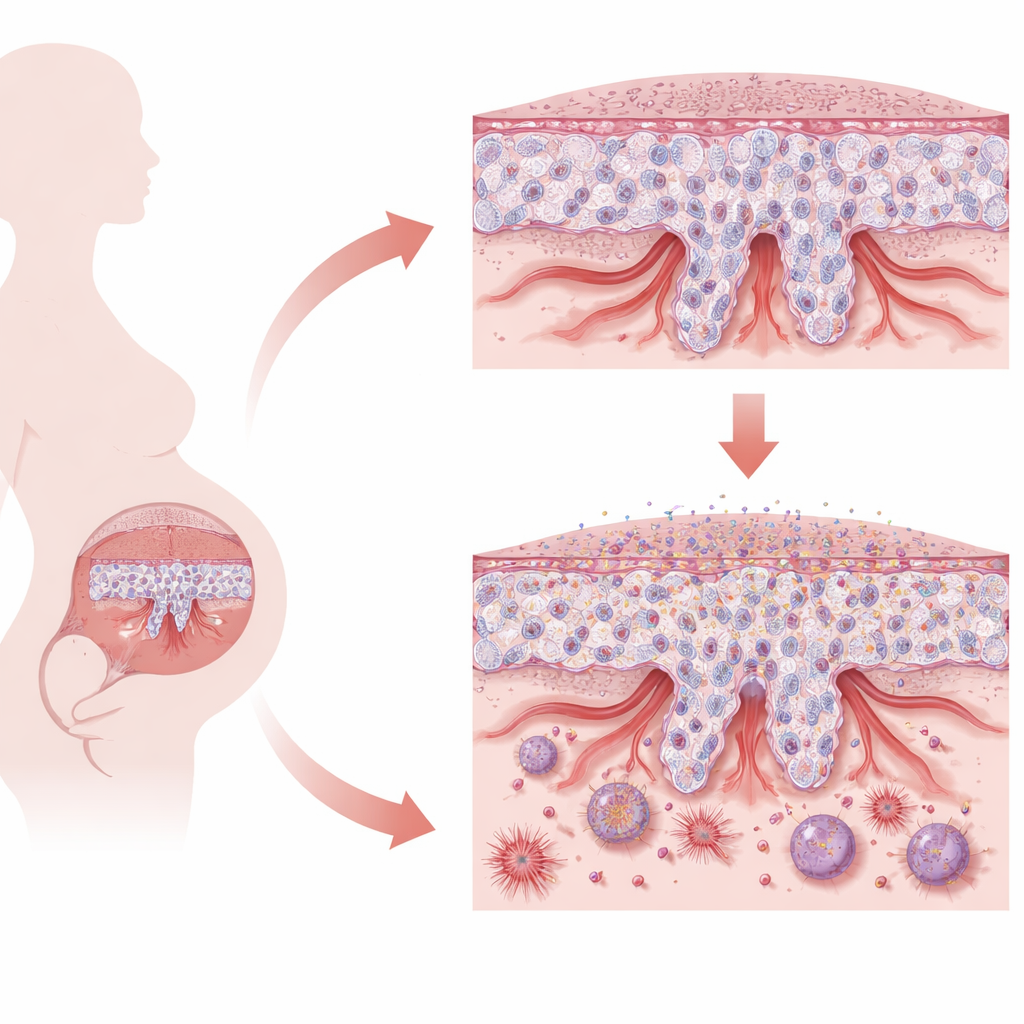
Das empfindliche Gleichgewicht der Plazenta
Die Plazenta besteht aus spezialisierten Zellen, den Trophoblasten. Früh in der Schwangerschaft müssen sich stammzellähnliche Trophoblasten zwischen zwei Hauptaufgaben entscheiden. Einige fusionieren zu einer durchgehenden Oberflächenschicht, die für Nährstoff- und Gasaustausch zuständig ist. Andere differenzieren zu invasiven Zellen, die in die Gebärmutter der Mutter eindringen und die Spiralarterien umbauen, um diese für eine ausreichende Blutversorgung des wachsenden Fötus zu erweitern. Dieses sorgfältige Gleichgewicht zwischen dem Verweilen in einem stammzellähnlichen Zustand, Identitätswechsel und ausreichender Invasion ist essenziell. Scheitert der Prozess, wie bei früh einsetzender Präeklampsie, bleibt die Plazenta flach, gestresst und weniger in der Lage, eine gesunde Schwangerschaft zu unterstützen.
Ein plazentares Protein, das zu stark hochreguliert ist
Die Forscher konzentrierten sich auf BAP1, ein Protein, das besser aus der Krebsforschung bekannt ist. In gesunden Plazenten zu Beginn der Schwangerschaft ist BAP1 in stammzellähnlichen Trophoblasten reichlich vorhanden, fällt aber normalerweise ab, während diese Zellen reifen. Anhand von Plazentaproben von Frauen mit und ohne Schwangerschaftskomplikationen fanden die Wissenschaftler heraus, dass BAP1 und seine Partnerproteine ASXL2 und ASXL3 in Plazenten mit früh einsetzender Präeklampsie spezifisch erhöht waren, nicht jedoch bei der später einsetzenden, stärker mütterlich geprägten Form der Erkrankung. Dieses Muster deutet darauf hin, dass übermäßige BAP1-Aktivität eng mit plazentaren, statt ausschließlich mütterlichen, Ursachen der Störung verbunden ist.
Plazentazellen in einem unreifen Zustand festhalten
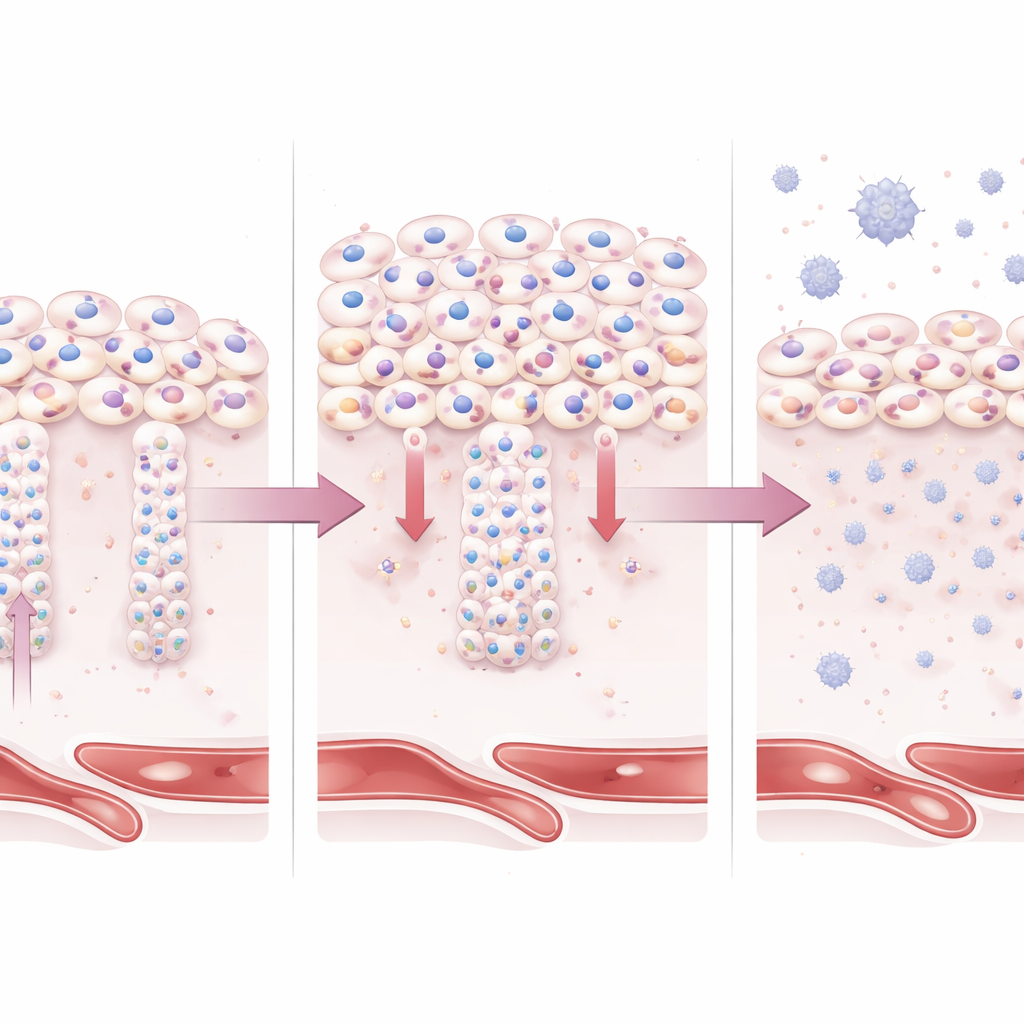
Um zu untersuchen, was BAP1 in menschlichen Plazentazellen bewirkt, nutzten die Wissenschaftler menschliche Trophoblast-Stammzellen und im Labor gezüchtete 3D-Plazenta-Organoide. Als sie die BAP1-Spiegel künstlich erhöhten, hafteten die Zellen stärker aneinander und behielten ausgeprägt eine epithelial‑ beziehungsweise schollenartige Identität bei. Diese Zellen waren weniger befähigt, sich in die invasiven Trophoblasten zu verwandeln, die normalerweise in die Gebärmutter eindringen, und sie produzierten weniger von den Enzymen, die für den Umbau der mütterlichen Blutgefäße nötig sind. Ebenso blieben Zellen, die sich zur hormonproduzierenden Oberflächenschicht fusionieren sollten, als separate, nicht fusionierte Einheiten bestehen. Molekulare Analysen zeigten, dass Gene und Proteine, die mit Zelladhäsion und strukturellen Verbindungen zusammenhängen, hochreguliert waren, während solche, die mit Invasion, Hormonproduktion, Stoffwechsel und Stressanpassung verknüpft sind, heruntergefahren wurden.
Von fehlerhaften Zellentscheidungen zu plazentarem Stress
In Organoid-Modellen, die frühes menschliches Plazentagewebe nachahmen, führte ein Überschuss an BAP1 zu kleineren oder schlecht ausgebildeten Bereichen fusionierter Oberflächenzellen und zu einer Überrepräsentation stammzellähnlicher Trophoblasten. Gleichzeitig aktivierten die Organoide angeborene Immun- und Entzündungswege, einschließlich Interferon-ähnlicher Signale, die ebenfalls in Plazenten mit früh einsetzender Präeklampsie beobachtet werden. Durch die Kombination von RNA-Sequenzierung und Proteinanalyse erstellten die Forscher eine durch BAP1 getriebene molekulare „Signatur“ und zeigten, dass diese stark mit Mustern übereinstimmt, die spezifisch in früh einsetzender Präeklampsie auftreten, nicht jedoch bei anderen Schwangerschaftskomplikationen wie Gestationsdiabetes oder plazentaren Folgen von COVID-19. Dies verknüpft eine erhöhte BAP1-Aktivität sowohl mit der strukturellen Fehlfunktion als auch mit der entzündlichen Atmosphäre der erkrankten Plazenta.
Was das für Mütter und Kinder bedeutet
Insgesamt zeichnet die Arbeit BAP1 als Wächter, der während der Schwangerschaft fein abgestimmt sein muss. Bleibt BAP1 zu hoch, können sich Trophoblasten nicht zu den spezialisierten Zelltypen entwickeln, die für tiefe uterine Invasion und robuste, hormonsekretierende Oberflächen nötig sind. Das Ergebnis ist eine flache, gestresste und entzündete Plazenta – Kennzeichen der früh einsetzenden Präeklampsie. Obwohl weitere Forschung nötig ist, um zu klären, ob Veränderungen von BAP1 Auslöser oder Folge frühen Stresses sind, liefert diese Studie eine klare mechanistische Verbindung zwischen fehlregulierten Zellidentitätsprogrammen in der Plazenta und einer lebensbedrohlichen Schwangerschaftserkrankung. Sie eröffnet Wege zu neuen Biomarkern und langfristig möglicherweise gezielten Therapien.
Zitation: Doria-Borrell, P., Ferrero-Micó, A., Navarro-Serna, S. et al. BAP1 dysregulation impairs trophoblast differentiation and contributes to placental dysfunction in preeclampsia. Cell Death Dis 17, 410 (2026). https://doi.org/10.1038/s41419-026-08650-z
Schlüsselwörter: Präeklampsie, Plazenta, Trophoblast, BAP1, Schwangerschaftskomplikationen