Clear Sky Science · zh
C4BPA对肌肉祖细胞分化的影响:对杜氏肌营养不良症治疗的启示
为何这个肌肉故事重要
杜氏肌营养不良症(DMD)是一种严重的儿童疾病,会逐渐剥夺男孩行走、呼吸和独立生活的能力。大多数研究集中在脆弱的肌纤维本身,这些纤维因缺乏称为肌营养不良蛋白(dystrophin)的关键蛋白而易损。本文则转向肌细胞的“邻居”——通常帮助修复损伤的支持细胞,展示在DMD中它们如何通过一种分泌蛋白开始破坏肌肉重建。理解这一隐藏的元凶,可能为减缓疾病进程并增强未来基因疗法的效果打开新途径。
从帮手变为阻碍者
我们的肌肉并非独自修复。当发生损伤时,处于休眠状态的类干细胞——肌母细胞(myoblasts)被唤醒,分裂并融合形成新的肌纤维。周围存在纤维脂肪祖细胞(FAPs),它们通常搭建临时支架并协同修复。在健康肌肉中,这些FAPs会短暂增殖,愈合完成后就消退。然而在DMD中,它们长期处于活化状态,肌肉逐渐被瘢痕和脂肪替代。作者提出问题:这些异常的FAPs是否直接干扰肌母细胞形成新纤维的能力?
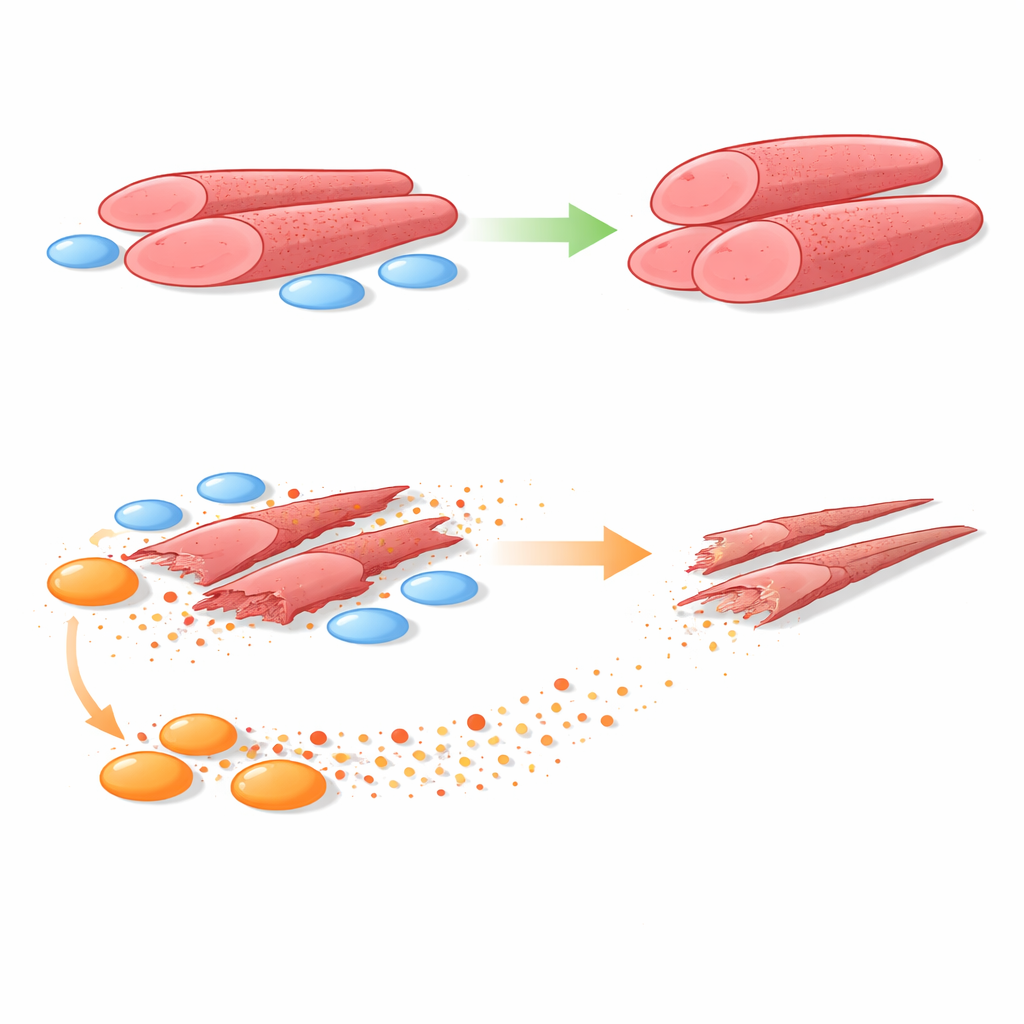
健康细胞与病变细胞的并列测试
为回答这一问题,团队将人源肌母细胞与从健康男孩和DMD男孩的肌肉活检中获得的FAPs共同培养。他们使用的体系允许两种细胞类型直接接触,或通过仅允许分泌分子通过的多孔隔膜分离。在这两种设置中,健康的FAPs都能促进肌母细胞形成更大、更强健的肌管。相反,来自DMD的FAPs持续使这些肌管的体积变小、所含细胞核数量减少——这是肌肉形成受损的明显标志。当取消物理接触时,DMD FAPs仍然有害,表明可溶性因子是主要罪魁。
追踪有毒信号
研究者随后使用质谱技术对健康与DMD FAPs分泌的蛋白进行了目录化,该技术可同时鉴定数百种分子。在检测到的760种蛋白中,近一半在DMD FAPs中含量更高。通过将该列表与人类肌肉细胞表面的受体进行交叉比对,他们将候选范围缩小到29种可能对肌母细胞起作用的分子。进一步测试中,筛出了一种关键蛋白——C4BPA,其在DMD FAP培养物及DMD患者的血液和肌肉组织中明显升高。当将纯化的C4BPA暴露于健康肌母细胞时,这些细胞融合成细长粗大肌管的能力显著下降,驱动肌肉生长的基因被下调,而与肌肉衰减相关的基因被上调。
从培养皿到工程肌肉
为检验该效应是否影响实际肌肉功能,团队使用了从人细胞在软支架中生长出的三维“微型肌肉”。这些工程组织在电刺激下能够收缩,模拟真实肌肉。当C4BPA在形成过程中存在时,所得纤维更薄,产生的抽搐力和强直力较弱,并表现出更早的疲劳迹象。最后,研究者探讨阻断C4BPA是否能逆转部分损害。通过基因沉默方法降低DMD FAPs的C4BPA产量,并将这些改造后的细胞与健康肌母细胞共培养,肌管形成获得改善:更多肌母细胞融合,每根肌管含有更多细胞核,表明抑制C4BPA能部分恢复FAPs应有的支持作用。
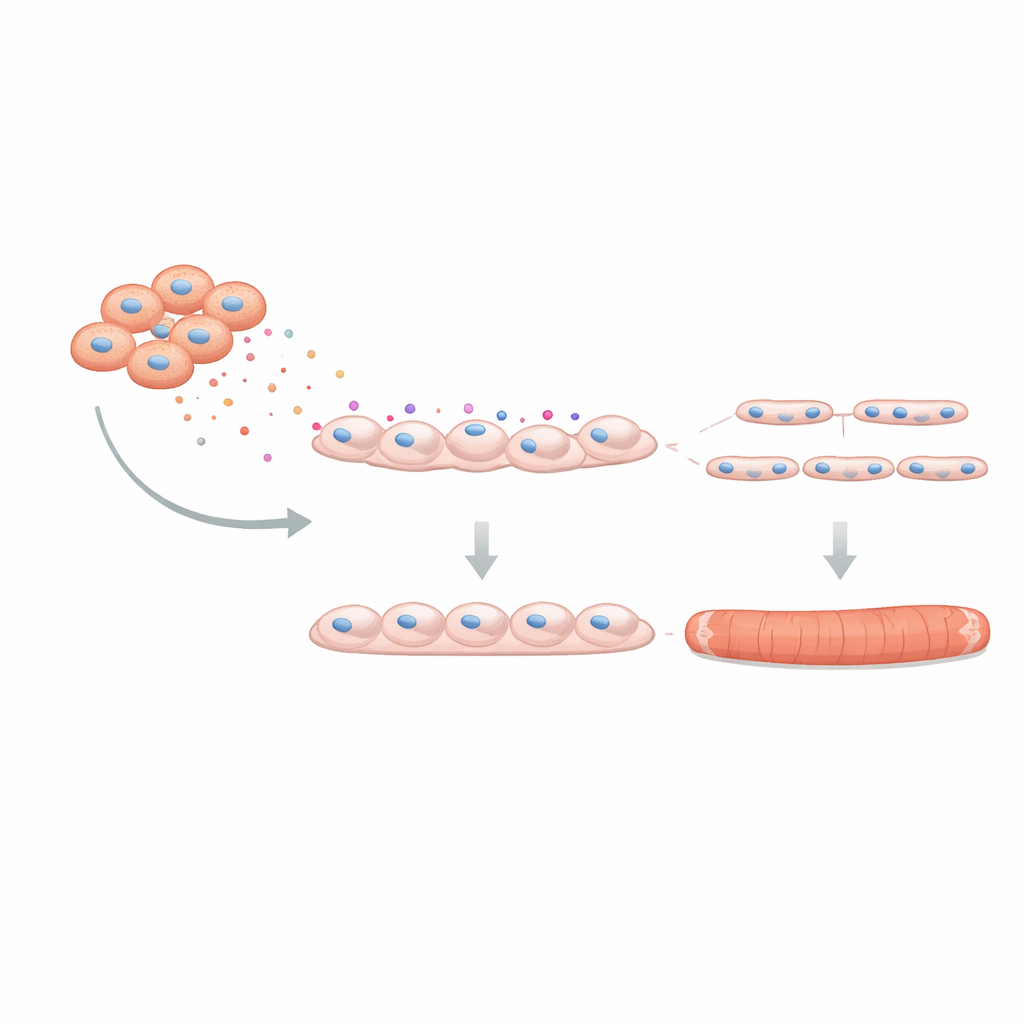
这对未来治疗意味着什么
这项研究表明,在杜氏肌营养不良症中,肌肉中的支持细胞通过过度产生C4BPA成为“坏邻居”,这种蛋白破坏新肌纤维的生长和功能。虽然这并不能修复肌营养不良蛋白的基因缺陷,但以C4BPA或类似分泌因子为靶点,可能有助于保护存量肌肉并使组织对新兴的基因与细胞疗法保持更高的响应性。简言之,研究提示治疗DMD可能不仅需要修复肌肉的“砖块”,还要安抚周围的“施工队”,以便再生得以进行而不是被阻断。
引用: Fernández-Simón, E., Tejedera-Villafranca, A., Fernández-Garabay, X. et al. Impact of C4BPA on Muscle progenitor cell differentiation: insights for Duchenne muscular dystrophy treatment. Cell Death Dis 17, 313 (2026). https://doi.org/10.1038/s41419-026-08588-2
关键词: 杜氏肌营养不良症, 肌肉再生, 纤维脂肪祖细胞, C4BPA, 肌肉干细胞