Clear Sky Science · de
Auswirkung von C4BPA auf die Differenzierung von Muskelvorläuferzellen: Erkenntnisse für die Behandlung der Duchenne-Muskeldystrophie
Warum diese Muskelgeschichte wichtig ist
Die Duchenne-Muskeldystrophie (DMD) ist eine schwere Kindheitskrankheit, die Jungen nach und nach die Fähigkeit zu laufen, zu atmen und unabhängig zu leben raubt. Die meisten Forschungen konzentrieren sich auf die Muskelfasern selbst, die fragil sind, weil ihnen ein wichtiges Protein namens Dystrophin fehlt. Dieser Artikel betrachtet stattdessen die „Nachbarn“ der Muskelzellen — Unterstützungszellen, die normalerweise bei der Reparatur helfen — und zeigt, wie sie bei DMD den Muskelaufbau durch ein einziges sezerniertes Protein zu sabotieren beginnen. Das Verständnis dieses verborgenen Übeltäters könnte neue Wege eröffnen, die Krankheit zu verlangsamen und künftige Gentherapien zu stärken.
Helfer, die zu Hindernissen werden
Unsere Muskeln reparieren sich nicht allein. Bei Schäden erwachen ruhende, stammzellähnliche Zellen, sogenannte Myoblasten, teilen sich und verschmelzen zu neuen Muskelfasern. Um sie herum leben fibroadipogene Vorläuferzellen, oder FAPs, die normalerweise ein temporäres Gerüst bilden und die Reparatur koordinieren. In gesundem Muskel expandieren diese FAPs kurzfristig und verschwinden nach Abschluss der Heilung wieder. Bei DMD bleiben sie jedoch aktiviert, und der Muskel füllt sich allmählich mit Narben- und Fettgewebe. Die Autoren fragten: Beeinträchtigen diese veränderten FAPs direkt die Fähigkeit der Myoblasten, neue Fasern zu bilden?
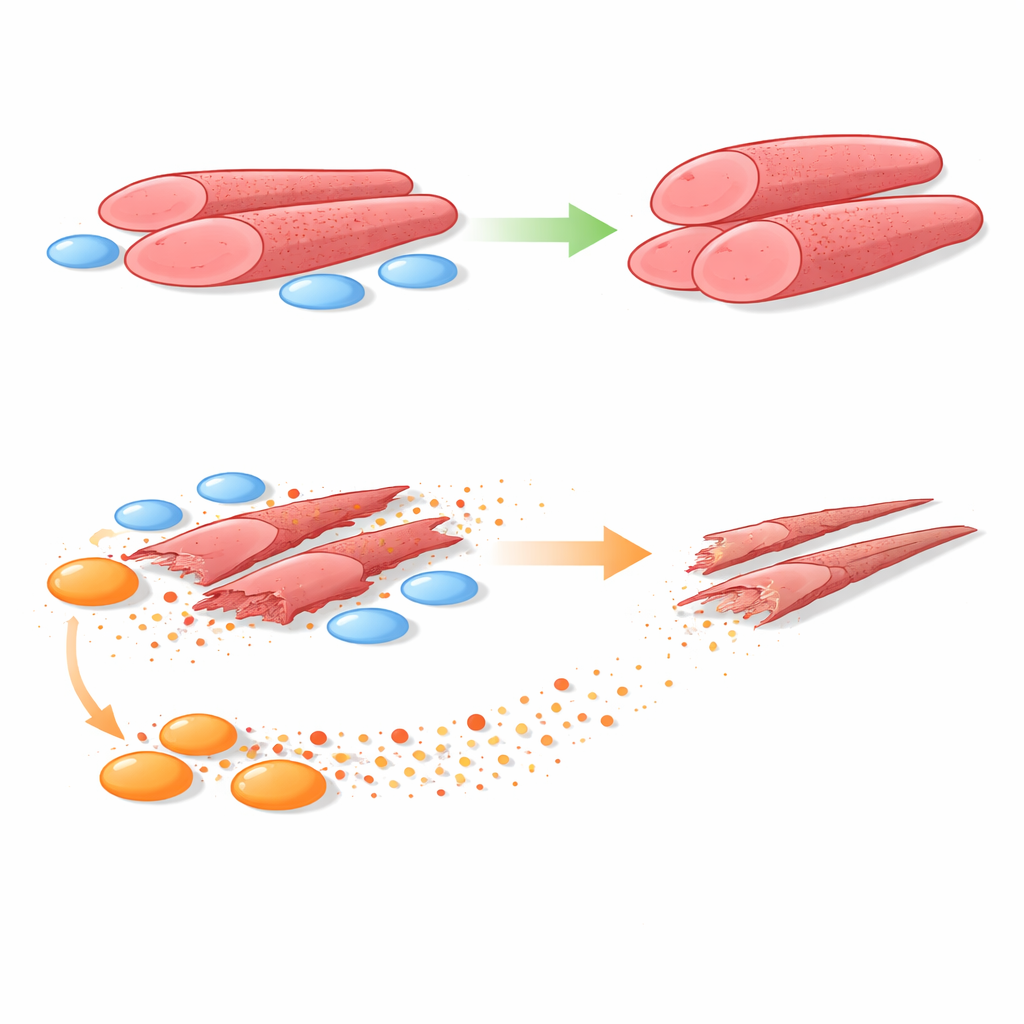
Direkter Vergleich von gesunden und erkrankten Zellen
Um dies zu klären, züchtete das Team menschliche Myoblasten zusammen mit FAPs aus Muskelbiopsien gesunder Jungen und Jungen mit DMD. Sie verwendeten Systeme, die entweder direkten Kontakt zwischen den beiden Zelltypen zuließen oder durch eine poröse Barriere trennten, die nur sezernierte Moleküle passieren lässt. In beiden Anordnungen förderten gesunde FAPs die Bildung größerer, robusterer Muskelröhren durch die Myoblasten. Im starken Gegensatz dazu verringerten DMD-FAPs konsequent die Größe dieser Röhren und die Anzahl der darin enthaltenen Zellkerne — eindeutige Zeichen schlechterer Muskelbildung. Selbst ohne physischen Kontakt schadeten die DMD-FAPs weiterhin, was auf lösliche Faktoren als Hauptschuldige hindeutet.
Auf der Spur eines toxischen Signals
Die Forscher katalogisierten anschließend die von gesunden und DMD-FAPs freigesetzten Proteine mittels Massenspektrometrie, einer Technik, die Hunderte von Molekülen gleichzeitig identifizieren kann. Von 760 detektierten Proteinen waren fast die Hälfte in DMD-FAPs stärker vertreten. Durch Abgleich dieser Liste mit Rezeptoren, die auf menschlichen Muskelzellen vorhanden sind, schränkten sie die Auswahl auf 29 Kandidaten ein, die plausibel auf Myoblasten wirken könnten. Weitere Tests hoben ein Schlüsselprotein hervor, genannt C4BPA, das in DMD-FAP-Kulturen deutlich erhöht war und auch im Blut und Muskelgewebe von DMD-Patienten nachgewiesen wurde. Wurden gesunde Myoblasten im Labor reinem C4BPA ausgesetzt, sank ihre Fähigkeit, zu langen, dicken Röhren zu fusionieren, deutlich; gleichzeitig wurden Gene, die Muskelwachstum antreiben, herunterreguliert, während Gene, die mit Muskelabbau assoziiert sind, hochreguliert wurden.
Vom Petrischälchen zum konstruierten Muskel
Um zu prüfen, ob dieser Effekt für die tatsächliche Muskelfunktion relevant ist, nutzte das Team einen dreidimensionalen „Mini-Muskel“, der aus menschlichen Zellen in einem weichen Gerüst gezüchtet wurde. Diese konstruierten Gewebe können sich bei elektrischer Stimulation zusammenziehen und simulieren so echte Muskelarbeit. War C4BPA während ihrer Bildung vorhanden, waren die resultierenden Fasern dünner und erzeugten schwächere Zuckungs- und Tetanik-Kräfte, begleitet von Anzeichen früherer Ermüdung. Schließlich untersuchten die Forscher, ob das Blockieren von C4BPA einen Teil des Schadens rückgängig machen kann. Durch genetisches Stummschalten zur Reduktion der C4BPA-Produktion in DMD-FAPs kultivierten sie diese modifizierten Zellen zusammen mit gesunden Myoblasten. Die Bildung von Muskelröhren verbesserte sich: mehr Myoblasten fusionierten, und jede Röhre enthielt mehr Kerne — ein Hinweis darauf, dass das Dämpfen von C4BPA die unterstützende Rolle der FAPs teilweise wiederherstellt.
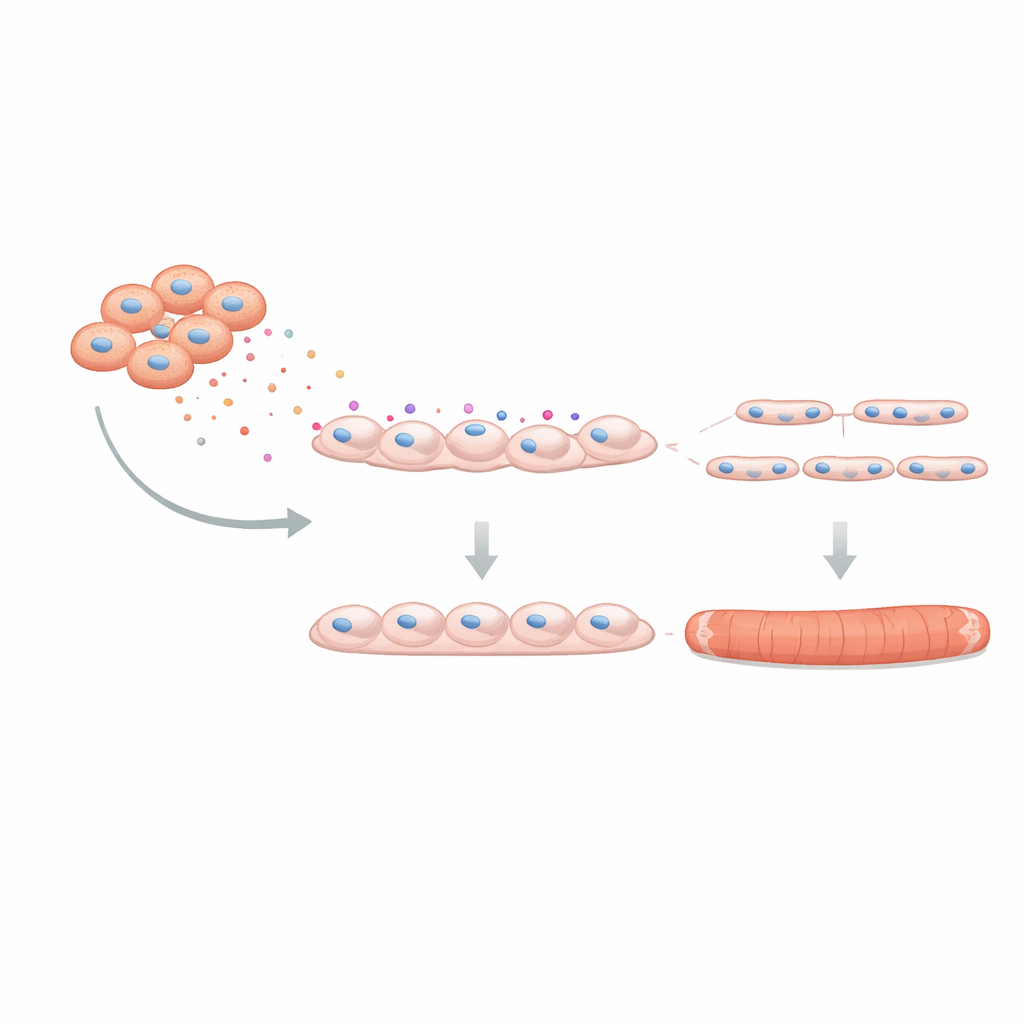
Was das für künftige Therapien bedeutet
Die Studie zeigt, dass sich in der Duchenne-Muskeldystrophie Stützzellen im Muskel zu „schlechten Nachbarn“ wandeln, indem sie C4BPA übermäßig produzieren — ein Protein, das das Wachstum und die Funktion neuer Muskelfasern stört. Obwohl dies den zugrundeliegenden genetischen Defekt in Dystrophin nicht behebt, könnte das Anvisieren von C4BPA oder ähnlichen sezernierten Faktoren helfen, den verbleibenden Muskel zu erhalten und das Gewebe empfänglicher für aufkommende Gen- und Zelltherapien zu machen. Vereinfacht gesagt legt die Arbeit nahe, dass die Behandlung von DMD nicht nur das Reparieren der „Bausteine“ des Muskels erfordern wird, sondern auch das Beruhigen der umgebenden „Baumannschaft“, damit die Regeneration fortschreiten kann, anstatt blockiert zu werden.
Zitation: Fernández-Simón, E., Tejedera-Villafranca, A., Fernández-Garabay, X. et al. Impact of C4BPA on Muscle progenitor cell differentiation: insights for Duchenne muscular dystrophy treatment. Cell Death Dis 17, 313 (2026). https://doi.org/10.1038/s41419-026-08588-2
Schlüsselwörter: Duchenne-Muskeldystrophie, Muskelregeneration, fibroadipogene Vorläuferzellen, C4BPA, Muskelstammzellen