Clear Sky Science · it
Impatto di C4BPA sulla differenziazione delle cellule progenitrici muscolari: intuizioni per il trattamento della distrofia muscolare di Duchenne
Perché questa storia muscolare è importante
La distrofia muscolare di Duchenne (DMD) è una grave malattia dell’infanzia che lentamente priva i bambini della capacità di camminare, respirare e vivere in modo indipendente. La maggior parte della ricerca si è concentrata sulle fibre muscolari stesse, fragili perché prive di una proteina chiave chiamata distrofina. Questo articolo guarda invece ai “vicini” delle cellule muscolari — cellule di supporto che normalmente aiutano a riparare i danni — e mostra come, nella DMD, esse comincino a sabotare la ricostruzione muscolare tramite una singola proteina secreta. Comprendere questo colpevole nascosto potrebbe aprire nuove strade per rallentare la malattia e potenziare future terapie geniche.
Aiutanti che diventano ostacoli
I nostri muscoli non si riparano da soli. Quando si verifica un danno, cellule dormienti di tipo staminale chiamate mioblasti si attivano, si dividono e si fondono in nuove fibre muscolari. Intorno a loro vivono le cellule progenitrici fibro-adipogeniche, o FAP, che normalmente depositano uno scheletro temporaneo e aiutano a coordinare la riparazione. Nei muscoli sani, queste FAP si espandono per un breve periodo e poi scompaiono una volta completata la guarigione. Nella DMD, però, rimangono attivate e il muscolo si riempie gradualmente di cicatrice e grasso. Gli autori si sono chiesti: queste FAP alterate interferiscono direttamente con la capacità dei mioblasti di formare nuove fibre?
Test affiancati di cellule sane e malate
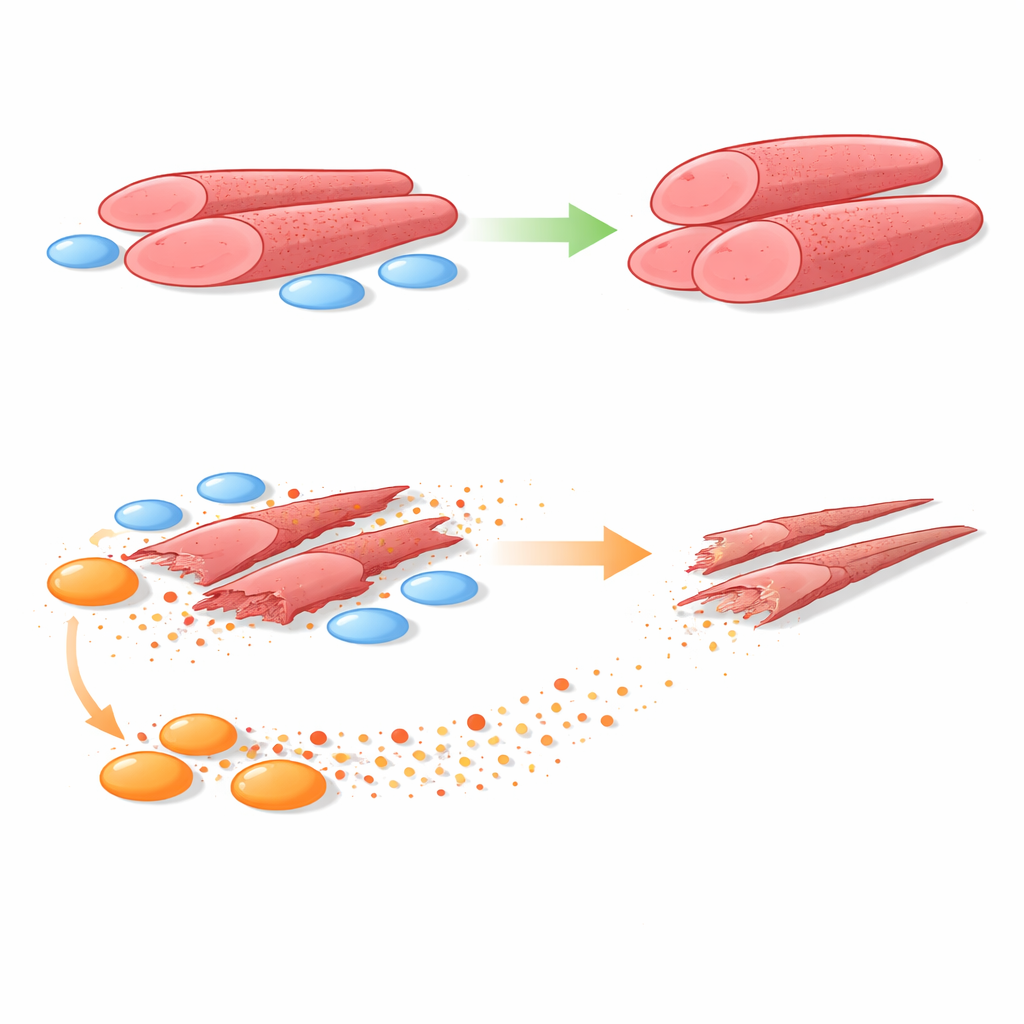
Per rispondere, il team ha coltivato mioblasti umani insieme a FAP prelevate da biopsie muscolari di ragazzi sani e di ragazzi con DMD. Hanno utilizzato sistemi che permettevano il contatto diretto tra i due tipi cellulari oppure la separazione tramite una barriera porosa che lascia passare solo molecole secrete. In entrambi gli allestimenti, le FAP sane favorivano la formazione di tubi muscolari più grandi e robusti da parte dei mioblasti. In netto contrasto, le FAP della DMD riducevano sistematicamente le dimensioni di questi tubi e il numero di nuclei cellulari in essi contenuti — segnali chiari di una peggiore formazione muscolare. Quando il contatto fisico veniva rimosso, le FAP DMD continuavano comunque a danneggiare, indicando che i fattori solubili erano i principali responsabili.
Alla ricerca di un segnale tossico
I ricercatori hanno quindi catalogato le proteine rilasciate dalle FAP sane e dalle FAP DMD usando la spettrometria di massa, una tecnica che può identificare centinaia di molecole contemporaneamente. Su 760 proteine rilevate, quasi la metà era più abbondante nelle FAP DMD. Incrociando questa lista con i recettori presenti sulle cellule muscolari umane, hanno ristretto il campo a 29 candidati che plausibilmente potevano agire sui mioblasti. Test successivi hanno individuato una proteina chiave, chiamata C4BPA, nettamente più elevata nelle colture di FAP DMD e presente anche nel sangue e nel tessuto muscolare dei pazienti con DMD. Quando mioblasti sani sono stati esposti in laboratorio a C4BPA purificata, la loro capacità di fondersi in tubi lunghi e spessi è calata drasticamente, i geni che promuovono la crescita muscolare sono stati soppressi mentre sono aumentati i geni associati all’atrofia.
Dal piatto di Petri al muscolo ingegnerizzato
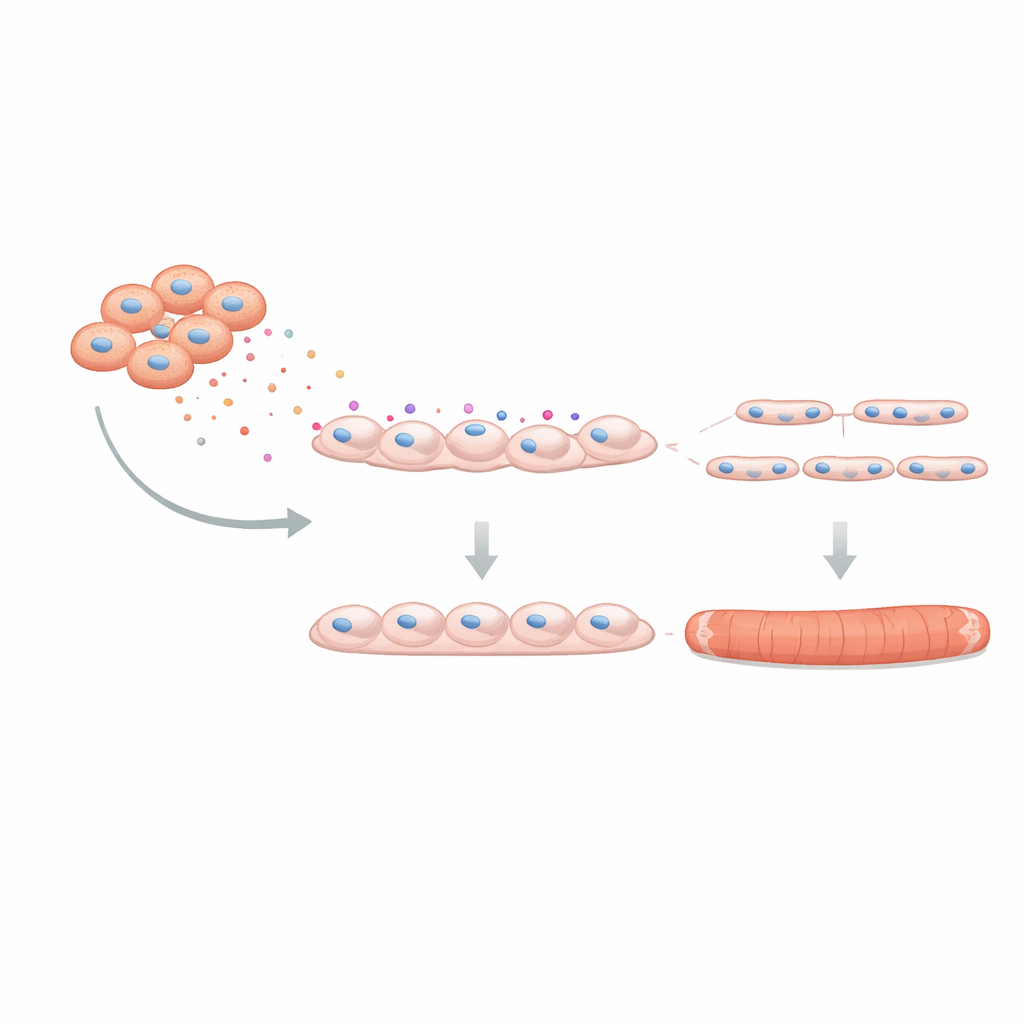
Per verificare se questo effetto incideva sulla funzione muscolare reale, il team ha usato un “mini-muscolo” tridimensionale coltivato da cellule umane in uno scaffold morbido. Questi tessuti ingegnerizzati possono contrarsi quando stimolati elettricamente, imitando il muscolo reale. Quando C4BPA era presente durante la loro formazione, le fibre risultanti erano più sottili e producevano forze di contrazione (twitch e tetaniche) più deboli, con segni di affaticamento precoce. Infine, i ricercatori hanno chiesto se bloccare C4BPA potesse annullare parte del danno. Riducendo geneticamente la produzione di C4BPA nelle FAP DMD e co-coltivando queste cellule modificate con mioblasti sani, la formazione dei tubi muscolari è migliorata: più mioblasti si sono fusi e ogni tubo conteneva più nuclei, indicando che attenuare C4BPA ripristina parzialmente il ruolo di supporto che le FAP dovrebbero svolgere.
Cosa significa per i trattamenti futuri
Questo studio rivela che nella distrofia muscolare di Duchenne, le cellule di supporto nel muscolo diventano “cattivi vicini” sovraproducendo C4BPA, una proteina che altera la crescita e la funzione delle nuove fibre muscolari. Pur non correggendo il difetto genetico di base nella distrofina, mirare a C4BPA o a fattori secreti simili potrebbe aiutare a preservare il muscolo residuo e mantenere il tessuto più ricettivo alle emergenti terapie geniche e cellulari. In termini semplici, il lavoro suggerisce che trattare la DMD potrebbe richiedere non solo di riparare i “mattoni” del muscolo ma anche di calmare la “squadra di costruzione” circostante affinché la rigenerazione proceda invece di essere bloccata.
Citazione: Fernández-Simón, E., Tejedera-Villafranca, A., Fernández-Garabay, X. et al. Impact of C4BPA on Muscle progenitor cell differentiation: insights for Duchenne muscular dystrophy treatment. Cell Death Dis 17, 313 (2026). https://doi.org/10.1038/s41419-026-08588-2
Parole chiave: Distrofia muscolare di Duchenne, rigenerazione muscolare, progenitori fibro-adipogenici, C4BPA, cellule staminali muscolari