Clear Sky Science · ru
Влияние C4BPA на дифференцировку мышечных прогениторных клеток: выводы для лечения мышечной дистрофии Дюшенна
Почему эта история о мышцах важна
Мышечная дистрофия Дюшенна (ДМД) — тяжелое детское заболевание, которое постепенно лишает мальчиков способности ходить, дышать и жить самостоятельно. Большинство исследований сосредоточено на самих мышечных волокнах, которые уязвимы из‑за отсутствия ключевого белка — дистрофина. В этой статье внимание переключается на «соседей» мышечных клеток — поддерживающие клетки, которые обычно помогают восстанавливать повреждения — и показывается, как при ДМД они начинают мешать восстановлению мышц посредством одного секретируемого белка. Понимание этого скрытого виновника может открыть новые пути замедления болезни и повысить эффективность будущих генотерапий.
Помощники, превращающиеся в препятствия
Мышцы не восстанавливаются в одиночку. При повреждении пробуждаются спящие стволоподобные клетки — миобласты, которые делятся и сливаются в новые мышечные волокна. Вокруг них находятся фиброадипогенные прогениторные клетки (FAP), которые обычно создают временный каркас и координируют восстановление. В здоровой ткани FAP временно разрастаются, а затем исчезают по мере заживления. При ДМД же они остаются активными, и мышца постепенно заполняется рубцовой и жировой тканью. Авторы задали вопрос: мешают ли изменённые FAP непосредственно способности миобластов формировать новые волокна?
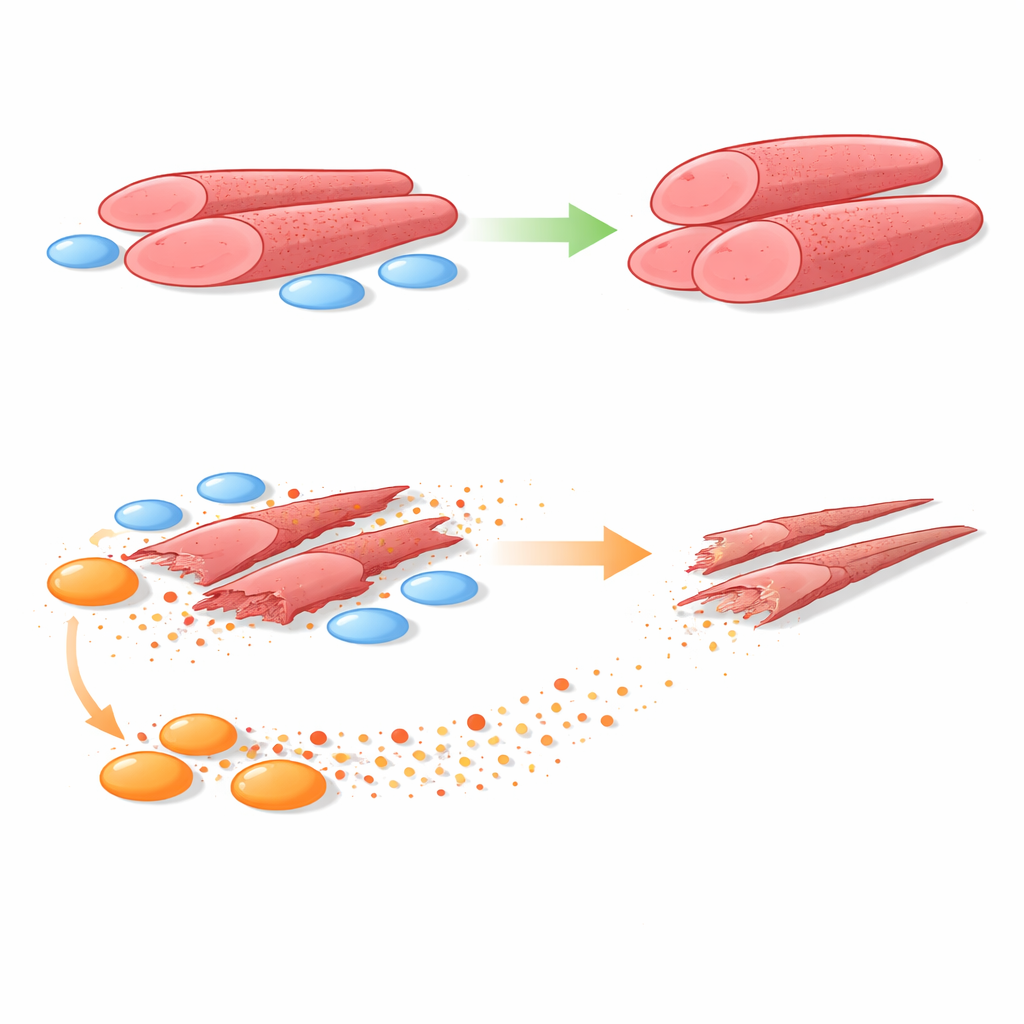
Сравнительные тесты здоровых и больных клеток
Для ответа команда выращивала человеческие миобласты вместе с FAP, выделенными из мышечных биопсий здоровых мальчиков и мальчиков с ДМД. Использовали системы, позволяющие либо прямой контакт между двумя типами клеток, либо разделение пористым барьером, через который проходят только секретируемые молекулы. В обоих вариантах здоровые FAP стимулировали миобласты формировать большие, более прочные мышечные трубки. Напротив, FAP из ДМД последовательно уменьшали размер этих трубок и количество содержащихся в них ядер — явные признаки худшей миогенеза. Когда физический контакт исключали, вред от DMD‑FAP сохранялся, что указывало на растворимые факторы как на главных нарушителей.
В поисках токсического сигнала
Далее исследователи каталогизировали белки, выделяемые здоровыми и DMD‑FAP, с помощью масс‑спектрометрии — метода, позволяющего идентифицировать сотни молекул одновременно. Из 760 обнаруженных белков почти половина была более представлена в DMD‑FAP. Сопоставив этот список с рецепторами, присутствующими на человеческих мышечных клетках, они сузили круг до 29 кандидатов, которые могли действовать на миобласты. Последующие тесты выделили один ключевой белок — C4BPA, уровень которого был заметно выше в культурах DMD‑FAP, а также в крови и мышечной ткани пациентов с ДМД. При обработке здоровых миобластов очищенным C4BPA в лаборатории их способность сливаться в длинные толстые трубки резко снижалась, при этом выключались гены, стимулирующие рост мышц, и активировались гены, связанные с истощением мышц.
От чашки Петри к инженерным мышцам
Чтобы выяснить, влияет ли это на реальную мышечную функцию, команда использовала трёхмерные «мини‑мыщцы», выращенные из человеческих клеток в мягком каркасе. Эти созданные ткани сокращаются при электрической стимуляции, имитируя настоящие мышцы. При наличии C4BPA в процессе формирования получившиеся волокна были тоньше и производили более слабые одиночные (твитч) и тетанические силы, с признаками более быстрой утомляемости. Наконец, исследователи проверили, можно ли отменить часть повреждения, блокируя C4BPA. С помощью генетического заглушения производства C4BPA в DMD‑FAP и совместного культивирования этих модифицированных клеток со здоровыми миобластами образование мышечных трубок улучшилось: больше миобластов сливалось, и в каждой трубке оказалось больше ядер, что указывает на частичное восстановление поддерживающей роли FAP.
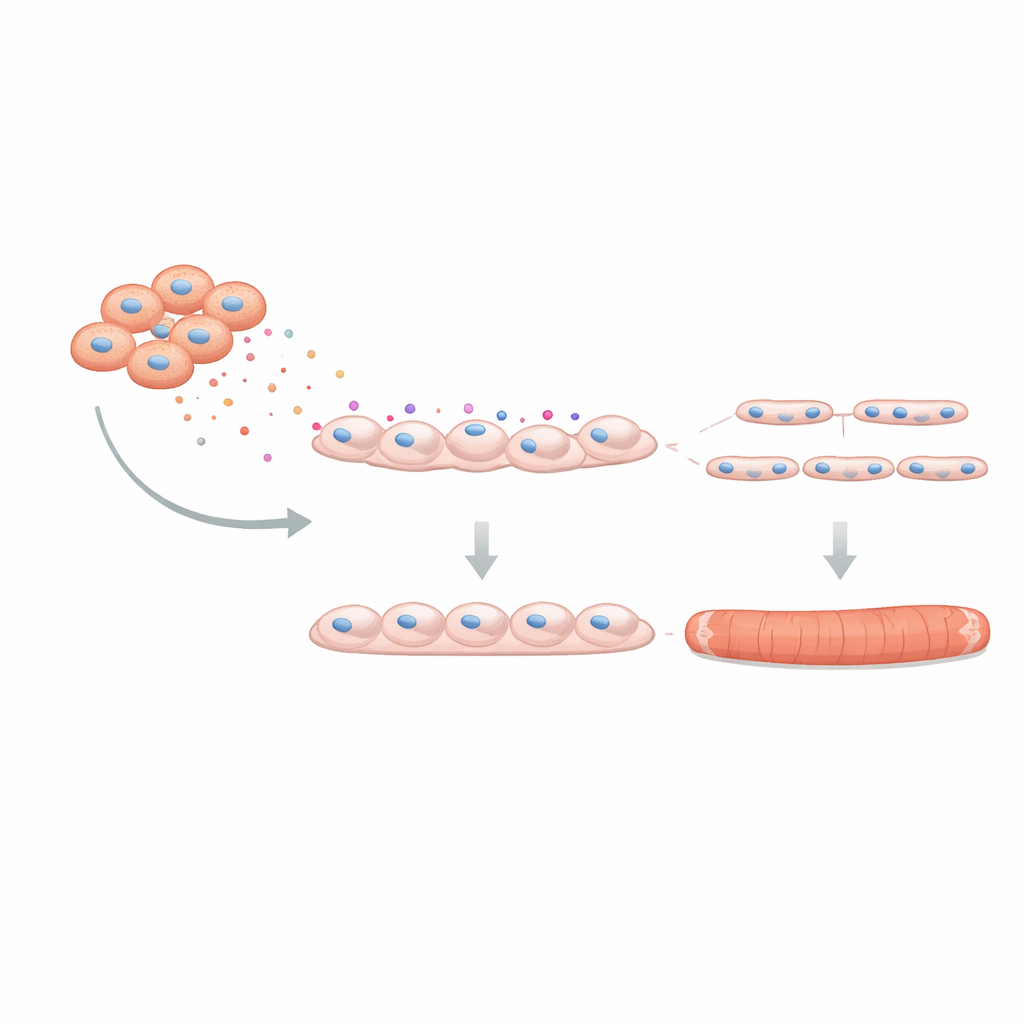
Что это значит для будущих терапий
Исследование показывает, что при мышечной дистрофии Дюшенна поддерживающие клетки в мышце становятся «плохими соседями», чрезмерно вырабатывая C4BPA — белок, нарушающий рост и функцию новых мышечных волокон. Хотя это не устраняет первичный генетический дефект с дистрофином, мишение C4BPA или аналогичных секретируемых факторов может помочь сохранить оставшиеся мышцы и сделать ткань более отзывчивой к новым генным и клеточным терапииям. Проще говоря, работа предлагает, что лечение ДМД должно включать не только восстановление «кирпичей» мышцы, но и усмирение окружающей «строительной бригады», чтобы регенерация шла, а не блокировалась.
Цитирование: Fernández-Simón, E., Tejedera-Villafranca, A., Fernández-Garabay, X. et al. Impact of C4BPA on Muscle progenitor cell differentiation: insights for Duchenne muscular dystrophy treatment. Cell Death Dis 17, 313 (2026). https://doi.org/10.1038/s41419-026-08588-2
Ключевые слова: мышечная дистрофия Дюшенна, регенерация мышц, фиброадипогенные прогениторы, C4BPA, мышечные стволовые клетки