Clear Sky Science · nl
Invloed van C4BPA op differentiatie van spierprogenitorcellen: inzichten voor de behandeling van Duchenne spierdystrofie
Waarom dit spierverhaal ertoe doet
Duchenne spierdystrofie (DMD) is een ernstige kinderziekte die jongens geleidelijk berooft van hun vermogen om te lopen, te ademen en onafhankelijk te leven. De meeste onderzoeken hebben zich gericht op de spiervezels zelf, die kwetsbaar zijn omdat ze een sleutelproteïne, dystrofine, missen. Dit artikel bekijkt in plaats daarvan de “buren” van spiercellen — ondersteunende cellen die normaal bij schade helpen herstellen — en toont hoe deze in DMD het spierherstel beginnen te saboteren via één uitgescheiden proteïne. Het begrijpen van deze verborgen schuldige kan nieuwe wegen openen om de ziekte te vertragen en toekomstige gentherapieën te versterken.
Helpers die hindernissen worden
Onze spieren herstellen niet zelfstandig. Wanneer er schade optreedt, ontwaken sikkelachtige stamcellen genaamd myoblasten, delen ze zich en versmelten ze tot nieuwe spiervezels. In hun omgeving leven fibroadipogene progenitorcellen, of FAPs, die normaal een tijdelijke steiger vormen en het herstel coördineren. In gezonde spier breiden deze FAPs zich kort uit en verdwijnen ze weer zodra de genezing voltooid is. Bij DMD blijven ze echter actief, en vult de spier zich geleidelijk met littekenweefsel en vet. De auteurs vroegen zich af: verstoren deze gewijzigde FAPs rechtstreeks het vermogen van myoblasten om nieuwe vezels te vormen?
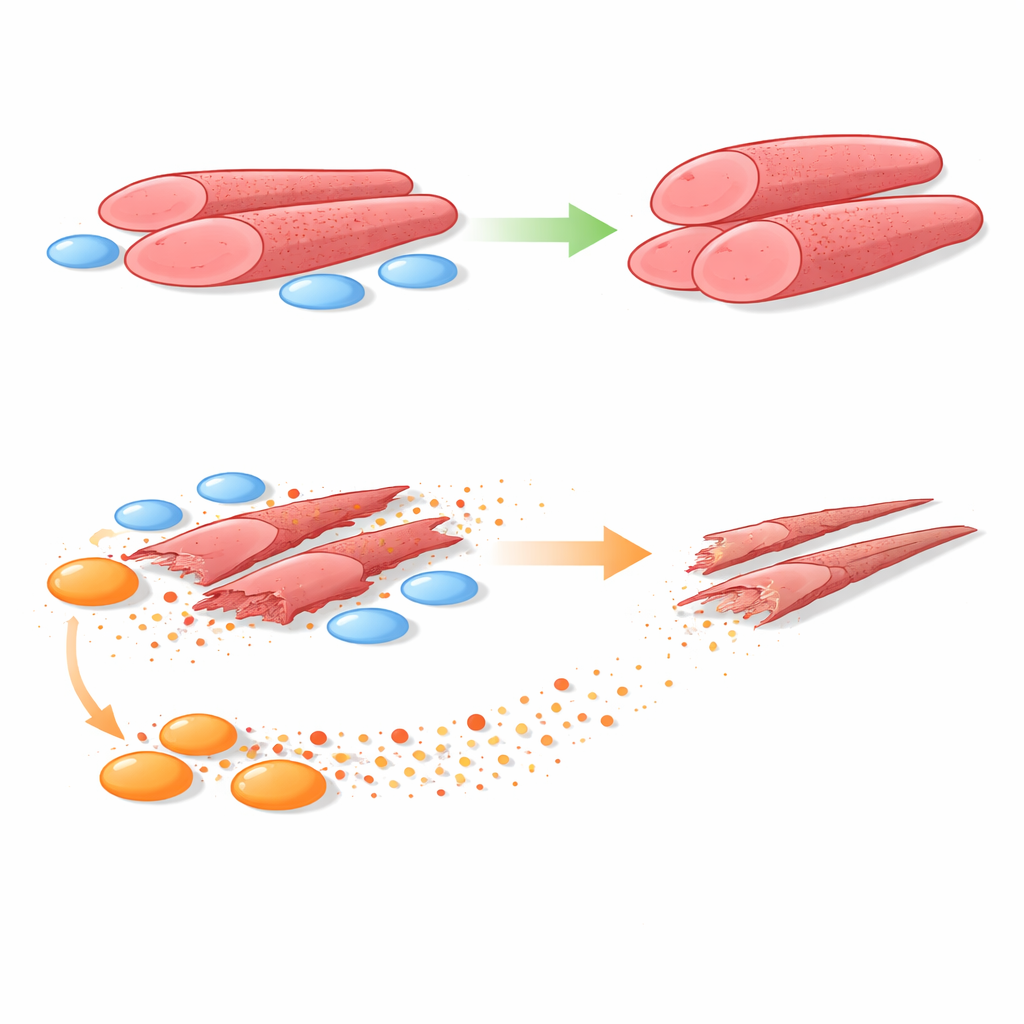
Zij-aan-zij testen van gezonde en zieke cellen
Om dit te onderzoeken kweekte het team humane myoblasten samen met FAPs afkomstig van spierbiopten van gezonde jongens en jongens met DMD. Ze gebruikten systemen die óf directe contact tussen de twee celtypen toestonden óf ze scheidden met een poreuze barrière die alleen uitgescheiden moleculen doorlaat. In beide opstellingen stimuleerden gezonde FAPs myoblasten om grotere, robuustere spiertubes te vormen. In scherp contrast verminderden DMD-FAPs consequent de grootte van deze buizen en het aantal celkernen daarin — duidelijke tekenen van slechtere spiervorming. Toen fysiek contact werd verwijderd, bleven DMD-FAPs schadelijk, wat wijst op oplosbare factoren als de belangrijkste boosdoeners.
Op zoek naar een toxisch signaal
Vervolgens brachten de onderzoekers de eiwitten in kaart die door gezonde en DMD-FAPs werden uitgescheiden met behulp van massaspectrometrie, een techniek die honderden moleculen tegelijk kan identificeren. Van de 760 gedetecteerde eiwitten was bijna de helft meer aanwezig in DMD-FAPs. Door deze lijst te kruisen met receptoren aanwezig op menselijke spiercellen, beperkte men de kandidaten tot 29 eiwitten die plausibel op myoblasten kunnen inwerken. Verdere tests wezen één sleuteleiwit aan, genoemd C4BPA, dat duidelijk hoger was in DMD-FAPcultures en ook in het bloed en spierweefsel van DMD-patiënten. Toen gezonde myoblasten in het lab werden blootgesteld aan gezuiverd C4BPA, daalde hun vermogen om tot lange, dikke buizen te versmelten scherp, en genen die spiergroei stimuleren werden naar beneden bijgeregeld terwijl genen geassocieerd met spierverlies werden opgevoerd.
Van petrischaal naar gekweekte spier
Om te zien of dit effect van belang was voor daadwerkelijke spierfunctie, gebruikte het team een driedimensionale “mini-spier” gekweekt uit menselijke cellen in een zachte scaffold. Deze geënte weefsels kunnen samentrekken bij elektrische stimulatie en bootsen echte spier na. Wanneer C4BPA aanwezig was tijdens hun vorming, waren de resulterende vezels dunner en produceerden ze zwakkere twitch- en tetanische krachten, met aanwijzingen voor snellere vermoeidheid. Ten slotte vroegen de onderzoekers of het blokkeren van C4BPA een deel van de schade ongedaan kon maken. Met een genetische stillegmethode om C4BPA-productie in DMD-FAPs te verminderen, co-kweekt men deze gemodificeerde cellen met gezonde myoblasten. De vorming van spiertubes verbeterde: meer myoblasten versmolten en elke buis bevatte meer kernen, wat aangeeft dat het dempen van C4BPA de ondersteunende rol van FAPs gedeeltelijk herstelt.
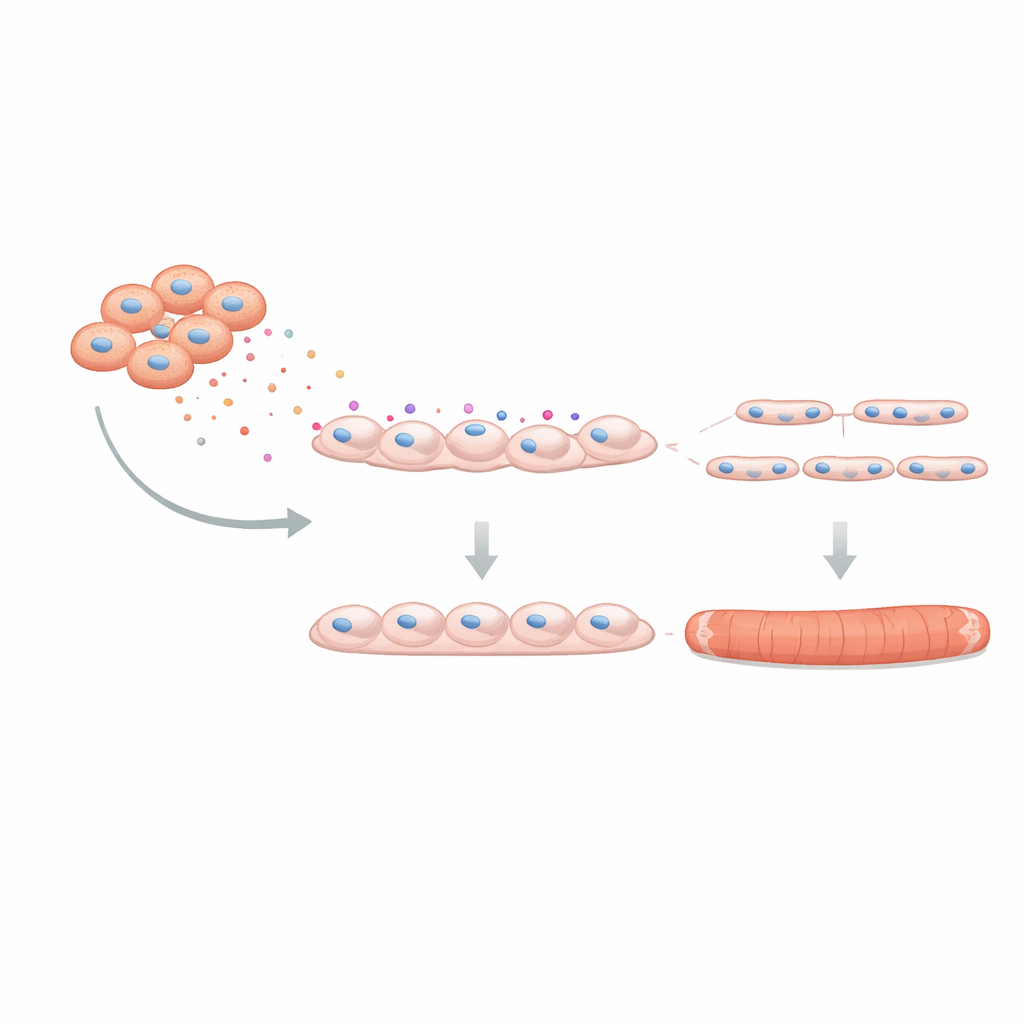
Wat dit betekent voor toekomstige behandelingen
Deze studie onthult dat in Duchenne spierdystrofie ondersteunende cellen in de spier “slechte buren” worden door overproductie van C4BPA, een proteïne dat de groei en functie van nieuwe spiervezels verstoort. Hoewel dit de onderliggende genetische fout in dystrofine niet repareert, kan het richten op C4BPA of soortgelijke uitgescheiden factoren helpen de resterende spier te behouden en het weefsel ontvankelijker te houden voor opkomende gen- en celtherapieën. Simpel gezegd suggereert het werk dat de behandeling van DMD niet alleen het herstellen van de spier zelf vereist, maar ook het tot rust brengen van de omliggende “bouwploeg” zodat regeneratie kan doorgaan in plaats van geblokkeerd te worden.
Bronvermelding: Fernández-Simón, E., Tejedera-Villafranca, A., Fernández-Garabay, X. et al. Impact of C4BPA on Muscle progenitor cell differentiation: insights for Duchenne muscular dystrophy treatment. Cell Death Dis 17, 313 (2026). https://doi.org/10.1038/s41419-026-08588-2
Trefwoorden: Duchenne spierdystrofie, spierregeneratie, fibroadipogene progenitoren, C4BPA, spierstamcellen