Clear Sky Science · fr
Impact de C4BPA sur la différenciation des progéniteurs musculaires : enseignements pour le traitement de la dystrophie musculaire de Duchenne
Pourquoi cette histoire musculaire compte
La dystrophie musculaire de Duchenne (DMD) est une maladie infantile grave qui prive progressivement les garçons de leur capacité à marcher, à respirer et à vivre de manière autonome. La plupart des recherches se sont concentrées sur les fibres musculaires elles‑mêmes, fragiles parce qu’elles manquent d’une protéine clé, la dystrophine. Cet article porte plutôt sur les « voisins » des cellules musculaires — des cellules de soutien qui aident normalement à réparer les dommages — et montre comment, dans la DMD, elles commencent à saboter la reconstruction musculaire via une seule protéine sécrétée. Comprendre ce coupable caché pourrait ouvrir de nouvelles voies pour ralentir la maladie et renforcer les futures thérapies géniques.
Des aides qui deviennent des obstacles
Nos muscles ne se réparent pas seuls. Lorsqu’un dommage survient, des cellules dormantes de type souches, appelées myoblastes, se réveillent, se divisent et fusionnent pour former de nouvelles fibres musculaires. Autour d’elles vivent des cellules progénitrices fibroadipogéniques, ou FAPs, qui déposent normalement un échafaudage temporaire et aident à coordonner la réparation. Dans un muscle sain, ces FAPs se multiplient brièvement puis disparaissent une fois la guérison achevée. Dans la DMD, cependant, elles restent activées, et le muscle se remplit progressivement de cicatrice et de graisse. Les auteurs se sont demandé : ces FAPs altérées interfèrent‑elles directement avec la capacité des myoblastes à former de nouvelles fibres ?
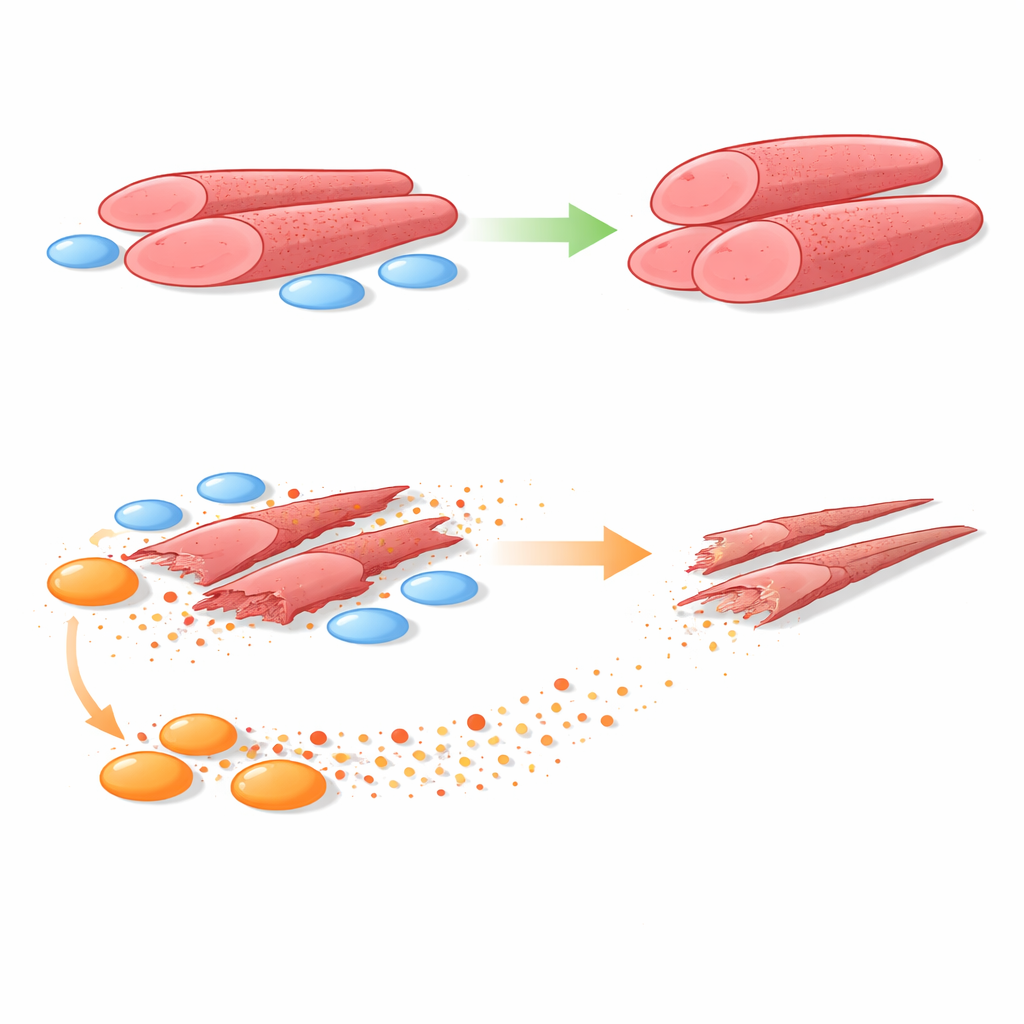
Tests côte à côte de cellules saines et malades
Pour répondre à cette question, l’équipe a cultivé des myoblastes humains avec des FAPs prélevées sur des biopsies musculaires de garçons sains et de garçons atteints de DMD. Ils ont utilisé des systèmes permettant soit un contact direct entre les deux types cellulaires, soit une séparation par une barrière poreuse laissant passer uniquement les molécules sécrétées. Dans les deux configurations, les FAPs saines encourageaient les myoblastes à former des tubes musculaires plus grands et plus robustes. En net contraste, les FAPs issues de DMD réduisaient systématiquement la taille de ces tubes et le nombre de noyaux qu’ils contenaient — signes évidents d’une formation musculaire altérée. Lorsque le contact physique était supprimé, les FAPs de DMD faisaient toujours des dégâts, ce qui pointe vers des facteurs solubles comme principaux responsables.
À la recherche d’un signal toxique
Les chercheurs ont ensuite catalogué les protéines libérées par les FAPs saines et celles de DMD en utilisant la spectrométrie de masse, une technique capable d’identifier des centaines de molécules à la fois. Sur 760 protéines détectées, près de la moitié étaient plus abondantes dans les FAPs de DMD. En recoupant cette liste avec les récepteurs présents sur les cellules musculaires humaines, ils ont réduit le nombre de candidats à 29 protéines susceptibles d’agir sur les myoblastes. Des tests complémentaires ont isolé une protéine clé, appelée C4BPA, nettement plus élevée dans les cultures de FAPs de DMD et également détectée à des taux augmentés dans le sang et le tissu musculaire des patients DMD. Lorsque des myoblastes sains ont été exposés in vitro à du C4BPA purifié, leur capacité à fusionner en longs tubes épais a fortement diminué, les gènes favorisant la croissance musculaire étaient réprimés tandis que des gènes associés à la fonte musculaire étaient activés.
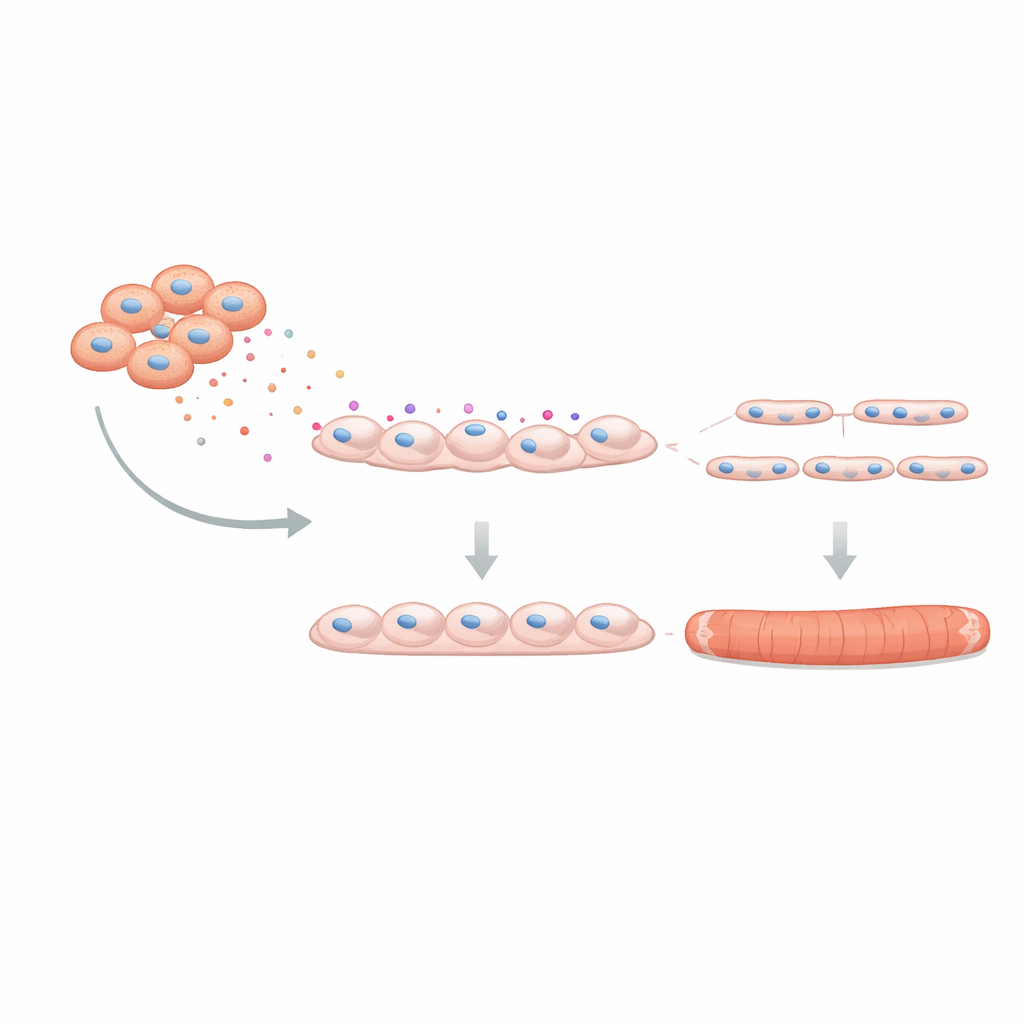
Du plat de culture au muscle reconstitué
Pour vérifier si cet effet avait un impact sur la fonction musculaire réelle, l’équipe a utilisé un « mini‑muscle » tridimensionnel cultivé à partir de cellules humaines dans un échafaudage souple. Ces tissus ingénierés peuvent se contracter lorsqu’ils sont stimulés électriquement, imitant le muscle réel. Lorsque le C4BPA était présent lors de leur formation, les fibres obtenues étaient plus fines et produisaient des forces de contraction (twitch et tetanique) plus faibles, avec des signes de fatigue précoce. Enfin, les chercheurs ont testé si bloquer le C4BPA pouvait inverser une partie des dégâts. En réduisant génétiquement la production de C4BPA dans des FAPs de DMD, puis en co‑cultivant ces cellules modifiées avec des myoblastes sains, la formation des tubes musculaires s’est améliorée : davantage de myoblastes ont fusionné et chaque tube contenait plus de noyaux, indiquant qu’atténuer le C4BPA restaure partiellement le rôle de soutien que les FAPs devraient jouer.
Ce que cela signifie pour les traitements futurs
Cette étude révèle que, dans la dystrophie musculaire de Duchenne, les cellules de soutien du muscle deviennent de « mauvais voisins » en surproduisant C4BPA, une protéine qui perturbe la croissance et la fonction des nouvelles fibres musculaires. Bien que cela ne corrige pas le défaut génétique sous‑jacent de la dystrophine, cibler le C4BPA ou des facteurs sécrétés similaires pourrait aider à préserver le muscle restant et à rendre le tissu plus réceptif aux thérapies géniques et cellulaires émergentes. En termes simples, le travail suggère que traiter la DMD pourrait nécessiter non seulement de réparer les « briques » musculaires mais aussi d’apaiser l’« équipe de construction » environnante pour permettre à la régénération de se dérouler au lieu d’être bloquée.
Citation: Fernández-Simón, E., Tejedera-Villafranca, A., Fernández-Garabay, X. et al. Impact of C4BPA on Muscle progenitor cell differentiation: insights for Duchenne muscular dystrophy treatment. Cell Death Dis 17, 313 (2026). https://doi.org/10.1038/s41419-026-08588-2
Mots-clés: Dystrophie musculaire de Duchenne, régénération musculaire, progéniteurs fibroadipogéniques, C4BPA, cellules souches musculaires