Clear Sky Science · he
השפעת C4BPA על התמיינות תאי פרוגניור שריר: תובנות לטיפול בנוירומשריית Duchenne
למה הסיפור הזה של השריר חשוב
נוירומשריית Duchenne (DMD) היא מחלה קשה בילדות שמאיטה את היכולת של בנים ללכת, לנשום ולחיות באופן עצמאי. רוב המחקר התמקד בסיבי השריר עצמם, הרגישים משום שהם חסרים חלבון מרכזי הנקרא דיסטורפין. מאמר זה בוחן במקום זאת את "השכנים" של תאי השריר — תאי תמיכה שמסייעים בדרך כלל לתיקון הנזק — ומראה כיצד, ב-DMD, הם מתחילים לסכל את שיקומו של השריר דרך חלבון מופרש יחיד. הבנת התוקם הבלתי נראה הזה עשויה לפתוח דרכים חדשות להאט את המחלה ולהגביר את היענותן של תרפיות גנטיות עתידיות.
עוזרים שהופכים למכשולים
השרירים שלנו לא מתחדשים מעצמם. כשמתרחש נזק, תאים דמויי-גזע רדומים הנקראים מיובלסטים מתעוררים, מתחלקים ומתמזגים לסיבי שריר חדשים. סביבם חיים תאי פרוגניור פיברו-שומניים, או FAPs, שבדרך כלל יוצרים תבנית זמנית ועוזרים לתאם את התיקון. בשריר בריא, ה-FAPs מתרחבים לזמן קצר ואז נעלמים כשההחלמה הושלמה. ב-DMD, עם זאת, הם נשארים פעילים, והשריר מתמלא בהדרגה בצלקת ושומן. המחברים רצו לדעת: האם ה-FAPs המשתנים הללו מפריעים ישירות ליכולתם של המיובלסטים ליצור סיבים חדשים?
בדיקות צמודות של תאים בריאים וחולים
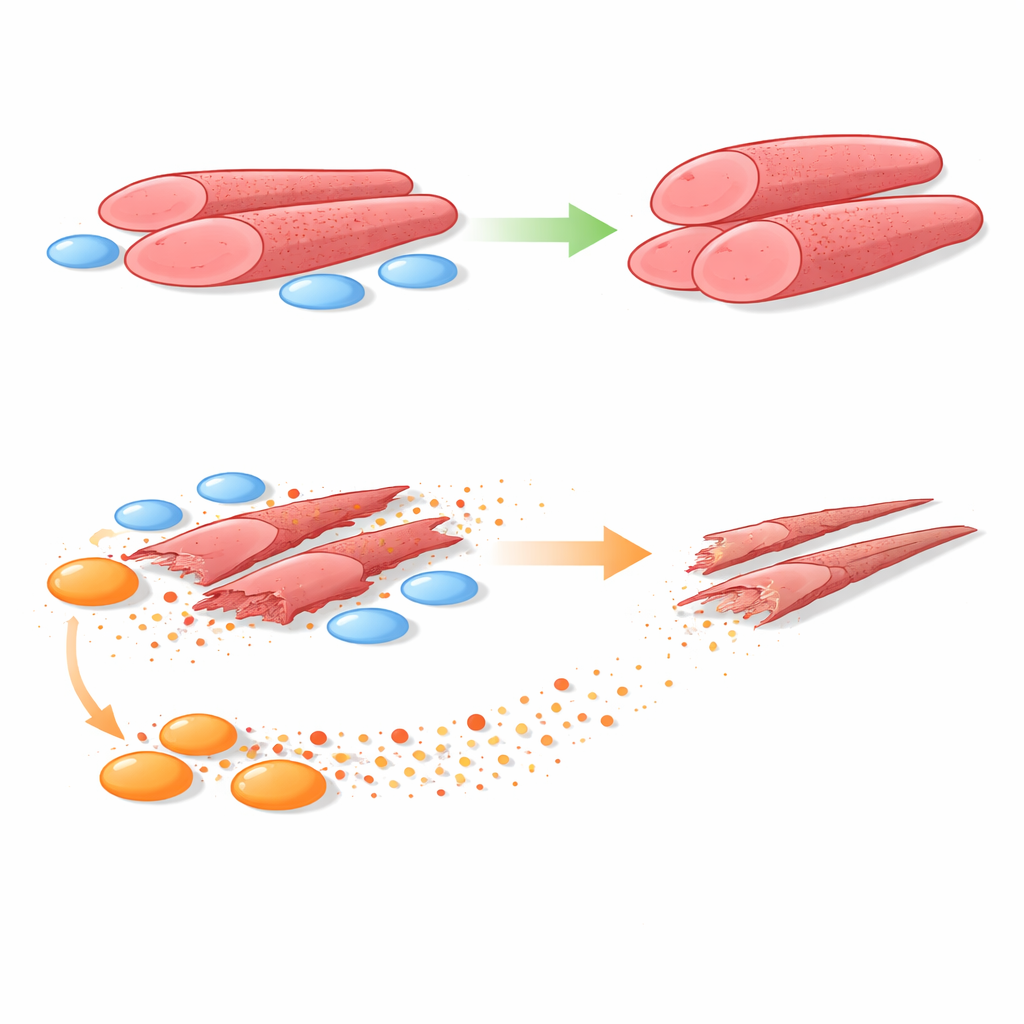
כדי לענות על כך, הצוות גידל מיובלסטים אנושיים יחד עם FAPs שנלקחו מביופסיות שריר של בנים בריאים ושל בנים עם DMD. הם השתמשו במערכות שאיפשרו מגע ישיר בין סוגי התאים או הפרדה באמצעות מחסום נקבובי שמאפשר מעבר רק למולקולות מופרשות. בשתי ההתקנות, ה-FAPs הבריאים עודדו את המיובלסטים ליצור צינורות שריר גדולים וחזקים יותר. בניגוד לכך, FAPs של DMD הקטינו באופן עקבי את גודל הצינורות ומספר הגרעינים בהם — סימנים ברורים להיווצרות שריר לקויה. כאשר המגע הפיזי הוסר, ה-FAPs של DMD עדיין גרמו נזק, מה שמצביע על כך שמדובר בגורמים מסיסים כמבצעים הראשיים.
לרדוף אחרי אות רעיל
החוקרים לאחר מכן רשמו את החלבונים שמשתחררים מ-FAPs בריאים ו-FAPs של DMD באמצעות ספקטרומטריה מסיבית, טכניקה שיכולה לזהות מאות מולקולות במקביל. מתוך 760 חלבונים שזוהו, כמעט מחצית היו בשפע רב יותר ב-FAPs של DMD. על ידי חיתוך רשימה זו מול קולטנים שנמצאים על תאי שריר אנושיים, הם צמצמו את השדה ל-29 מועמדים שיכלו להשפיע באופן סביר על המיובלסטים. בדיקות נוספות זיהו חלבון מפתח אחד, שנקרא C4BPA, שהיה גבוה משמעותית בתרביות FAPs של DMD וכמו כן בדם וברקמות השריר של חולי DMD. כאשר מיובלסטים בריאים נחשפו ל-C4BPA מטוהר במעבדה, יכולתם להתמזג לצינורות ארוכים ועבים הצטמצמה בחדות, וגנים המקדמים גדילה שרירית נדוכו בעוד שגנים הקשורים להתנוונות שריר הועלו.
מצלחת פטרי לשריר מהונדס
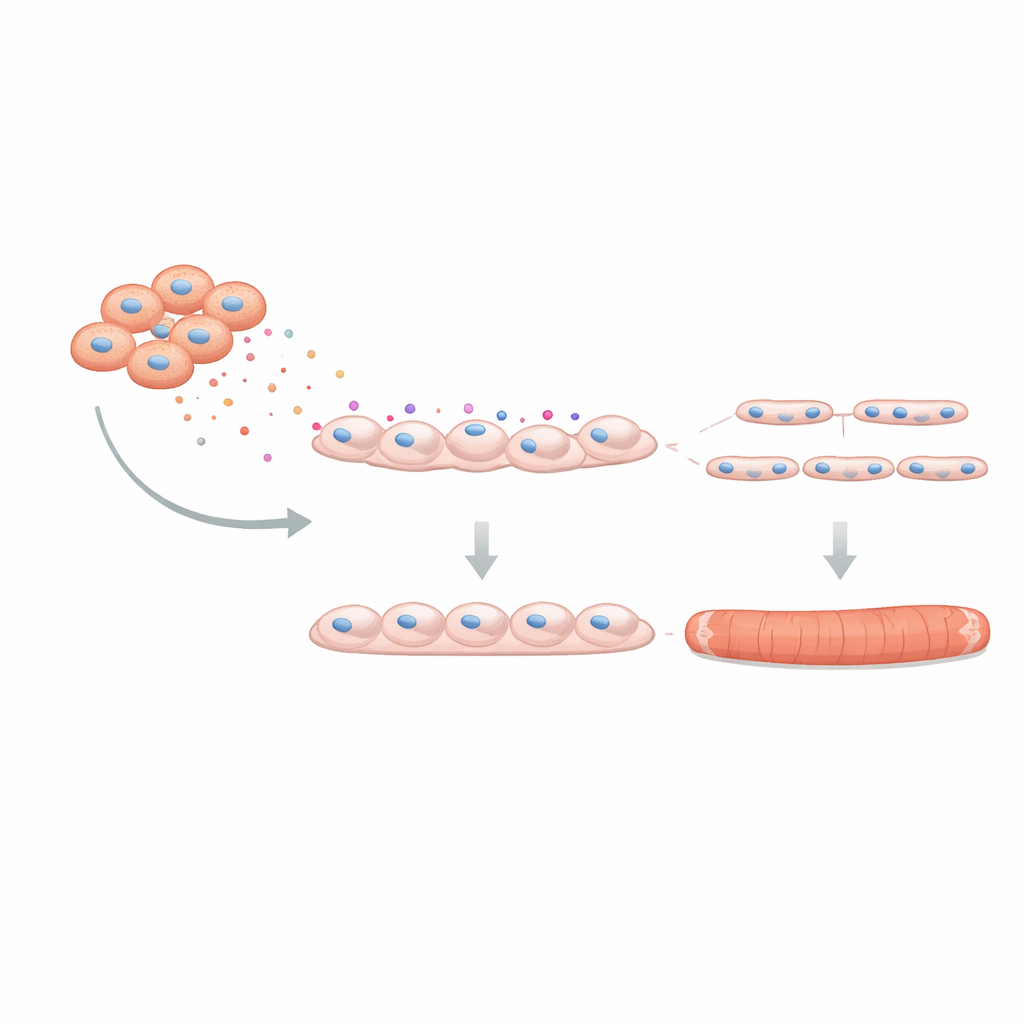
כדי לבדוק האם השפעה זו חשובה לתפקוד שריר אמיתי, הצוות השתמש ב"מיני-שריר" תלת־ממדי שגודל מתאים אנושיים בתוך תבנית רכה. רקמות מהונדסות אלה יכולות להתכווץ כאשר הן מומרצות חשמלית, מדמות שריר אמיתי. כאשר C4BPA נוכח במהלך ההיווצרות שלהן, הסיבים שנוצרו היו דקים יותר וייצרו כוחות טוויץ' וטטנוס חלשים יותר, עם סימנים לעייפות מוקדמת. לבסוף, החוקרים בחנו האם חסימת C4BPA יכולה לבטל חלק מהנזק. באמצעות שיטה של השתקה גנטית להקטין את ייצור ה-C4BPA ב-FAPs של DMD, הם תרבנו תאים ממוטבים אלה יחד עם מיובלסטים בריאים. יצירת צינורות השריר השתפרה: יותר מיובלסטים התמזגו וכל צינור כלל יותר גרעינים, מה שמעיד שהפחתת C4BPA משחזרת חלקית את תפקיד התמיכה ש-FAPs אמורים למלא.
מה המשמעות לטיפולים עתידיים
מחקר זה מראה שבנוירומשריית Duchenne, תאי תמיכה בשריר הופכים ל"שכנים רעים" על ידי ייצור יתר של C4BPA, חלבון שמפריע לגדילה ולתפקוד של סיבים שריריים חדשים. אף שהממצא לא מתקנן את הפגם הגנטי הבסיסי בדיסטורפין, ייצוב C4BPA או גורמים מופרשים דומים עשוי לסייע בשימור השריר הנותר ולהפוך את הרקמה לרגישה יותר לתרפיות גנטיות ותאיות מתפתחות. בפשטות, העבודה מצביעה על כך שעיבוד DMD עשוי לדרוש לא רק תיקון "לבני" השריר אלא גם הרגעת "צוות הבנייה" הסובב כדי שההתחדשות תתקדם במקום להיחסם.
ציטוט: Fernández-Simón, E., Tejedera-Villafranca, A., Fernández-Garabay, X. et al. Impact of C4BPA on Muscle progenitor cell differentiation: insights for Duchenne muscular dystrophy treatment. Cell Death Dis 17, 313 (2026). https://doi.org/10.1038/s41419-026-08588-2
מילות מפתח: נוירומשריית Duchenne, התחדשות שריר, תאי פרוגניור פיברו-שומניים, C4BPA, תאי גזע שריריים