Clear Sky Science · es
Impacto de C4BPA en la diferenciación de células progenitoras musculares: ideas para el tratamiento de la distrofia muscular de Duchenne
Por qué importa esta historia muscular
La distrofia muscular de Duchenne (DMD) es una enfermedad infantil grave que, de forma progresiva, priva a los niños de la capacidad de caminar, respirar y vivir de forma independiente. La mayor parte de la investigación se ha centrado en las fibras musculares en sí, que son frágiles porque carecen de una proteína clave llamada distrofina. Este artículo examina en cambio a los “vecinos” de las células musculares: células de apoyo que normalmente ayudan a reparar el daño, y muestra cómo, en la DMD, comienzan a sabotear la reconstrucción muscular mediante una única proteína secretada. Comprender a este culpable oculto podría abrir nuevas vías para frenar la enfermedad y potenciar futuras terapias génicas.
Ayudantes que se vuelven obstáculos
Nuestros músculos no se reparan por sí solos. Cuando ocurre una lesión, células dormantes con carácter de progenitor llamadas mioblastos despiertan, se dividen y se fusionan en nuevas fibras musculares. A su alrededor viven los progenitores fibroadipogénicos, o FAPs, que normalmente depositan un andamiaje temporal y ayudan a coordinar la reparación. En el músculo sano, estos FAPs se expanden por un tiempo breve y luego desaparecen una vez finalizada la curación. En la DMD, sin embargo, permanecen activados y el músculo se llena gradualmente de cicatriz y grasa. Los autores se preguntaron: ¿interfieren directamente estos FAPs alterados con la capacidad de los mioblastos para formar nuevas fibras?
Pruebas comparadas de células sanas y enfermas
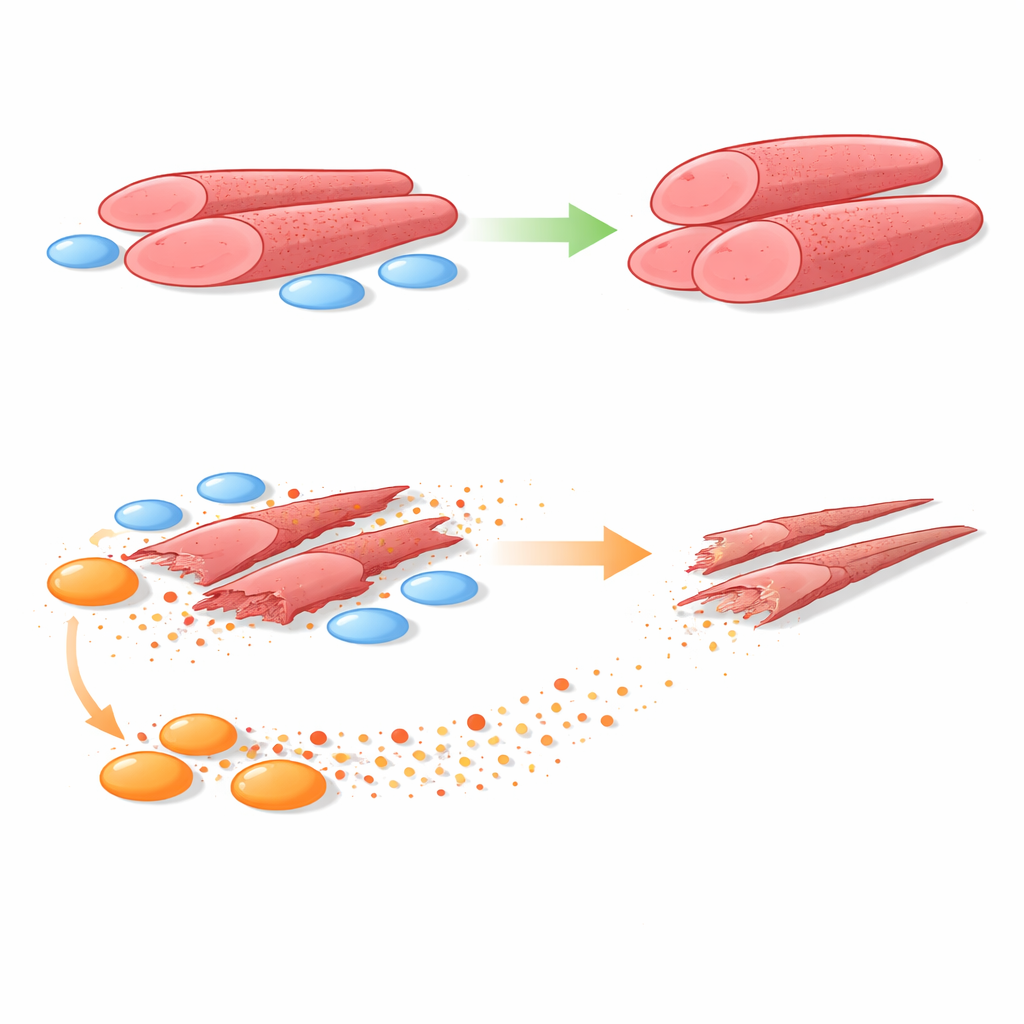
Para responder a esto, el equipo cultivó mioblastos humanos junto con FAPs obtenidos de biopsias musculares de niños sanos y de niños con DMD. Utilizaron sistemas que permitían tanto el contacto directo entre los dos tipos celulares como la separación mediante una barrera porosa que deja pasar solo las moléculas secretadas. En ambos montajes, los FAPs sanos favorecieron que los mioblastos formaran tubos musculares más grandes y robustos. En marcado contraste, los FAPs de DMD redujeron de forma constante el tamaño de estos tubos y el número de núcleos celulares que contenían, señales claras de una formación muscular peor. Cuando se eliminó el contacto físico, los FAPs de DMD siguieron haciendo daño, lo que apunta a factores solubles como los principales responsables.
Rastreando una señal tóxica
Los investigadores catalogaron a continuación las proteínas liberadas por los FAPs sanos y los de DMD mediante espectrometría de masas, una técnica capaz de identificar cientos de moléculas a la vez. De las 760 proteínas detectadas, casi la mitad era más abundante en los FAPs de DMD. Al cruzar esta lista con los receptores presentes en las células musculares humanas, redujeron el campo a 29 candidatos que podrían actuar plausiblemente sobre los mioblastos. Pruebas adicionales identificaron una proteína clave, llamada C4BPA, que estaba marcada y significativamente incrementada en cultivos de FAPs de DMD y también en la sangre y el tejido muscular de pacientes con DMD. Cuando mioblastos sanos se expusieron en el laboratorio a C4BPA purificada, su capacidad de fusionarse en tubos largos y gruesos cayó drásticamente, y los genes que impulsan el crecimiento muscular se reprimieron mientras que los genes asociados al desgaste muscular se activaron.
Del plato de Petri al músculo diseñado
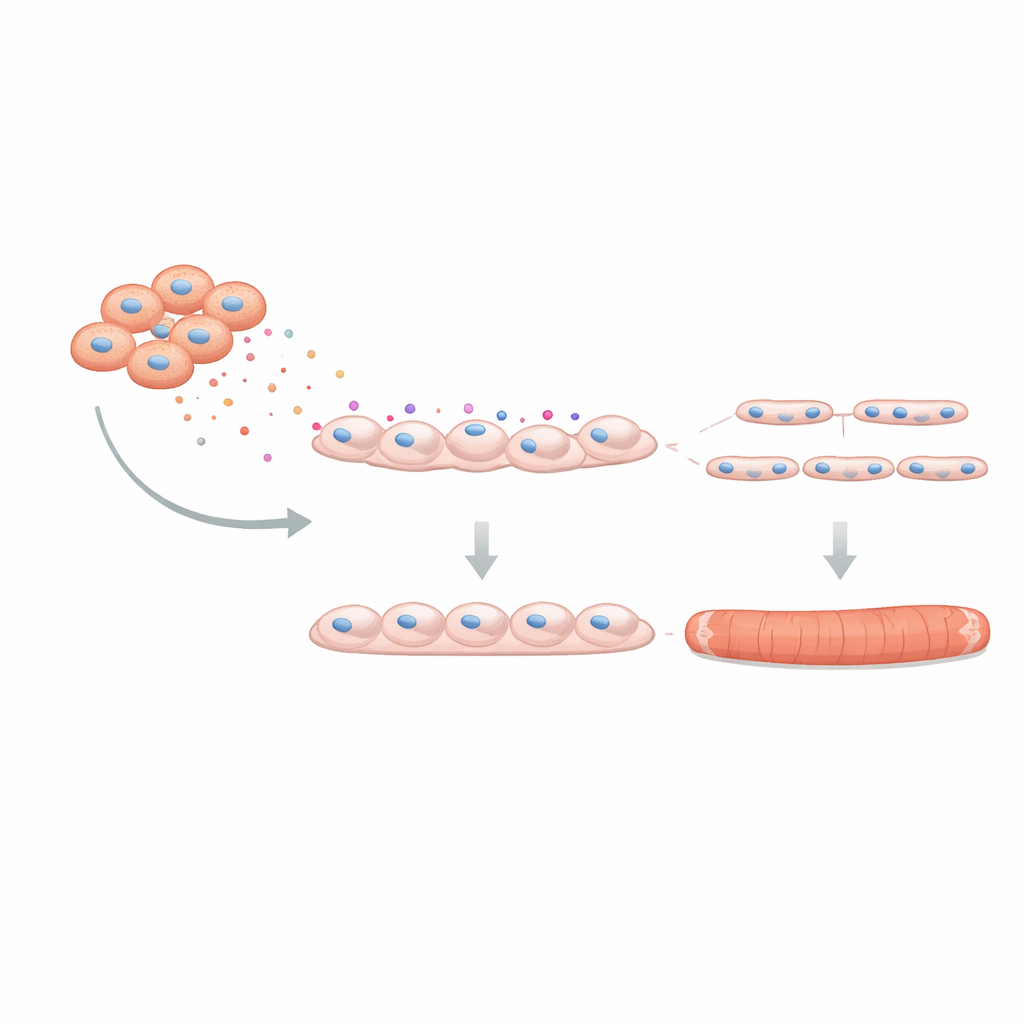
Para comprobar si este efecto importaba para la función muscular real, el equipo utilizó un “mini-músculo” tridimensional crecido a partir de células humanas en un andamio blando. Estos tejidos diseñados pueden contraerse cuando se estimulan eléctricamente, imitando al músculo real. Cuando C4BPA estuvo presente durante su formación, las fibras resultantes eran más delgadas y producían fuerzas de contracción (twitch y tetánicas) más débiles, con signos de fatiga temprana. Finalmente, los investigadores preguntaron si bloquear C4BPA podría deshacer parte del daño. Usando un enfoque de silenciamiento genético para reducir la producción de C4BPA en FAPs de DMD, cocultivaron estas células modificadas con mioblastos sanos. La formación de tubos musculares mejoró: se fusionaron más mioblastos y cada tubo contenía más núcleos, lo que indica que atenuar C4BPA restaura parcialmente el papel de apoyo que deberían desempeñar los FAPs.
Qué significa esto para tratamientos futuros
Este estudio revela que en la distrofia muscular de Duchenne, las células de apoyo en el músculo se convierten en “malos vecinos” al producir en exceso C4BPA, una proteína que perturba el crecimiento y la función de las nuevas fibras musculares. Aunque no corrige el defecto genético subyacente de la distrofina, dirigirse a C4BPA u otros factores secretados similares podría ayudar a preservar el músculo restante y mantener el tejido más receptivo a las terapias génicas y celulares emergentes. En términos sencillos, el trabajo sugiere que tratar la DMD puede requerir no solo reparar los “ladrillos” del músculo, sino también calmar a la “brigada de construcción” circundante para que la regeneración pueda avanzar en lugar de ser bloqueada.
Cita: Fernández-Simón, E., Tejedera-Villafranca, A., Fernández-Garabay, X. et al. Impact of C4BPA on Muscle progenitor cell differentiation: insights for Duchenne muscular dystrophy treatment. Cell Death Dis 17, 313 (2026). https://doi.org/10.1038/s41419-026-08588-2
Palabras clave: Distrofia muscular de Duchenne, regeneración muscular, progenitores fibroadipogénicos, C4BPA, células madre musculares