Clear Sky Science · pl
Wpływ C4BPA na różnicowanie progenitorów mięśniowych: wnioski dla leczenia dystrofii mięśniowej Duchenne’a
Dlaczego ta opowieść o mięśniach ma znaczenie
Dystrofia mięśniowa Duchenne’a (DMD) to ciężka choroba wieku dziecięcego, która stopniowo odbiera chłopcom zdolność chodzenia, oddychania i samodzielnego życia. Większość badań koncentrowała się na samych włóknach mięśniowych, które są kruche z powodu braku kluczowego białka — dystrofiny. Ten artykuł przygląda się zamiast tego „sąsiadom” komórek mięśniowych — komórkom wspierającym, które normalnie pomagają naprawiać uszkodzenia — i pokazuje, jak w DMD zaczynają one sabotować odbudowę mięśni przez jedno wydzielane białko. Zrozumienie tego ukrytego winowajcy może otworzyć nowe drogi do spowolnienia choroby i wzmocnienia przyszłych terapii genowych.
Pomocnicy, którzy stają się przeszkodą
Nasze mięśnie nie naprawiają się same. Gdy dochodzi do uszkodzenia, uśpione, przypominające komórki macierzyste myoblasty budzą się, dzielą i łączą w nowe włókna mięśniowe. W ich otoczeniu występują progenitory fibroadipogenne, czyli FAPy, które zwykle tworzą tymczasowy ruszt i pomagają koordynować naprawę. W zdrowym mięśniu FAPy rozszerzają się na krótko, a potem znikają po zakończeniu gojenia. W DMD natomiast pozostają aktywowane, a mięsień stopniowo wypełnia się blizną i tłuszczem. Autorzy chcieli sprawdzić: czy te zmienione FAPy bezpośrednio utrudniają myoblastom tworzenie nowych włókien?
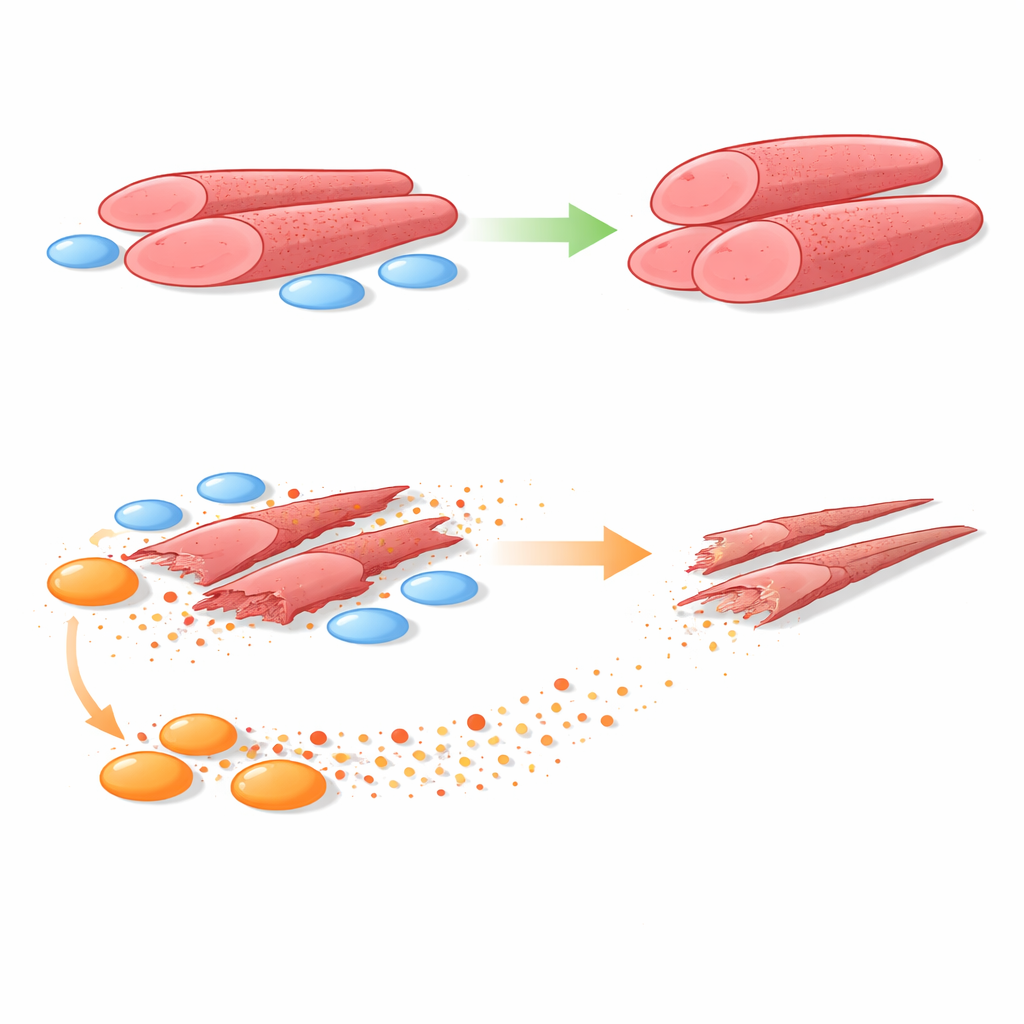
Badania porównawcze zdrowych i chorych komórek
Aby to ustalić, zespół hodował ludzkie myoblasty razem z FAPami pobranymi z biopsji mięśni zdrowych chłopców oraz chłopców z DMD. Użyto systemów pozwalających na bezpośredni kontakt między dwoma typami komórek lub separację za pomocą porowatej bariery przepuszczającej jedynie wydzielane cząsteczki. W obu układach zdrowe FAPy sprzyjały tworzeniu przez myoblasty większych, bardziej odpornych rur mięśniowych. W ostrym kontraście FAPy z DMD konsekwentnie zmniejszały rozmiar tych struktur i liczbę zawartych w nich jąder komórkowych — jasne oznaki gorszej formacji mięśni. Gdy fizyczny kontakt został wyeliminowany, FAPy z DMD nadal szkodziły, co wskazuje, że głównymi sprawcami są czynniki rozpuszczalne.
Śledztwo w sprawie toksycznego sygnału
Następnie badacze skatalogowali białka wydzielane przez zdrowe i DMD FAPy za pomocą spektrometrii mas, techniki potrafiącej zidentyfikować setki molekuł jednocześnie. Spośród 760 wykrytych białek niemal połowa występowała w większej ilości w FAPach DMD. Poprzez korelację tej listy z receptorami obecnymi na ludzkich komórkach mięśniowych zawęzili listę do 29 kandydatów, które mogłyby oddziaływać na myoblasty. Dalsze testy wyodrębniły jedno kluczowe białko o nazwie C4BPA, które było wyraźnie podwyższone w hodowlach FAPów z DMD oraz we krwi i tkance mięśniowej pacjentów z DMD. Gdy zdrowe myoblasty wystawiono w laboratorium na działanie oczyszczonego C4BPA, ich zdolność do łączenia się w długie, grube włókna gwałtownie spadła, a geny napędzające wzrost mięśni zostały przygaszone, podczas gdy geny związane z zanikiem mięśni zostały wzmocnione.
Od szalki Petriego do inżynierowanego mięśnia
Aby sprawdzić, czy ten efekt ma znaczenie dla rzeczywistej funkcji mięśni, zespół użył trójwymiarowego „mini-mięśnia” hodowanego z ludzkich komórek w miękkim ruszcie. Takie tkanki inżynieryjne mogą się kurczyć po pobudzeniu elektrycznym, naśladując prawdziwy mięsień. Gdy C4BPA był obecny podczas ich formowania, powstałe włókna były cieńsze i wytwarzały słabsze siły skurczowe (twitch i tetanic), z objawami wcześniejszego zmęczenia. Wreszcie badacze zapytali, czy zablokowanie C4BPA może cofnąć część uszkodzeń. Stosując genetyczne wyciszenie w celu zmniejszenia produkcji C4BPA w FAPach z DMD, współhodowali te zmodyfikowane komórki ze zdrowymi myoblastami. Tworzenie rur mięśniowych poprawiło się: więcej myoblastów zlewało się, a każda rura zawierała więcej jąder, co wskazuje, że stłumienie C4BPA częściowo przywraca wspierającą rolę, jaką FAPy powinny pełnić.
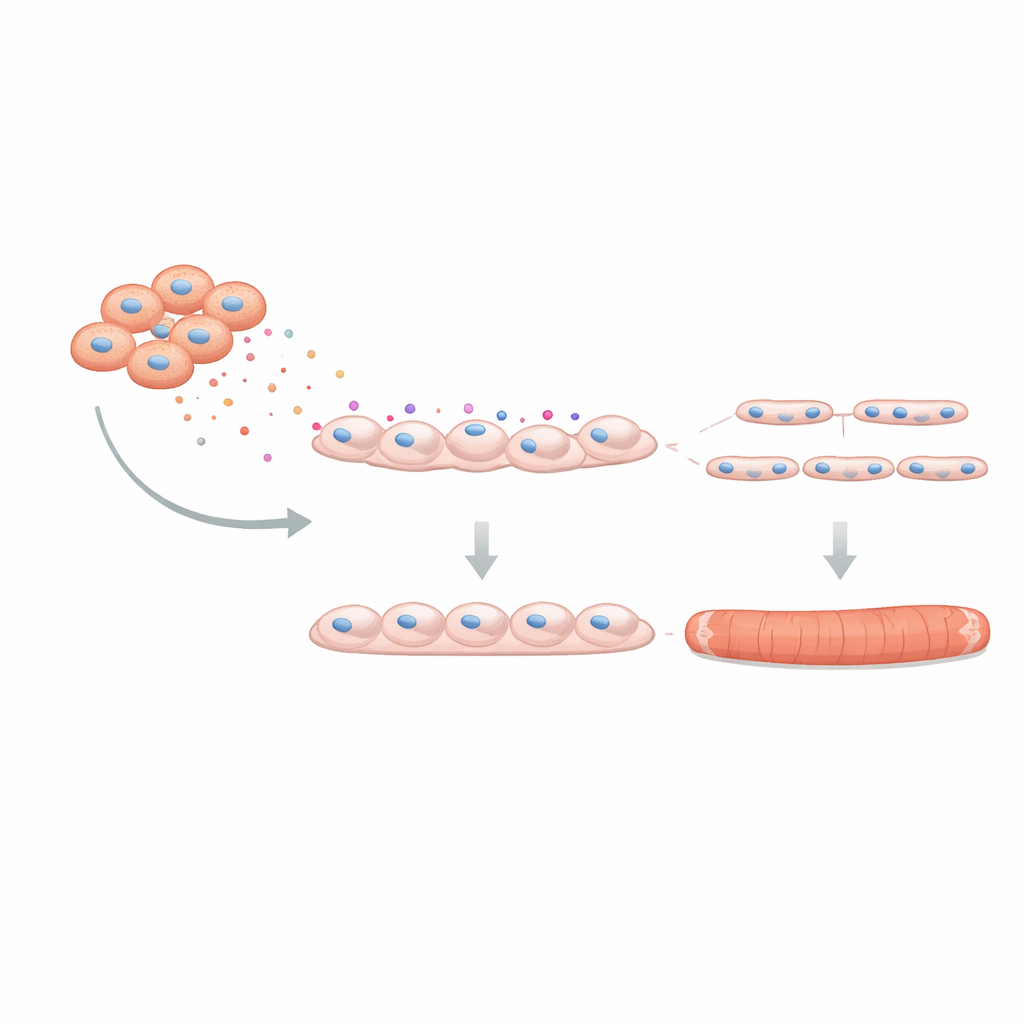
Co to znaczy dla przyszłych terapii
To badanie ukazuje, że w dystrofii mięśniowej Duchenne’a komórki wspierające w mięśniu stają się „złymi sąsiadami” przez nadprodukcję C4BPA — białka, które zaburza wzrost i funkcję nowych włókien mięśniowych. Choć nie naprawia to podstawowego defektu genetycznego dotyczącego dystrofiny, ukierunkowanie na C4BPA lub podobne wydzielane czynniki mogłoby pomóc zachować pozostałą masę mięśniową i utrzymać tkankę bardziej podatną na rozwijające się terapie genowe i komórkowe. Mówiąc prościej, praca ta sugeruje, że leczenie DMD może wymagać nie tylko naprawy „cegieł” mięśnia, lecz także uspokojenia otaczającej „ekipy budowlanej”, aby regeneracja mogła postępować zamiast być blokowana.
Cytowanie: Fernández-Simón, E., Tejedera-Villafranca, A., Fernández-Garabay, X. et al. Impact of C4BPA on Muscle progenitor cell differentiation: insights for Duchenne muscular dystrophy treatment. Cell Death Dis 17, 313 (2026). https://doi.org/10.1038/s41419-026-08588-2
Słowa kluczowe: Dystrofia mięśniowa Duchenne’a, regeneracja mięśni, progenitory fibroadipogenne, C4BPA, komórki macierzyste mięśni