Clear Sky Science · pt
Impacto do C4BPA na diferenciação de células progenitoras musculares: insights para o tratamento da distrofia muscular de Duchenne
Por que esta história muscular importa
A distrofia muscular de Duchenne (DMD) é uma doença infantil grave que, de forma progressiva, tira dos meninos a capacidade de caminhar, respirar e viver de maneira independente. A maior parte das pesquisas concentrou-se nas fibras musculares em si, que são frágeis porque carecem de uma proteína essencial chamada distrofina. Este artigo olha em vez disso para os “vizinhos” das células musculares — células de suporte que normalmente ajudam a reparar danos — e mostra como, na DMD, elas passam a sabotar a reconstrução muscular por meio de uma única proteína secretada. Entender esse culpado oculto pode abrir novas formas de desacelerar a doença e potencializar futuras terapias gênicas.
Ajudantes que viram obstáculos
Meus músculos não se reparam sozinhos. Quando ocorre dano, células dormentes com características de célula-tronco chamadas mioblastos despertam, se dividem e se fundem em novas fibras musculares. Ao redor deles vivem os progenitores fibroadipogênicos, ou FAPs, que normalmente montam um andaime temporário e ajudam a coordenar a reparação. Em músculo saudável, esses FAPs se expandem por um curto período e depois desaparecem quando a cicatrização termina. Na DMD, porém, eles permanecem ativados, e o músculo gradualmente se enche de cicatriz e gordura. Os autores queriam saber: esses FAPs alterados interferem diretamente na capacidade dos mioblastos de formar novas fibras?
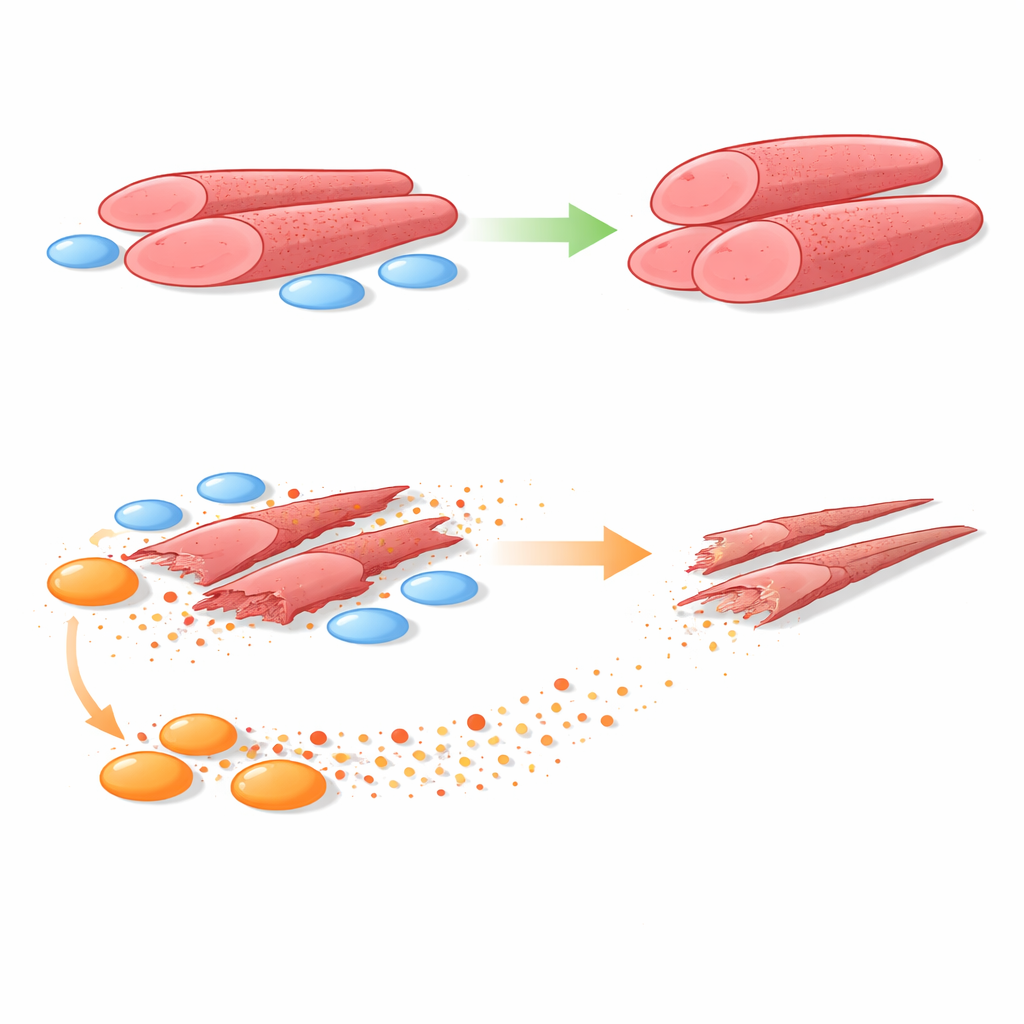
Testes lado a lado com células saudáveis e doentes
Para responder a isso, a equipe cultivou mioblastos humanos junto com FAPs obtidos de biópsias musculares de meninos saudáveis e de meninos com DMD. Eles usaram sistemas que permitiam tanto contato direto entre os dois tipos celulares quanto separação por uma barreira porosa que deixa passar apenas moléculas secretadas. Em ambos os arranjos, FAPs saudáveis incentivaram os mioblastos a formar tubos musculares maiores e mais robustos. Em forte contraste, FAPs de DMD reduziram consistentemente o tamanho desses tubos e o número de núcleos celulares que continham — sinais claros de formação muscular prejudicada. Quando o contato físico foi removido, os FAPs de DMD ainda causaram dano, indicando fatores solúveis como os principais ofensores.
Em busca de um sinal tóxico
Os pesquisadores, em seguida, catalogaram as proteínas liberadas por FAPs saudáveis e por FAPs de DMD usando espectrometria de massa, uma técnica que pode identificar centenas de moléculas de uma só vez. Das 760 proteínas detectadas, quase metade estava mais abundante nos FAPs de DMD. Ao cruzar essa lista com os receptores presentes nas células musculares humanas, eles reduziram o campo para 29 candidatos que poderiam plausivelmente agir sobre os mioblastos. Testes adicionais destacaram uma proteína-chave, chamada C4BPA, que estava marcadamente mais alta em culturas de FAPs de DMD e também no sangue e no tecido muscular de pacientes com DMD. Quando mioblastos saudáveis foram expostos ao C4BPA purificado no laboratório, sua capacidade de fundir-se em tubos longos e espessos caiu acentuadamente, e genes que promovem o crescimento muscular foram reduzidos enquanto genes associados à perda muscular foram ativados.
Do prato de cultura ao músculo engenheirizado
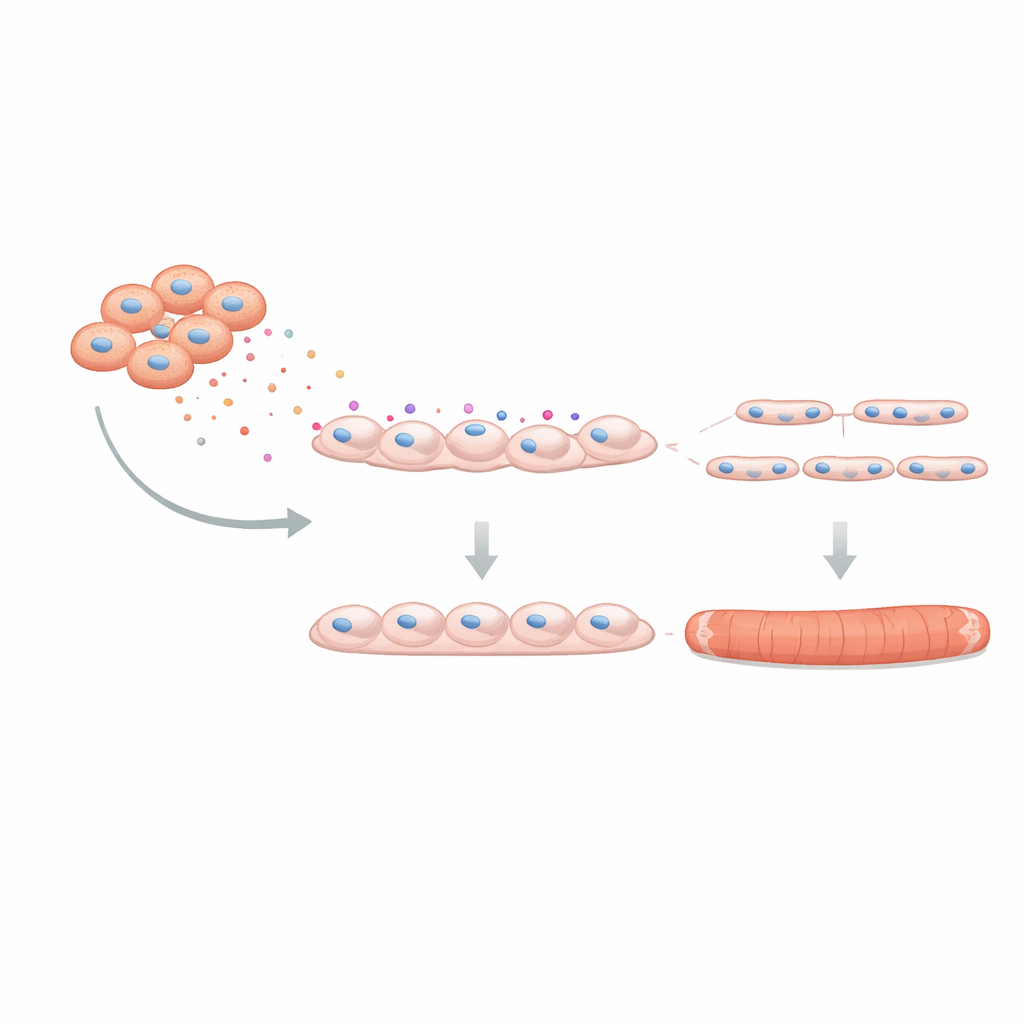
Para avaliar se esse efeito importava para a função muscular real, a equipe usou um “mini-músculo” tridimensional cultivado a partir de células humanas em um andaime maleável. Esses tecidos engenheirizados podem se contrair quando estimulados eletricamente, imitando o músculo verdadeiro. Quando o C4BPA estava presente durante sua formação, as fibras resultantes eram mais finas e produziam forças de contração (twitch e tetânica) mais fracas, com sinais de fadiga precoce. Por fim, os pesquisadores perguntaram se bloquear o C4BPA poderia reverter parte do dano. Usando uma abordagem de silenciamento genético para reduzir a produção de C4BPA em FAPs de DMD, eles cocultivaram essas células modificadas com mioblastos saudáveis. A formação de tubos musculares melhorou: mais mioblastos se fundiram e cada tubo continha mais núcleos, indicando que atenuar o C4BPA restaura parcialmente o papel de suporte que os FAPs deveriam exercer.
O que isso significa para tratamentos futuros
Este estudo revela que, na distrofia muscular de Duchenne, as células de suporte no músculo se tornam “maus vizinhos” ao superproduzirem C4BPA, uma proteína que atrapalha o crescimento e a função de novas fibras musculares. Embora isso não corrija o defeito genético subjacente na distrofina, direcionar o C4BPA ou fatores secretados semelhantes poderia ajudar a preservar o músculo remanescente e manter o tecido mais receptivo às emergentes terapias gênicas e celulares. Em termos simples, o trabalho sugere que tratar a DMD pode exigir não apenas consertar os “tijolos” do músculo, mas também acalmar a “equipe de construção” ao redor para que a regeneração avance em vez de ser bloqueada.
Citação: Fernández-Simón, E., Tejedera-Villafranca, A., Fernández-Garabay, X. et al. Impact of C4BPA on Muscle progenitor cell differentiation: insights for Duchenne muscular dystrophy treatment. Cell Death Dis 17, 313 (2026). https://doi.org/10.1038/s41419-026-08588-2
Palavras-chave: Distrofia muscular de Duchenne, regeneração muscular, progenitores fibroadipogênicos, C4BPA, células-tronco musculares