Clear Sky Science · sv
Påverkan av C4BPA på differentiering av muskelprogenitorceller: insikter för behandling av Duchennes muskeldystrofi
Varför den här muskelfortsättningen är viktig
Duchennes muskeldystrofi (DMD) är en allvarlig barndomssjukdom som gradvis berövar pojkar deras förmåga att gå, andas och leva självständigt. Det mesta av forskningen har fokuserat på muskeltrådarna själva, som är sköra eftersom de saknar ett nyckelprotein kallat dystrofin. Denna artikel granskar istället musklernas ”grannar” — stödceller som normalt hjälper till att reparera skador — och visar hur de vid DMD börjar sabotera muskeltillväxten genom ett enda utsöndrat protein. Att förstå denna dolda syndabock kan öppna nya vägar för att bromsa sjukdomen och förbättra framtida genbaserade behandlingar.
Hjälpare som blir hinder
Våra muskler reparerar sig inte ensamma. När skada uppstår vaknar vilande, stamliknande celler kallade myoblaster, delar sig och smälter samman till nya muskelfibrer. Runt dem finns fibroadipogena progenitorceller, eller FAPs, som normalt lägger en temporär stomme och hjälper till att samordna reparationen. I frisk muskel expanderar dessa FAPs under en kort tid och försvinner sedan när läkningsprocessen är klar. I DMD förblir de däremot aktiverade, och muskeln fylls gradvis med ärrvävnad och fett. Författarna ville veta: stör dessa förändrade FAPs direkt myoblasternas förmåga att bilda nya fibrer?
Sida vid sida: tester av friska och sjuka celler
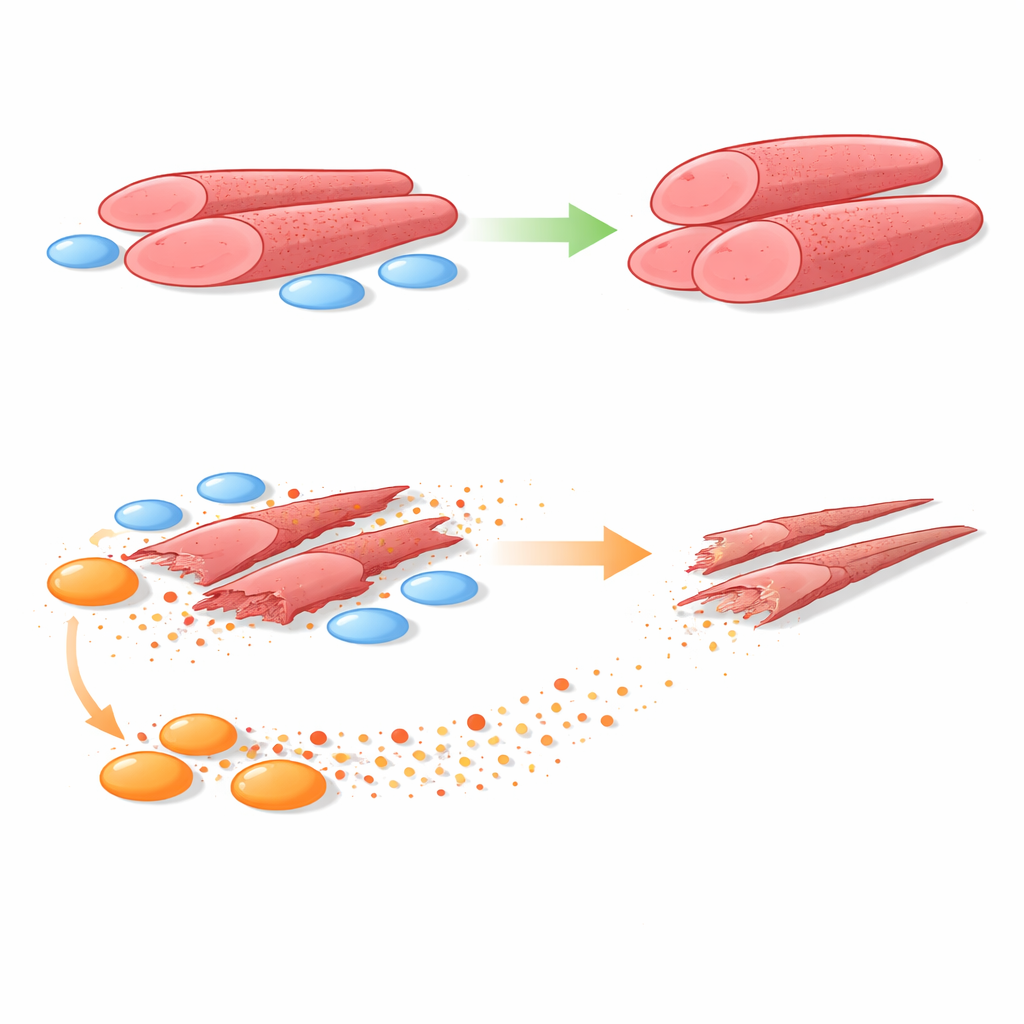
För att svara på det odlade teamet mänskliga myoblaster tillsammans med FAPs hämtade från muskelbiopsier av friska pojkar och pojkar med DMD. De använde system som antingen tillät direktkontakt mellan celltyperna eller separation via en porös barriär som bara släpper igenom utsöndrade molekyler. I båda uppsättningarna uppmuntrade friska FAPs myoblaster att bilda större, mer robusta muskelrör. I skarp kontrast minskade DMD-FAPs konsekvent storleken på dessa rör och antalet cellkärnor de innehöll — tydliga tecken på sämre muskeltillväxt. När fysisk kontakt togs bort orsakade DMD-FAPs fortfarande skada, vilket pekar på lösliga faktorer som huvudsyndare.
På spåret av en toxisk signal
Forskarna katalogiserade nästa de proteiner som frisattes av friska respektive DMD-FAPs med hjälp av masspektrometri, en teknik som kan identifiera hundratals molekyler samtidigt. Av 760 detekterade proteiner var nästan hälften mer rikliga i DMD-FAPs. Genom att jämföra denna lista med receptorer som finns på mänskliga muskelceller begränsade de fältet till 29 kandidater som rimligen skulle kunna påverka myoblaster. Vidare tester pekade ut ett nyckelprotein, kallat C4BPA, som var markant högre i DMD-FAP-kulturer och även i blod och muskelvävnad från DMD-patienter. När friska myoblaster exponerades för renat C4BPA i laboratoriet sjönk deras förmåga att smälta samman till långa, tjocka rör dramatiskt, och gener som driver muskeltillväxt dämpades medan gener kopplade till muskelförtvining ökade.
Från petriskål till konstruerad muskel
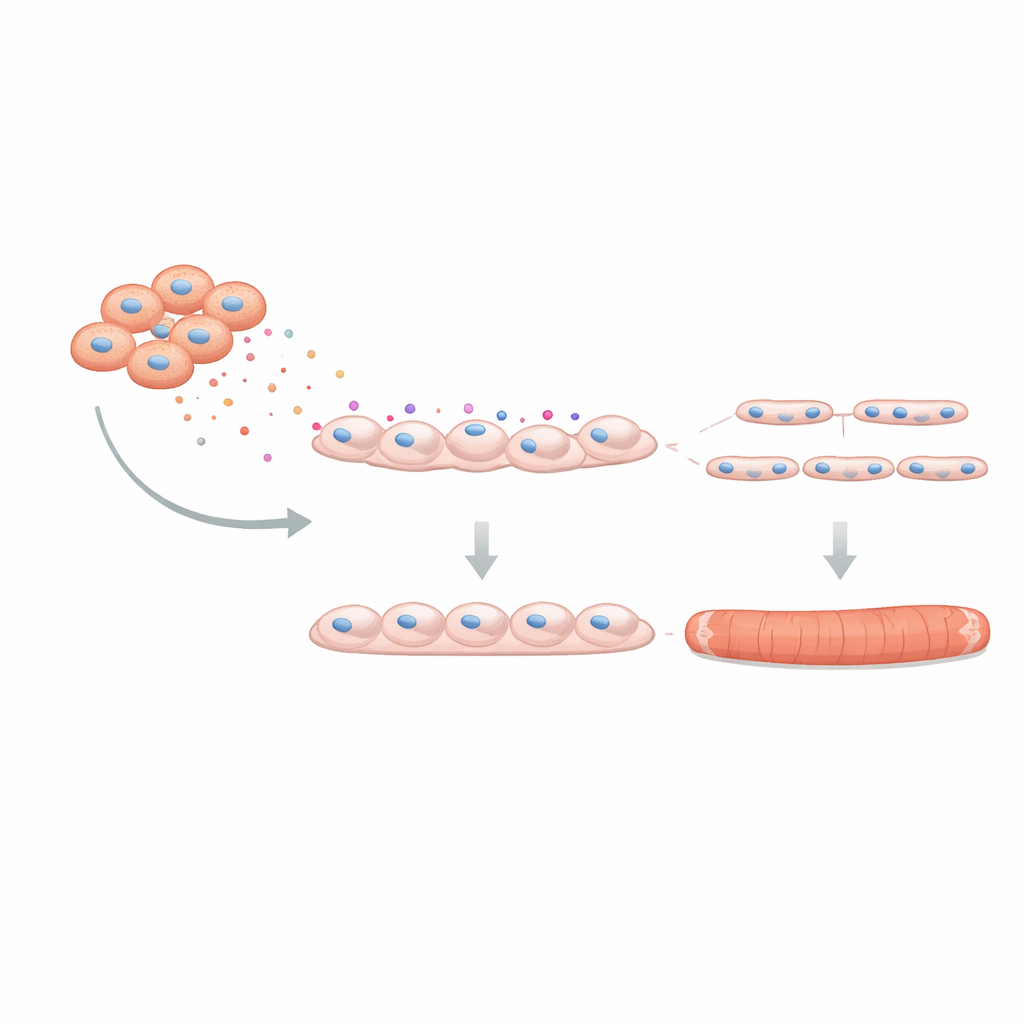
För att se om denna effekt påverkade faktisk muskelfunktion använde teamet en tredimensionell ”mini-muskel” odlad från mänskliga celler i ett mjukt scaffold. Dessa konstruerade vävnader kan kontraheras vid elektrisk stimulering och efterliknar riktig muskel. När C4BPA fanns närvarande under bildningen blev de resulterande fibrerna tunnare och producerade svagare twitched- och tetaniska krafter, med tecken på tidigare utmattning. Slutligen undersökte forskarna om blockering av C4BPA kunde återställa något av skadan. Genom genetisk tystning för att minska C4BPA-produktionen i DMD-FAPs samodlade de dessa modifierade celler med friska myoblaster. Bildningen av muskelrör förbättrades: fler myoblaster smälte samman och varje rör innehöll fler kärnor, vilket indikerar att dämpning av C4BPA delvis återställer den stödjande roll som FAPs borde ha.
Vad detta betyder för framtida behandlingar
Denna studie visar att stödjeceller i muskeln vid Duchennes muskeldystrofi blir ”dåliga grannar” genom att överproducera C4BPA, ett protein som stör tillväxten och funktionen hos nya muskelfibrer. Även om det inte åtgärdar den underliggande genetiska defekten i dystrofin, kan riktade insatser mot C4BPA eller liknande utsöndrade faktorer hjälpa till att bevara kvarvarande muskelmassa och göra vävnaden mer mottaglig för framväxande gen- och cellterapier. I enkla termer antyder arbetet att behandling av DMD kan kräva att man inte bara reparerar muskelns byggstenar utan också lugnar den omgivande ”byggarbetsstyrkan” så att regeneration kan fortskrida istället för att blockeras.
Citering: Fernández-Simón, E., Tejedera-Villafranca, A., Fernández-Garabay, X. et al. Impact of C4BPA on Muscle progenitor cell differentiation: insights for Duchenne muscular dystrophy treatment. Cell Death Dis 17, 313 (2026). https://doi.org/10.1038/s41419-026-08588-2
Nyckelord: Duchennes muskeldystrofi, muskeltillväxt, fibroadipogena progenitorer, C4BPA, muskelstamceller