Clear Sky Science · zh
NUP93 促进 SOX2 的核内转运以激活 G3BP1 转录并削弱胰腺癌对吉西他滨的应答
这项研究为何重要
胰腺癌是最致命的癌症之一,部分原因在于它常常对像吉西他滨这样的化疗药物产生抵抗。该研究揭示了胰腺癌细胞内部的一条隐蔽分子通路,这条通路帮助细胞修复吉西他滨旨在引发的 DNA 损伤。通过将这条链条从细胞边界追溯到遗传核心,作者们发现了一个新的薄弱环节,未来的治疗可能利用该环节来提高化疗的疗效。
核的门卫
每个细胞都将其 DNA 存放在一个受保护的隔室——细胞核内,细胞核上布满了被称为核孔的小型通道。蛋白质 NUP93 是这些通道的关键结构成分。通过挖掘大型癌症数据库并分析患者样本,研究人员发现胰腺导管腺癌中的 NUP93 水平显著高于正常胰腺组织。肿瘤中 NUP93 含量较高的患者其生存率往往更差。体外培养的胰腺癌细胞对 NUP93 尤其依赖:当降低其水平时,这些细胞增殖变慢且克隆形成减少,表明 NUP93 与侵袭性肿瘤行为相关。
癌细胞如何规避化疗
吉西他滨通过在 DNA 复制过程中插入自身来引发错误和断裂,从而阻止肿瘤细胞分裂。然而,癌细胞可以通过激活 DNA 修复系统来反击。比较高 NUP93 与低 NUP93 的肿瘤时,研究组发现参与 DNA 修复的基因在 NUP93 丰富时更为活跃。在细胞实验中,下调 NUP93 使胰腺癌细胞对吉西他滨敏感性大幅增加,而过表达 NUP93 则使细胞更难被杀死。缺失 NUP93 时 DNA 损伤标志增加,过度产生则使其减少;可视化断裂 DNA 的“彗星”实验也证实,缺乏 NUP93 的细胞在药物处理后积累了更多损伤。在小鼠模型中,缺失 NUP93 的肿瘤生长更慢且对吉西他滨的反应更好。
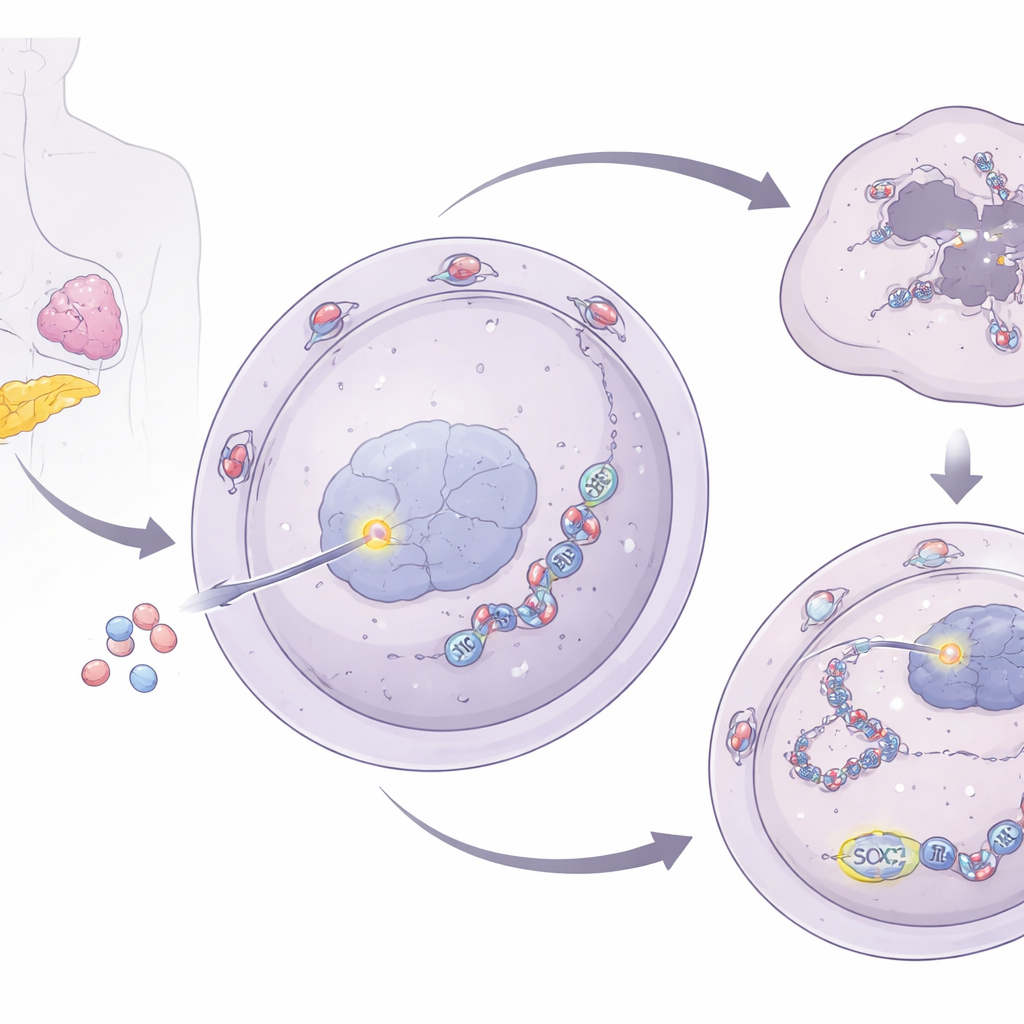
从核门到应激颗粒的中继
为了解 NUP93 如何增强 DNA 修复,研究人员考察了其与细胞应激颗粒的联系——这些是RNA与蛋白质的暂时聚集体,能帮助细胞在恶劣条件下存活。他们发现 NUP93 提升了核心应激颗粒蛋白 G3BP1 的水平。NUP93 增加时 G3BP1 上升;减少时 G3BP1 降低。重要的是,去除 G3BP1 会抵消 NUP93 促进细胞生长和吉西他滨耐药的作用,并在治疗后恢复 DNA 损伤。团队进一步将 G3BP1 的调控追溯到转录因子 SOX2:NUP93 在核孔处与 SOX2 发生物理相互作用并帮助将其运送入核内。进入核内后,SOX2 直接结合 G3BP1 基因的调控区,提升其表达。
从 RNA 保护到 DNA 修复
故事并未止步于 G3BP1。研究人员证明,G3BP1 反过来有助于稳定 RAD51 的信使 RNA(mRNA),RAD51 是一种高保真 DNA 修复通路——同源重组的核心因子。G3BP1 直接结合 RAD51 的 RNA 并减缓其降解,导致 RAD51 蛋白水平升高。有了更多的 RAD51,癌细胞更能修复吉西他滨引起的 DNA 断裂。耗竭 G3BP1 会使 RAD51 水平下降、RAD51 RNA 降解加快并导致 DNA 损伤积累。在小鼠模型中,抑制 SOX2 或 G3BP1 可减少肿瘤生长并显著增强吉西他滨的疗效,证实了这一中继在体内的关键作用。
一个可以帮助化疗发挥作用的新靶点
综述各环节,作者提出了一条明确通路:位于核孔的 NUP93 将 SOX2 送入细胞核,SOX2 激活 G3BP1,G3BP1 保护 RAD51 的 mRNA,从而提高 DNA 修复能力并帮助胰腺癌细胞抵抗吉西他滨。这条 NUP93–SOX2–G3BP1–RAD51 轴像一支内部救援队,修复化疗本应造成的损伤。通过破坏这条链中的一个或多个步骤,未来的疗法可能削弱癌细胞的防御,使现有药物更为有效,为改善这种公认难治疾病的预后带来新的希望。
引用: Sun, H., Yang, C., Du, J. et al. NUP93 facilitates the nuclear import of SOX2 to activate G3BP1 transcription and impairs gemcitabine response in pancreatic cancer. Cell Death Dis 17, 423 (2026). https://doi.org/10.1038/s41419-026-08586-4
关键词: 胰腺癌, 吉西他滨耐药, DNA 修复, 核孔, 应激颗粒