Clear Sky Science · ar
يسهّل NUP93 دخول SOX2 إلى النواة لتفعيل نسخ G3BP1 ويقلّل استجابة سرطان البنكرياس للجمسيتابين
لماذا يهم هذا البحث
يعد سرطان البنكرياس واحدًا من أكثر السرطانات فتكًا، جزئيًا لأنه كثيرًا ما يتجاهل أدوية العلاج الكيميائي مثل الجمسيتابين. يكشف هذا البحث سلسلة خفية من الأحداث الجزيئية داخل خلايا سرطان البنكرياس تساعدها على إصلاح تلف الحمض النووي الذي يفترض أن يسببه الجمسيتابين. من خلال تتبع هذه السلسلة من حدود الخلية إلى نواتها الوراثية، يبرز المؤلفون نقطة ضعف جديدة قد تستغلها علاجات مستقبلية لجعل العلاج الكيميائي أكثر فعالية.
حارس عند نواة الخلية
تحافظ كل خلية على حمضها النووي داخل حجرة محمية تُدعى النواة، والمكسوة ببوابات صغيرة تُعرف بالمسامات النووية. يعد البروتين NUP93 جزءًا هيكليًا أساسيًا لهذه البوابات. من خلال تحليل مجموعات كبيرة من بيانات السرطان وفحص عينات المرضى، وجد الباحثون أن مستويات NUP93 أعلى بكثير في سرطان القناة البنكرياسية الغدي مقارنة بالنسيج البنكرياسي الطبيعي. وارتبطت المستويات الأعلى من NUP93 في الأورام ببقاء أسوأ لدى المرضى. كانت خلايا سرطان البنكرياس المزروعة مخبريًا تعتمد بشكل خاص على NUP93: عندما انخفضت مستوياته، تباطأ نمو هذه الخلايا وتكوّنت مستعمرات أقل، ما يشير إلى ارتباط NUP93 بسلوك ورمي عدواني.
كيف تتجنب الخلايا السرطانية العلاج الكيميائي
يعمل الجمسيتابين عن طريق إدراج نفسه في الحمض النووي أثناء نسخه، مسببًا أخطاءً وكسورًا كان من المفترض أن توقف انقسام الخلايا الورمية. لكن الخلايا السرطانية يمكن أن تقاوم ذلك بتفعيل أنظمة إصلاح الحمض النووي. من خلال مقارنة الأورام ذات المستويات العالية والمنخفضة من NUP93، لاحظ الفريق أن الجينات المشاركة في إصلاح الحمض النووي كانت أكثر نشاطًا عندما كان NUP93 وافرًا. في تجارب خلوية، جعل إسكات NUP93 خلايا سرطان البنكرياس أكثر حساسية للجمسيتابين بكثير، بينما جعلت زيادته من الصعب قتلها. زادت مؤشرات تلف الحمض النووي عند فقدان NUP93 وتراجعت عند إفراطه، وأكد اختبار «المذنبة» الذي يصوّر الحمض النووي المكسور أن الخلايا التي تفتقد NUP93 تراكمت لديها أضرار أكثر بعد العلاج. في الفئران، نمت الأورام الناقصة NUP93 بوتيرة أبطأ واستجابت بشكل أفضل بكثير للجمسيتابين.
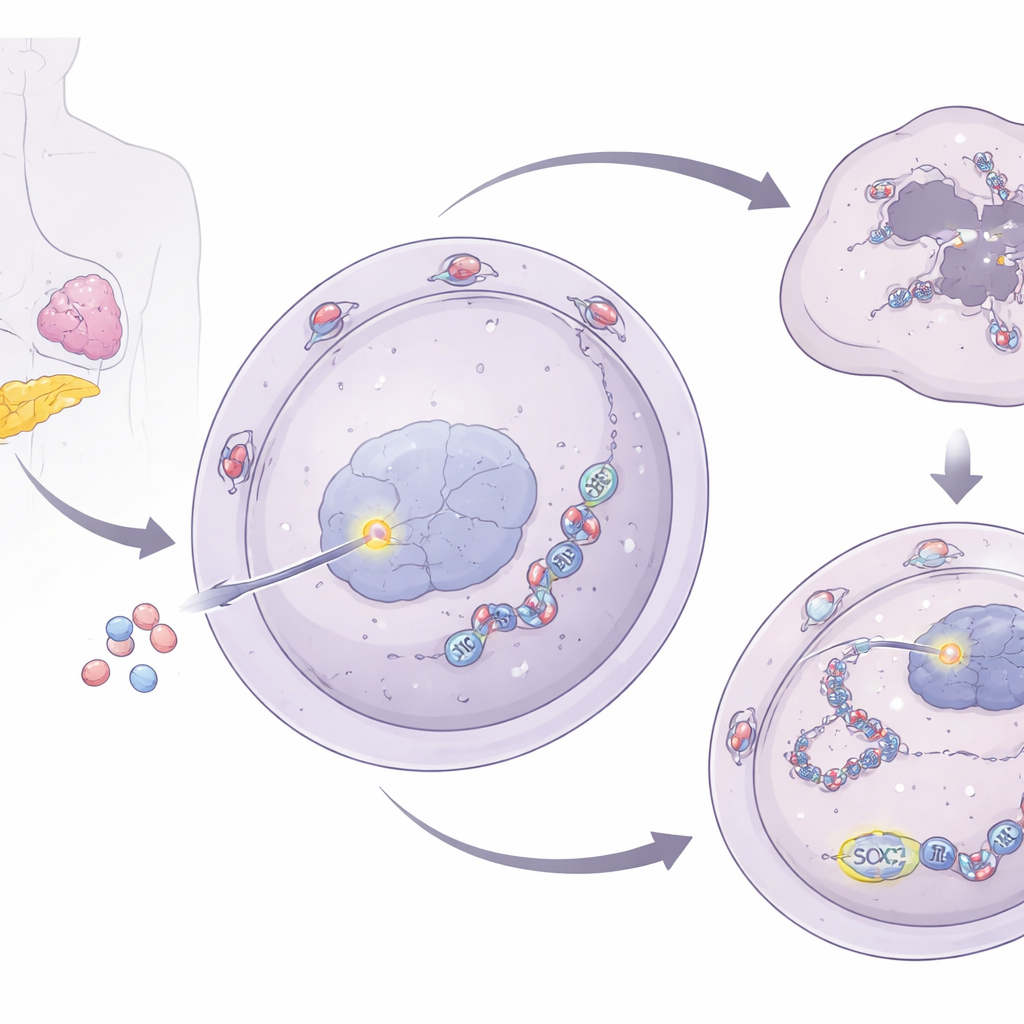
تتابع من بوابة النواة إلى حبيبات الإجهاد
لفهم كيف يعزّز NUP93 إصلاح الحمض النووي، نظر الباحثون في صلاته بحبيبات الإجهاد الخلوية—عناقيد مؤقتة من الرنا والبروتينات تساعد الخلايا على النجاة في ظروف قاسية. اكتشفوا أن NUP93 يزيد من مستويات G3BP1، وهو بروتين أساسي في حبيبات الإجهاد. عند زيادة NUP93، ارتفعت مستويات G3BP1؛ وعند خفض NUP93، انخفضت. والأهم أن إزالة G3BP1 ألغت قدرة NUP93 على تعزيز نمو الخلايا ومقاومة الجمسيتابين وأعادت ظهور تلف الحمض النووي بعد العلاج. ثم تتبّع الفريق سيطرة G3BP1 إلى SOX2، عامل نسخ معروف يشغّل أو يثبط الجينات. يتفاعل NUP93 جسديًا مع SOX2 عند المسام النووية ويساعد في نقله إلى النواة. وبمجرد دخوله، يرتبط SOX2 مباشرة بمنطقة التحكم في جين G3BP1، ما يزيد من إنتاجه.
من حماية الرنا إلى إصلاح الحمض النووي
القصة لا تتوقف عند G3BP1. أوضح الباحثون أن G3BP1 بدوره يساعد على تثبيت الرنا الرسول الخاص بـ RAD51، وهو لاعب مركزي في مسار إصلاح عالي الدقة يسمى الاستبدال المتجانس للحمض النووي. يرتبط G3BP1 مباشرة برنا RAD51 ويبطئ من تحلله، مما يؤدي إلى مستويات أعلى من بروتين RAD51. مع توافر المزيد من RAD51، تصبح الخلايا السرطانية أكثر قدرة على إصلاح الكسور التي يسببها الجمسيتابين. عندما نُقص G3BP1، هبطت مستويات RAD51، تحلل رنا RAD51 أسرع، وتراكم تلف الحمض النووي. في نماذج الفئران، قلّل تعطيل SOX2 أو G3BP1 من نمو الأورام وجعل الجمسيتابين أكثر فعالية بكثير، ما يؤكد أهمية هذا التتابع في أنظمة حية.
هدف جديد لمساعدة العلاج الكيميائي
بجمع القطع معًا، يقترح المؤلفون مسارًا واضحًا: NUP93 عند المسام النووية يقود SOX2 إلى النواة، وSOX2 ينشّط G3BP1، وG3BP1 يحفظ رنا RAD51، ليعزز في النهاية إصلاح الحمض النووي ويُعين خلايا سرطان البنكرياس على مقاومة الجمسيتابين. يعمل محور NUP93–SOX2–G3BP1–RAD51 مثل فريق إنقاذ داخلي يصلح الأضرار التي يفترض أن يسببها العلاج الكيميائي. من خلال تعطيل خطوة أو أكثر في هذه السلسلة، قد تُضعف العلاجات المستقبلية دفاعات الخلايا السرطانية وتجعل الأدوية الحالية أكثر قوة، مما يوفر أملًا جديدًا لتحسين النتائج في هذا المرض المعروف بصعوبة علاجه.
الاستشهاد: Sun, H., Yang, C., Du, J. et al. NUP93 facilitates the nuclear import of SOX2 to activate G3BP1 transcription and impairs gemcitabine response in pancreatic cancer. Cell Death Dis 17, 423 (2026). https://doi.org/10.1038/s41419-026-08586-4
الكلمات المفتاحية: سرطان البنكرياس, مقاومة الجمسيتابين, إصلاح الحمض النووي, المسامات النووية, حبيبات الإجهاد