Clear Sky Science · pl
NUP93 ułatwia import nuklearny SOX2, aktywuje transkrypcję G3BP1 i osłabia odpowiedź na gemcytabinę w raku trzustki
Dlaczego te badania są istotne
Rak trzustki należy do najbardziej śmiertelnych nowotworów, częściowo dlatego, że często opiera się leczeniu chemioterapeutycznemu, takiemu jak gemcytabina. W niniejszym badaniu odkryto ukryty ciąg zdarzeń molekularnych w komórkach raka trzustki, który pomaga naprawiać uszkodzenia DNA wywoływane przez gemcytabinę. Śledząc tę ścieżkę od granicy komórki do jej genetycznego jądra, badacze ujawniają nowe słabe ogniwo, które przyszłe terapie mogłyby wykorzystać, aby poprawić skuteczność chemioterapii.
Strażnik przy jądrze komórkowym
Każda komórka przechowuje DNA w chronionej przegrodzie zwanej jądrem komórkowym, które jest pokryte drobnymi portalami znanymi jako pory jądrowe. Białko NUP93 stanowi kluczowy element konstrukcyjny tych wrót. Analizując duże zbiory danych onkologicznych oraz próbki od pacjentów, badacze stwierdzili, że poziomy NUP93 są znacząco wyższe w gruczolakoraku przewodowym trzustki niż w prawidłowej tkance trzustki. Pacjenci, których guzy zawierały więcej NUP93, mieli zwykle gorsze przeżycie. Hodowane w laboratorium komórki raka trzustki były szczególnie zależne od NUP93: po obniżeniu jego poziomów komórki rosły wolniej i tworzyły mniej kolonii, co wskazuje, że NUP93 wiąże się z agresywnym zachowaniem guza.
Jak komórki nowotworowe unikają chemioterapii
Gemcytabina działa poprzez wbudowywanie się do DNA podczas jego kopiowania, wywołując błędy i pęknięcia, które powinny zatrzymać podziały komórek nowotworowych. Komórki nowotworowe potrafią jednak przeciwdziałać, aktywując układy naprawy DNA. Porównując guzy o wysokim i niskim poziomie NUP93, zespół zauważył, że geny zaangażowane w naprawę DNA są bardziej aktywne przy obfitym NUP93. W eksperymentach komórkowych wyciszenie NUP93 uczyniło komórki raka trzustki znacznie bardziej wrażliwymi na gemcytabinę, podczas gdy dodatkowy NUP93 utrudniał ich eliminację. Markery uszkodzeń DNA wzrastały po utracie NUP93 i malały przy jego nadprodukcji, a test „kometowy” obrazujący złamane DNA potwierdził, że komórki pozbawione NUP93 gromadziły więcej uszkodzeń po leczeniu. U myszy guzy pozbawione NUP93 rosły wolniej i znacznie lepiej reagowały na gemcytabinę.
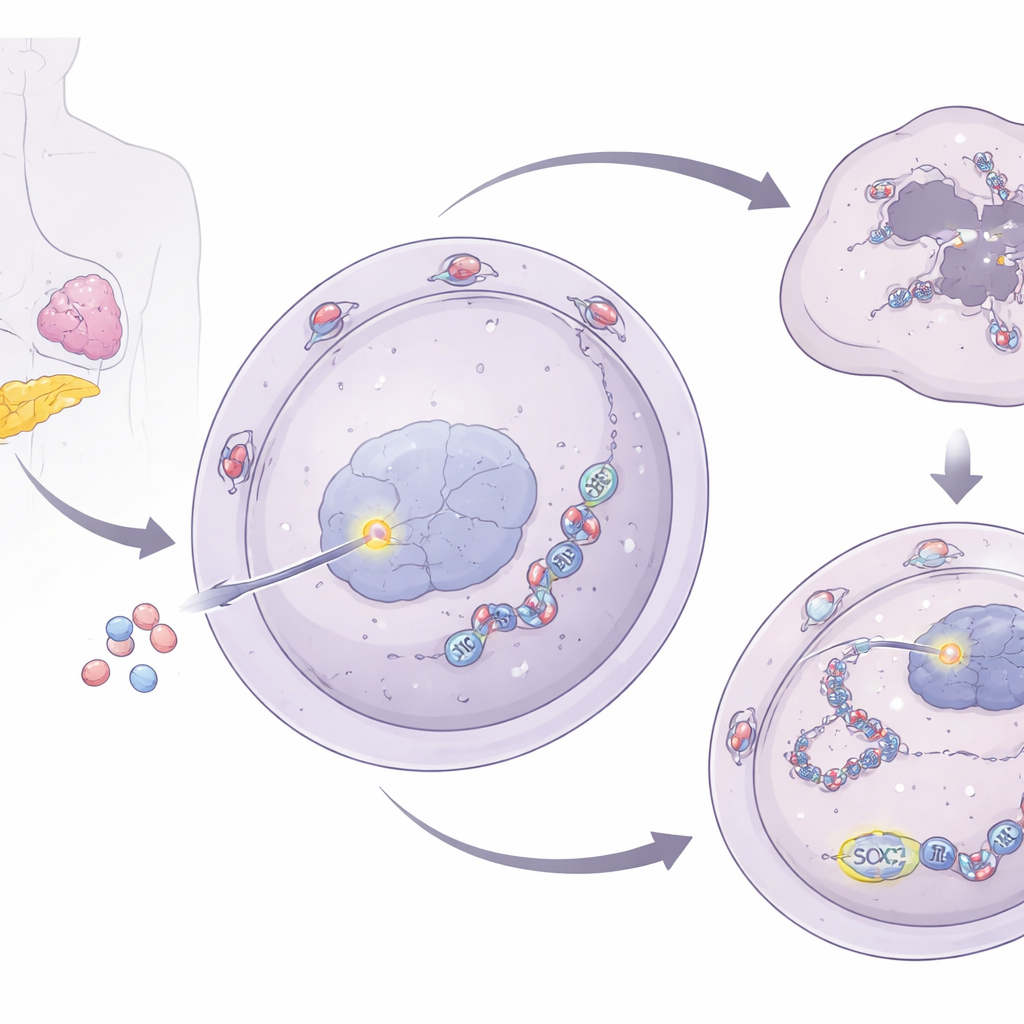
Przekaźnik od bramy jądrowej do cząstek stresowych
Aby zrozumieć, jak NUP93 wzmacnia naprawę DNA, badacze zbadali jego powiązania z komórkowymi cząstkami stresowymi — tymczasowymi skupiskami RNA i białek, które pomagają komórkom przetrwać trudne warunki. Odkryli, że NUP93 podnosi poziomy G3BP1, kluczowego białka cząstek stresowych. Gdy NUP93 był zwiększony, poziom G3BP1 rósł; gdy NUP93 został zredukowany, G3BP1 spadał. Co ważne, usunięcie G3BP1 znosiło zdolność NUP93 do promowania wzrostu komórek i oporności na gemcytabinę oraz przywracało uszkodzenia DNA po leczeniu. Zespół odnalazł następnie kontrolę G3BP1 w czynnika transkrypcyjnego SOX2, dobrze znanego regulatora włączającego i wyłączającego geny. NUP93 fizycznie wchodzi w interakcję z SOX2 przy porze jądrowej i pomaga transportować go do jądra. Po wejściu do jądra SOX2 wiąże się bezpośrednio z regionem kontrolnym genu G3BP1, zwiększając jego ekspresję.
Od ochrony RNA do naprawy DNA
Historia nie kończy się na G3BP1. Badacze wykazali, że G3BP1 z kolei stabilizuje mRNA RAD51, kluczowego komponentu wysokoprecyzyjnej ścieżki naprawy DNA zwanej rekombinacją homologiczna. G3BP1 wiąże się bezpośrednio z RNA RAD51 i spowalnia jego rozkład, prowadząc do wyższych poziomów białka RAD51. Przy większej ilości RAD51 komórki nowotworowe są lepiej wyposażone do naprawy złamań DNA wywołanych gemcytabiną. Po deplecji G3BP1 poziomy RAD51 spadały, RNA RAD51 degradowało się szybciej, a uszkodzenia DNA się kumulowały. W modelach mysich blokada SOX2 lub G3BP1 zmniejszała wzrost guza i znacznie zwiększała skuteczność gemcytabiny, potwierdzając wagę tego przekaźnika in vivo.
Nowy cel poprawiający chemioterapię
Składając elementy w całość, autorzy proponują jasną ścieżkę: NUP93 przy porze jądrowej wprowadza SOX2 do jądra, SOX2 aktywuje G3BP1, a G3BP1 chroni RNA RAD51, ostatecznie wzmacniając naprawę DNA i pomagając komórkom raka trzustki opierać się gemcytabinie. Oś NUP93–SOX2–G3BP1–RAD51 działa jak wewnętrzny zespół ratunkowy naprawiający uszkodzenia, które ma wyrządzić chemioterapia. Zakłócając jeden lub więcej kroków tego łańcucha, przyszłe terapie mogłyby osłabić obronę komórek nowotworowych i zwiększyć skuteczność istniejących leków, dając nową nadzieję na poprawę wyników w tej trudnej do leczenia chorobie.
Cytowanie: Sun, H., Yang, C., Du, J. et al. NUP93 facilitates the nuclear import of SOX2 to activate G3BP1 transcription and impairs gemcitabine response in pancreatic cancer. Cell Death Dis 17, 423 (2026). https://doi.org/10.1038/s41419-026-08586-4
Słowa kluczowe: rak trzustki, oporność na gemcytabinę, naprawa DNA, bramka jądrowa, cząstki stresowe