Clear Sky Science · nl
NUP93 vergemakkelijkt de nucleaire import van SOX2 om de transcriptie van G3BP1 te activeren en vermindert de respons op gemcitabine bij pancreaskanker
Waarom dit onderzoek ertoe doet
Pancreaskanker is een van de dodelijkste vormen van kanker, deels omdat het vaak chemotherapie zoals gemcitabine weet te weerstaan. Deze studie onthult een verborgen keten van moleculaire gebeurtenissen in pancreaskankercellen die hen helpt het DNA-schade te herstellen die gemcitabine juist zou moeten veroorzaken. Door deze keten te volgen van de celgrens naar de genetische kern, laten de auteurs een nieuw kwetsbaar punt zien dat toekomstige therapieën mogelijk kunnen benutten om chemotherapie effectiever te maken.
Een poortwachter bij de kern van de cel
Elke cel bewaart zijn DNA in een beschermde ruimte genaamd de kern, die bezaaid is met kleine doorgangen die nucleaire poriën worden genoemd. Het eiwit NUP93 is een belangrijk structureel onderdeel van deze poorten. Door grote kankerdatasets te analyseren en patiëntmonsters te onderzoeken, vonden de onderzoekers dat NUP93-niveaus aanzienlijk hoger zijn in pancreatisch ductaal adenocarcinoom dan in normaal pancreasweefsel. Patiënten wiens tumoren meer NUP93 bevatten, hadden doorgaans een slechtere overleving. In in-vitro gekweekte pancreaskankercellen waren die cellen bijzonder afhankelijk van NUP93: wanneer de niveaus werden verlaagd, groeiden deze cellen langzamer en vormden ze minder kolonies, wat aangeeft dat NUP93 gekoppeld is aan agressief tumorgedrag.
Hoe kankercellen chemotherapie ontwijken
Gemcitabine werkt door zich in te voegen in DNA tijdens de replicatie, waardoor fouten en breuken ontstaan die tumorcellen zouden moeten stoppen met delen. Kankercellen kunnen echter terugvechten door DNA-herstelsystemen te activeren. Door tumoren met hoge en lage NUP93-niveaus te vergelijken, zag het team dat genen die betrokken zijn bij DNA-herstel actiever waren wanneer NUP93 overvloedig aanwezig was. In celexperimenten maakte het onderdrukken van NUP93 pancreaskankercellen veel gevoeliger voor gemcitabine, terwijl extra NUP93 ze moeilijker te doden maakte. Merkers van DNA-schade namen toe wanneer NUP93 verdwenen was en namen af bij overexpressie; een "komet"-assay die gebroken DNA visualiseert, bevestigde dat cellen zonder NUP93 meer schade opstapelden na medicamenteuze behandeling. In muismodellen groeiden tumoren zonder NUP93 langzamer en reageerden veel beter op gemcitabine.
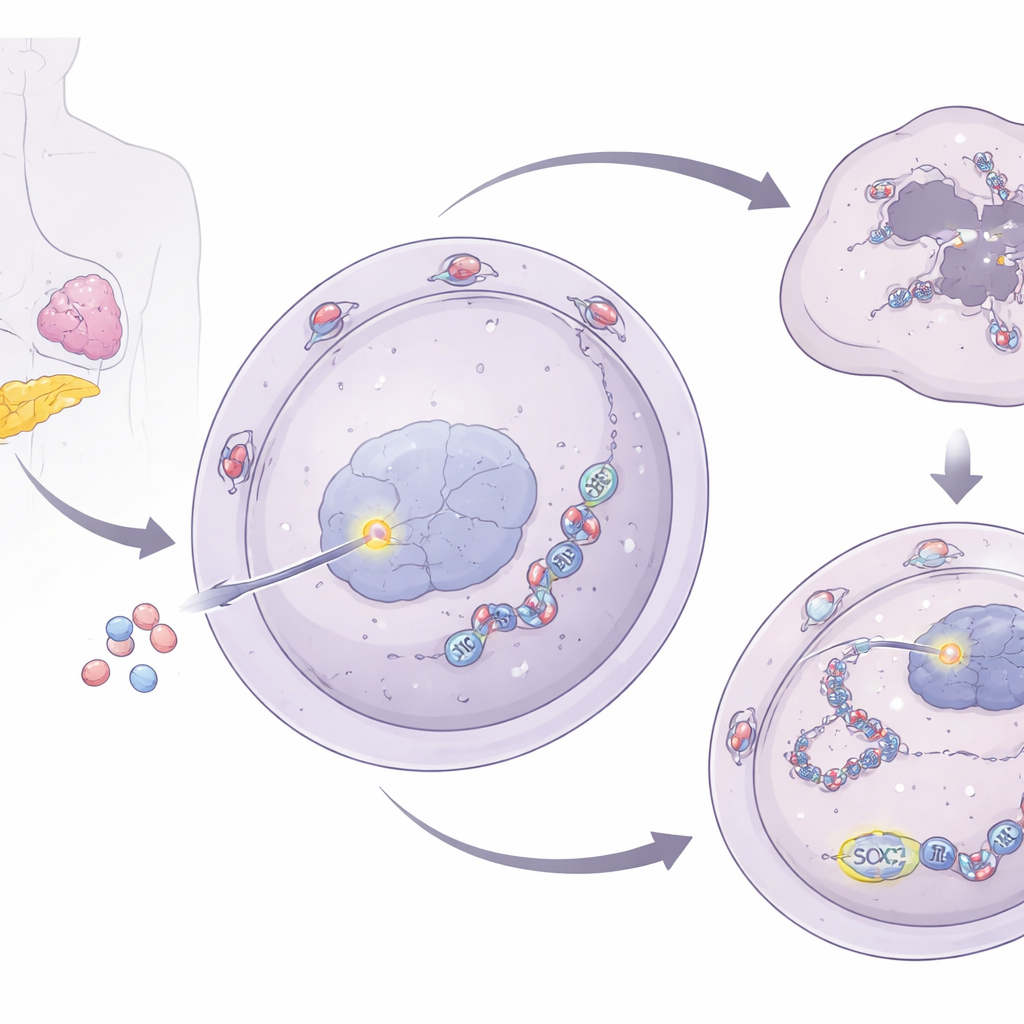
Een relais van de nucleaire poort naar stressgranules
Om te begrijpen hoe NUP93 DNA-herstel versterkt, onderzochten de onderzoekers de verbindingen met cellulaire stressgranules—tijdelijke clusters van RNA en eiwitten die cellen helpen overleven onder stress. Ze ontdekten dat NUP93 de niveaus van G3BP1 verhoogt, een kern-eiwit van stressgranules. Wanneer NUP93 werd verhoogd, steeg G3BP1; wanneer NUP93 werd verlaagd, daalde G3BP1. Belangrijk is dat het verwijderen van G3BP1 NUP93’s vermogen om celgroei en gemcitabine-resistentie te bevorderen teniet deed en de DNA-schade na behandeling herstelde. Het team traceerde de controle over G3BP1 vervolgens terug naar SOX2, een bekende transcriptiefactor die genen aan- of uitzet. NUP93 interageert fysiek met SOX2 bij de nucleaire porie en helpt bij het transport naar de kern. Eenmaal binnen bindt SOX2 direct aan de regelregio van het G3BP1-gen en verhoogt zo de productie ervan.
Van RNA-bescherming naar DNA-herstel
Het verhaal eindigt niet bij G3BP1. De onderzoekers lieten zien dat G3BP1 op zijn beurt helpt het boodschapper-RNA (mRNA) van RAD51 te stabiliseren, een centrale speler in een nauwkeurig DNA-herstelpad genaamd homologe recombinatie. G3BP1 bindt direct aan RAD51-RNA en vertraagt de afbraak, wat leidt tot hogere RAD51-eiwitniveaus. Met meer RAD51 beschikbaar zijn kankercellen beter uitgerust om gemcitabine-geïnduceerde DNA-breuken te herstellen. Wanneer G3BP1 werd uitgeput, daalden RAD51-niveaus, degradeerde RAD51-RNA sneller en stapelde DNA-schade zich op. In muismodellen verminderde het blokkeren van SOX2 of G3BP1 tumorgroei en maakte gemcitabine veel effectiever, wat het belang van dit relais in levende systemen bevestigt.
Een nieuw doelwit om chemotherapie te versterken
Als de onderdelen bij elkaar worden gebracht, stellen de auteurs een duidelijk pad voor: NUP93 bij de nucleaire porie begeleidt SOX2 de kern in, SOX2 activeert G3BP1, en G3BP1 behoudt RAD51-RNA, wat uiteindelijk DNA-herstel versterkt en pancreaskankercellen helpt resistent te zijn tegen gemcitabine. Deze NUP93–SOX2–G3BP1–RAD51-as werkt als een interne reddingseenheid die de schade herstelt die chemotherapie zou moeten toebrengen. Door een of meer stappen in deze keten te verstoren, zouden toekomstige therapieën de verdediging van kankercellen kunnen verzwakken en bestaande geneesmiddelen krachtiger kunnen maken, wat nieuwe hoop biedt voor het verbeteren van de uitkomsten bij deze berucht moeilijk te behandelen ziekte.
Bronvermelding: Sun, H., Yang, C., Du, J. et al. NUP93 facilitates the nuclear import of SOX2 to activate G3BP1 transcription and impairs gemcitabine response in pancreatic cancer. Cell Death Dis 17, 423 (2026). https://doi.org/10.1038/s41419-026-08586-4
Trefwoorden: pancreaskanker, resistentie tegen gemcitabine, DNA-herstel, nucleaire porie, stressgranules