Clear Sky Science · it
NUP93 facilita l'importazione nucleare di SOX2 per attivare la trascrizione di G3BP1 e compromette la risposta al gemcitabina nel carcinoma pancreatico
Perché questa ricerca è importante
Il carcinoma pancreatico è uno dei tumori più letali, in parte perché spesso resiste ai farmaci chemioterapici come il gemcitabina. Questo studio svela una catena nascosta di eventi molecolari all’interno delle cellule del carcinoma pancreatico che le aiuta a riparare il danno al DNA che il gemcitabina dovrebbe causare. Tracciando questa catena dal confine cellulare al nucleo genetico, gli autori rivelano un nuovo punto debole che terapie future potrebbero sfruttare per migliorare l’efficacia della chemioterapia.
Un guardiano al nucleo della cellula
Ogni cellula conserva il proprio DNA in un compartimento protetto chiamato nucleo, che è costellato di minuscoli varchi noti come pori nucleari. La proteina NUP93 è una componente strutturale chiave di questi varchi. Analizzando grandi dataset sul cancro e campioni di pazienti, i ricercatori hanno scoperto che i livelli di NUP93 sono significativamente più alti nell’adenocarcinoma duttale pancreatico rispetto al tessuto pancreatico normale. I pazienti i cui tumori esprimevano più NUP93 tendevano ad avere una sopravvivenza peggiore. Cellule di carcinoma pancreatico coltivate in laboratorio dipendevano particolarmente da NUP93: quando i suoi livelli venivano ridotti, queste cellule crescevano più lentamente e formavano meno colonie, indicando che NUP93 è legato a un comportamento tumorale aggressivo.
Come le cellule tumorali eludono la chemioterapia
Il gemcitabina agisce inserendosi nel DNA durante la replicazione, provocando errori e rotture che dovrebbero impedire la divisione delle cellule tumorali. Le cellule cancerose, tuttavia, possono contrattaccare attivando sistemi di riparazione del DNA. Confrontando tumori con livelli alti e bassi di NUP93, il team ha osservato che i geni coinvolti nella riparazione del DNA risultavano più attivi quando NUP93 era abbondante. In esperimenti cellulari, il silenziamento di NUP93 ha reso le cellule di carcinoma pancreatico molto più sensibili al gemcitabina, mentre un eccesso di NUP93 le rendeva più difficili da uccidere. I marcatori di danno al DNA aumentavano quando NUP93 veniva perso e diminuivano quando era sovraespresso, e un saggio a “cometa” che visualizza il DNA frammentato ha confermato che le cellule prive di NUP93 accumulavano più danni dopo il trattamento con il farmaco. Nei modelli murini, i tumori privi di NUP93 crescevano più lentamente e rispondevano molto meglio al gemcitabina.
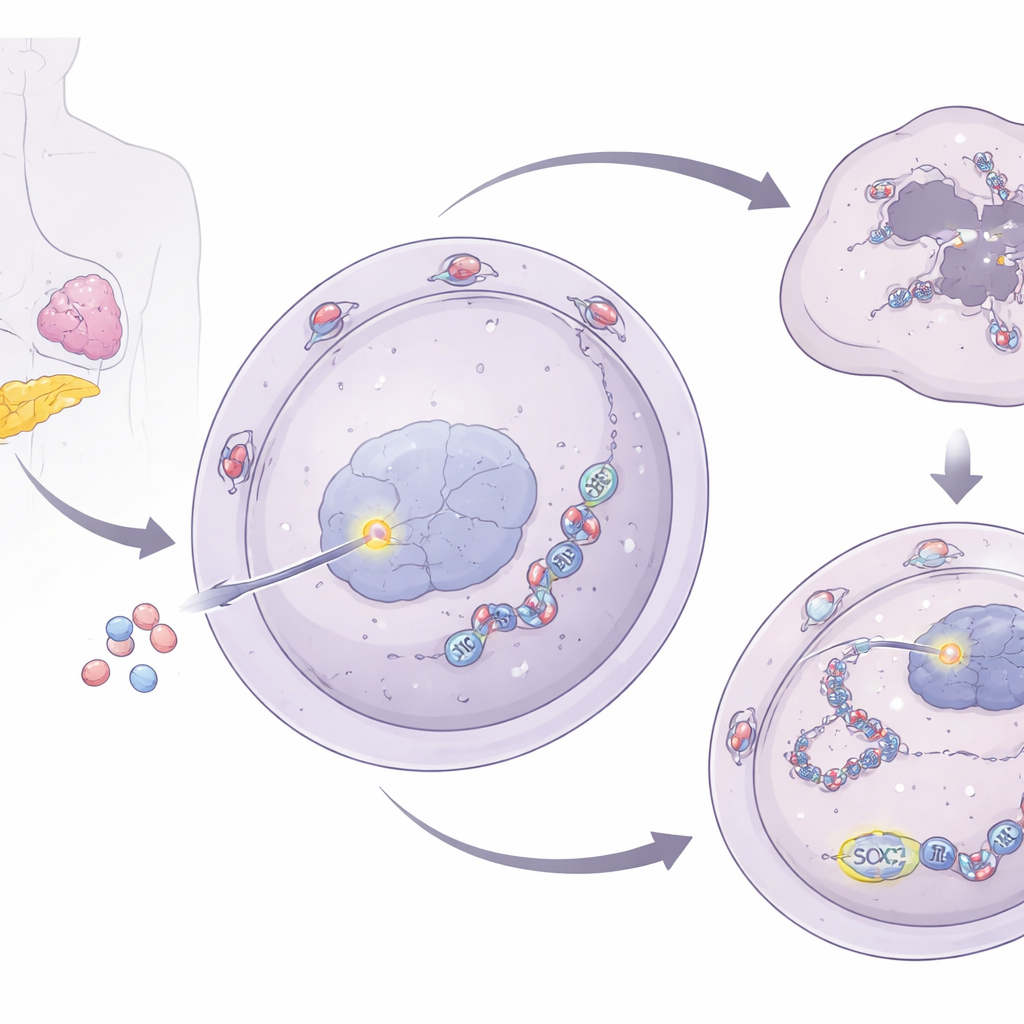
Una staffetta dal varco nucleare ai granuli di stress
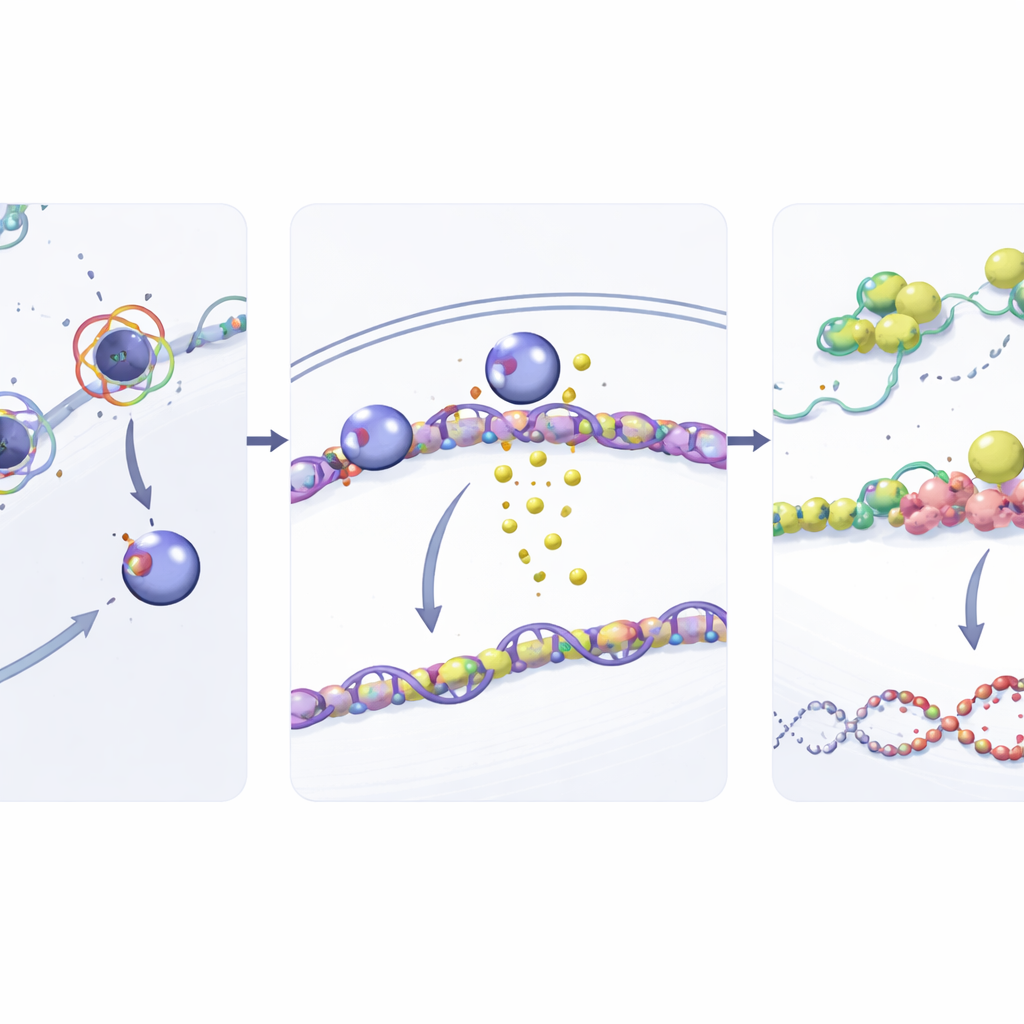
Per capire come NUP93 rafforzi la riparazione del DNA, i ricercatori hanno studiato i suoi legami con i granuli di stress cellulari—aggregati temporanei di RNA e proteine che aiutano le cellule a sopravvivere in condizioni avverse. Hanno scoperto che NUP93 aumenta i livelli di G3BP1, una proteina centrale dei granuli di stress. Quando NUP93 era aumentato, i livelli di G3BP1 salivano; quando NUP93 veniva ridotto, G3BP1 diminuiva. È importante che la rimozione di G3BP1 annullasse la capacità di NUP93 di promuovere la crescita cellulare e la resistenza al gemcitabina e ripristinasse il danno al DNA dopo il trattamento. Il team ha quindi ricondotto il controllo di G3BP1 a SOX2, un fattore di trascrizione noto che attiva o spegne i geni. NUP93 interagisce fisicamente con SOX2 al poro nucleare e ne facilita il trasporto nel nucleo. Una volta all’interno, SOX2 si lega direttamente alla regione regolatoria del gene G3BP1, aumentando la sua espressione.
Dalla protezione dell’RNA alla riparazione del DNA
La storia non finisce con G3BP1. I ricercatori hanno mostrato che G3BP1, a sua volta, aiuta a stabilizzare l’RNA messaggero di RAD51, un attore centrale in una via di riparazione del DNA ad alta fedeltà chiamata ricombinazione omologa. G3BP1 si lega direttamente all’RNA di RAD51 e ne rallenta la degradazione, portando a livelli proteici di RAD51 più elevati. Con più RAD51 disponibile, le cellule tumorali sono meglio attrezzate per riparare le rotture del DNA indotte dal gemcitabina. Quando G3BP1 veniva deplezionato, i livelli di RAD51 calavano, l’RNA di RAD51 si degradava più rapidamente e il danno al DNA si accumulateva. Nei modelli murini, bloccare SOX2 o G3BP1 riduceva la crescita tumorale e rendeva il gemcitabina molto più efficace, confermando l’importanza di questa staffetta nei sistemi viventi.
Un nuovo bersaglio per aiutare la chemioterapia
Mettendo insieme i pezzi, gli autori propongono un percorso chiaro: NUP93 al poro nucleare guida SOX2 nel nucleo, SOX2 attiva G3BP1, e G3BP1 preserva l’RNA di RAD51, potenziando in ultima analisi la riparazione del DNA e aiutando le cellule del carcinoma pancreatico a resistere al gemcitabina. Questo asse NUP93–SOX2–G3BP1–RAD51 agisce come una squadra di salvataggio interna che ripara il danno che la chemioterapia dovrebbe infliggere. Interrompendo uno o più passaggi di questa catena, terapie future potrebbero indebolire le difese delle cellule tumorali e rendere i farmaci esistenti più potenti, offrendo nuove speranze per migliorare gli esiti in questa malattia notoriamente difficile da trattare.
Citazione: Sun, H., Yang, C., Du, J. et al. NUP93 facilitates the nuclear import of SOX2 to activate G3BP1 transcription and impairs gemcitabine response in pancreatic cancer. Cell Death Dis 17, 423 (2026). https://doi.org/10.1038/s41419-026-08586-4
Parole chiave: carcinoma pancreatico, resistenza al gemcitabina, riparazione del DNA, pori nucleari, granuli di stress