Clear Sky Science · fr
NUP93 facilite l'importation nucléaire de SOX2 pour activer la transcription de G3BP1 et compromet la réponse au gemcitabine dans le cancer du pancréas
Pourquoi cette recherche est importante
Le cancer du pancréas fait partie des cancers les plus mortels, en partie parce qu’il résiste souvent aux chimiothérapies comme le gemcitabine. Cette étude révèle une chaîne d’événements moléculaires cachée à l’intérieur des cellules cancéreuses pancréatiques qui leur permet de réparer les dommages à l’ADN que le gemcitabine est censé provoquer. En retraçant cette chaîne depuis la frontière cellulaire jusqu’au noyau génétique, les auteurs mettent en lumière une nouvelle vulnérabilité que des traitements futurs pourraient exploiter pour améliorer l’efficacité de la chimiothérapie.
Un gardien à la porte du noyau
Chaque cellule conserve son ADN dans un compartiment protégé nommé noyau, percé de petites portes appelées pores nucléaires. La protéine NUP93 constitue une pièce structurale essentielle de ces portes. En exploitant de vastes bases de données sur le cancer et en analysant des échantillons de patients, les chercheurs ont observé que les niveaux de NUP93 étaient significativement plus élevés dans l’adénocarcinome canalaire du pancréas que dans le tissu pancréatique normal. Les patients dont les tumeurs présentaient davantage de NUP93 avaient tendance à avoir une survie plus faible. Des cellules de cancer pancréatique cultivées en laboratoire dépendaient particulièrement de NUP93 : lorsque ses niveaux étaient réduits, ces cellules se divisaient plus lentement et formaient moins de colonies, indiquant que NUP93 est lié à un comportement tumoral agressif.
Comment les cellules cancéreuses échappent à la chimiothérapie
Le gemcitabine agit en s’incorporant à l’ADN au moment de sa réplication, provoquant des erreurs et des cassures qui devraient arrêter la division des cellules tumorales. Les cellules cancéreuses, cependant, peuvent riposter en activant des systèmes de réparation de l’ADN. En comparant des tumeurs avec des niveaux élevés ou faibles de NUP93, l’équipe a constaté que les gènes impliqués dans la réparation de l’ADN étaient plus actifs lorsque NUP93 était abondant. Dans des expériences cellulaires, l’inhibition de NUP93 rendait les cellules pancréatiques beaucoup plus sensibles au gemcitabine, tandis qu’un excès de NUP93 les rendait plus difficiles à tuer. Les marqueurs de dommages à l’ADN augmentaient lors de la perte de NUP93 et diminuaient lorsqu’il était surproduit, et un test « comète » visualisant l’ADN brisé a confirmé que les cellules dépourvues de NUP93 accumulaient davantage de dommages après traitement. Chez la souris, les tumeurs privées de NUP93 croissaient plus lentement et répondaient bien mieux au gemcitabine.
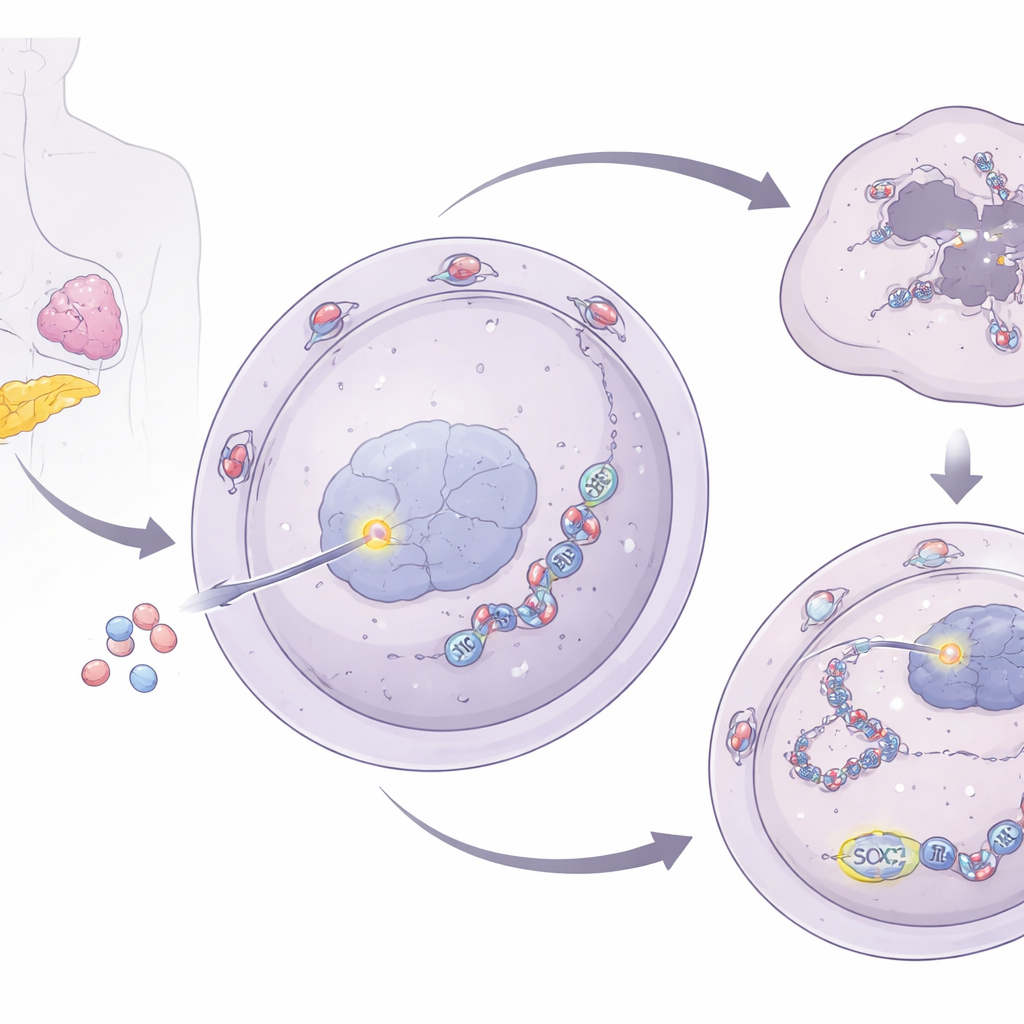
Une transmission du pore nucléaire aux granules de stress
Pour comprendre comment NUP93 renforce la réparation de l’ADN, les chercheurs ont examiné ses liens avec les granules de stress cellulaires — des amas temporaires d’ARN et de protéines qui aident les cellules à survivre en conditions difficiles. Ils ont découvert que NUP93 augmente les niveaux de G3BP1, une protéine centrale des granules de stress. Lorsque NUP93 était augmenté, les niveaux de G3BP1 montaient ; lorsqu’il était réduit, G3BP1 diminuait. Fait important, l’élimination de G3BP1 annulait la capacité de NUP93 à promouvoir la croissance cellulaire et la résistance au gemcitabine et rétablissait les dommages à l’ADN après traitement. L’équipe a ensuite rattaché le contrôle de G3BP1 à SOX2, un facteur de transcription bien connu qui active ou réprime des gènes. NUP93 interagit physiquement avec SOX2 au niveau du pore nucléaire et facilite son transport vers le noyau. Une fois à l’intérieur, SOX2 se lie directement à la région régulatrice du gène G3BP1 et en augmente l’expression.
De la protection de l’ARN à la réparation de l’ADN
L’histoire ne s’arrête pas à G3BP1. Les chercheurs ont montré que G3BP1 contribue à stabiliser l’ARN messager de RAD51, un acteur central d’une voie de réparation de haute fidélité appelée recombinaison homologue. G3BP1 se lie directement à l’ARN de RAD51 et ralentit sa dégradation, entraînant des niveaux protéiques de RAD51 plus élevés. Avec plus de RAD51 disponible, les cellules cancéreuses sont mieux armées pour réparer les cassures d’ADN induites par le gemcitabine. Lorsque G3BP1 était supprimé, les niveaux de RAD51 chutaient, l’ARN de RAD51 se dégradait plus rapidement et les dommages à l’ADN s’accumulaient. Dans des modèles murins, bloquer SOX2 ou G3BP1 réduisait la croissance tumorale et rendait le gemcitabine beaucoup plus efficace, confirmant l’importance de cette chaîne dans des systèmes vivants.
Une nouvelle cible pour améliorer la chimiothérapie
En réunissant les éléments, les auteurs proposent une voie claire : NUP93 au niveau du pore nucléaire accompagne SOX2 vers le noyau, SOX2 active G3BP1, et G3BP1 préserve l’ARN de RAD51, renforçant au final la réparation de l’ADN et aidant les cellules du cancer pancréatique à résister au gemcitabine. Cet axe NUP93–SOX2–G3BP1–RAD51 agit comme une équipe de secours interne qui répare les dommages que la chimiothérapie est censée infliger. En perturbant une ou plusieurs étapes de cette chaîne, des thérapies futures pourraient affaiblir les défenses des cellules cancéreuses et rendre les traitements existants plus puissants, offrant de nouveaux espoirs pour améliorer le pronostic de cette maladie notoirement difficile à traiter.
Citation: Sun, H., Yang, C., Du, J. et al. NUP93 facilitates the nuclear import of SOX2 to activate G3BP1 transcription and impairs gemcitabine response in pancreatic cancer. Cell Death Dis 17, 423 (2026). https://doi.org/10.1038/s41419-026-08586-4
Mots-clés: cancer du pancréas, résistance au gemcitabine, réparation de l'ADN, pore nucléaire, granules de stress