Clear Sky Science · ru
NUP93 облегчает ядерный импорт SOX2 для активации транскрипции G3BP1 и ухудшает ответ на гемцитабин при раке поджелудочной железы
Почему это исследование важно
Рак поджелудочной железы — один из самых смертоносных видов рака, отчасти потому, что часто не реагирует на химиотерапию, например на гемцитабин. В этом исследовании раскрывается скрытая цепочка молекулярных событий внутри клеток рака поджелудочной, которая помогает им восстанавливать те повреждения ДНК, которые должен вызывать гемцитабин. Проследив эту цепь от клеточной периферии до генетического ядра, авторы выявляют новую уязвимость, которую будущие методы лечения могут использовать, чтобы повысить эффективность химиотерапии.
Страж у ядра клетки
Каждая клетка хранит свою ДНК в защищённой структуре — ядре, усыпанном крошечными воротами, известными как ядерные поры. Белок NUP93 является ключевым структурным компонентом этих ворот. Анализируя крупные онкологические базы данных и образцы пациентов, исследователи обнаружили, что уровни NUP93 существенно выше при аденокарциноме протоков поджелудочной железы, чем в нормальной ткани поджелудочной. Пациенты с опухолями, в которых было больше NUP93, как правило, имели худший прогноз выживания. Клетки рака поджелудочной, выращенные в лаборатории, особенно зависели от NUP93: при его снижении эти клетки росли медленнее и образовывали меньше колоний, что указывает на связь NUP93 с агрессивным поведением опухоли.
Как раковые клетки увертываются от химиотерапии
Гемцитабин действует, встраиваясь в ДНК во время её копирования, вызывая ошибки и разрывы, которые должны остановить деление опухолевых клеток. Однако клетки рака могут противодействовать этому, активируя системы репарации ДНК. Сравнивая опухоли с высоким и низким уровнем NUP93, команда обнаружила, что гены, участвующие в репарации ДНК, более активны при избытке NUP93. В клеточных экспериментах снижение NUP93 делало клетки поджелудочной гораздо более чувствительными к гемцитабину, тогда как избыток NUP93 затруднял их уничтожение. Маркеры повреждения ДНК увеличивались при потере NUP93 и уменьшались при его переизбытке, а «кометный» тест, визуализирующий фрагментацию ДНК, подтвердил, что клетки без NUP93 накапливали больше повреждений после лечения. В экспериментах на мышах опухоли без NUP93 росли медленнее и значительно лучше реагировали на гемцитабин.
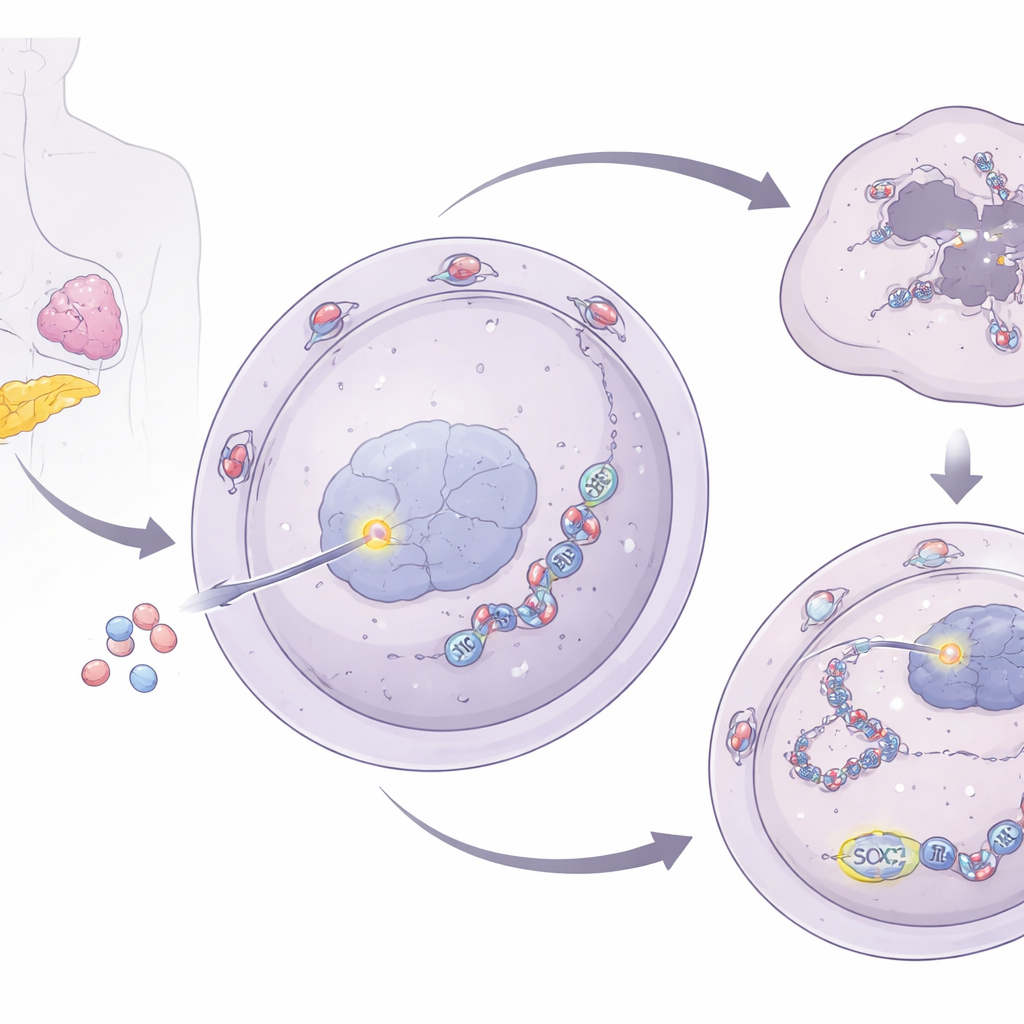
Реле от ядерной поры к стресс-гранулам
Чтобы понять, как NUP93 усиливает репарацию ДНК, исследователи изучили его связи со стресс-гранулами — временными конденсатами РНК и белков, которые помогают клеткам переживать неблагоприятные условия. Они обнаружили, что NUP93 повышает уровень G3BP1, ключевого белка стресс-гранул. При увеличении NUP93 уровень G3BP1 рос; при снижении NUP93 G3BP1 падал. Важно, что удаление G3BP1 сводило на нет способность NUP93 стимулировать рост клеток и устойчивость к гемцитабину и восстанавливало повреждение ДНК после лечения. Команда затем проследила контролирование G3BP1 до SOX2, хорошо известного транскрипционного фактора, который включает и выключает гены. NUP93 физически взаимодействует с SOX2 у ядерной поры и способствует его транспортировке в ядро. Попав внутрь, SOX2 прямо связывается с регуляторным участком гена G3BP1, повышая его экспрессию.
От защиты РНК к репарации ДНК
История не заканчивается на G3BP1. Исследователи показали, что G3BP1, в свою очередь, стабилизирует матричную РНК RAD51, центрального компонента высокоточной системы репарации ДНК — гомологичной рекомбинации. G3BP1 прямо связывается с РНК RAD51 и замедляет её распад, что приводит к повышению уровня белка RAD51. При наличии большего количества RAD51 клетки лучше справляются с восстановлением разрывов ДНК, вызванных гемцитабином. При истощении G3BP1 уровень RAD51 падал, РНК RAD51 деградировала быстрее, и повреждения ДНК накапливались. В моделях на мышах блокирование SOX2 или G3BP1 уменьшало рост опухолей и значительно усиливало эффект гемцитабина, подтверждая важность этой цепочки в живых организмах.
Новая мишень, помогающая химиотерапии
Соединив все звенья, авторы предлагают ясный путь: NUP93 у ядерной поры проводит SOX2 в ядро, SOX2 активирует G3BP1, а G3BP1 сохраняет РНК RAD51, в конечном итоге усиливая репарацию ДНК и помогая клеткам рака поджелудочной сопротивляться гемцитабину. Ось NUP93–SOX2–G3BP1–RAD51 действует как внутренняя команда спасения, ремонтирующая повреждения, которые должна вызывать химиотерапия. Нарушая один или несколько шагов этой цепочки, будущие терапии могут ослабить защиту раковых клеток и повысить эффективность существующих препаратов, что дает новую надежду на улучшение исходов при этой особенно трудно лечимой болезни.
Цитирование: Sun, H., Yang, C., Du, J. et al. NUP93 facilitates the nuclear import of SOX2 to activate G3BP1 transcription and impairs gemcitabine response in pancreatic cancer. Cell Death Dis 17, 423 (2026). https://doi.org/10.1038/s41419-026-08586-4
Ключевые слова: рак поджелудочной железы, резистентность к гемцитабину, репарация ДНК, ядерная пора, стресс-гранулы