Clear Sky Science · pt
NUP93 facilita a importação nuclear de SOX2 para ativar a transcrição de G3BP1 e reduz a resposta ao gemcitabina no câncer de pâncreas
Por que esta pesquisa importa
O câncer de pâncreas está entre os mais letais, em parte porque frequentemente resiste a medicamentos de quimioterapia como a gemcitabina. Este estudo revela uma cadeia oculta de eventos moleculares dentro das células do câncer de pâncreas que as ajuda a reparar o dano no DNA causado pela própria gemcitabina. Ao traçar essa sequência desde a fronteira celular até o núcleo genético, os autores identificam uma nova vulnerabilidade que tratamentos futuros podem explorar para tornar a quimioterapia mais eficaz.
Um porteiro no núcleo celular
Cada célula mantém seu DNA dentro de um compartimento protegido chamado núcleo, que é pontilhado por pequenas passagens conhecidas como poros nucleares. A proteína NUP93 é uma peça estrutural chave desses portões. Ao explorar grandes bancos de dados de câncer e analisar amostras de pacientes, os pesquisadores constataram que os níveis de NUP93 são significativamente maiores em adenocarcinoma ductal pancreático do que em tecido pancreático normal. Pacientes cujos tumores exibiam mais NUP93 tendiam a ter pior sobrevida. Células de câncer de pâncreas cultivadas em laboratório mostraram dependência especial de NUP93: quando seus níveis foram reduzidos, essas células cresceram mais devagar e formaram menos colônias, indicando que NUP93 está ligado a um comportamento tumoral agressivo.
Como as células cancerosas evitam a quimioterapia
A gemcitabina age ao se incorporar ao DNA enquanto ele é copiado, causando erros e quebras que deveriam interromper a divisão das células tumorais. As células cancerosas, no entanto, podem reagir ativando sistemas de reparo do DNA. Ao comparar tumores com níveis altos e baixos de NUP93, a equipe observou que genes envolvidos no reparo de DNA eram mais ativos quando NUP93 era abundante. Em experimentos celulares, reduzir NUP93 tornou as células de câncer de pâncreas muito mais sensíveis à gemcitabina, enquanto excesso de NUP93 as tornou mais difíceis de eliminar. Marcadores de dano ao DNA aumentaram quando NUP93 foi perdido e diminuíram quando ele foi superexpresso, e um ensaio de “cometa” que visualiza DNA quebrado confirmou que células sem NUP93 acumularam mais danos após o tratamento com o fármaco. Em camundongos, tumores sem NUP93 cresceram mais devagar e responderam muito melhor à gemcitabina.
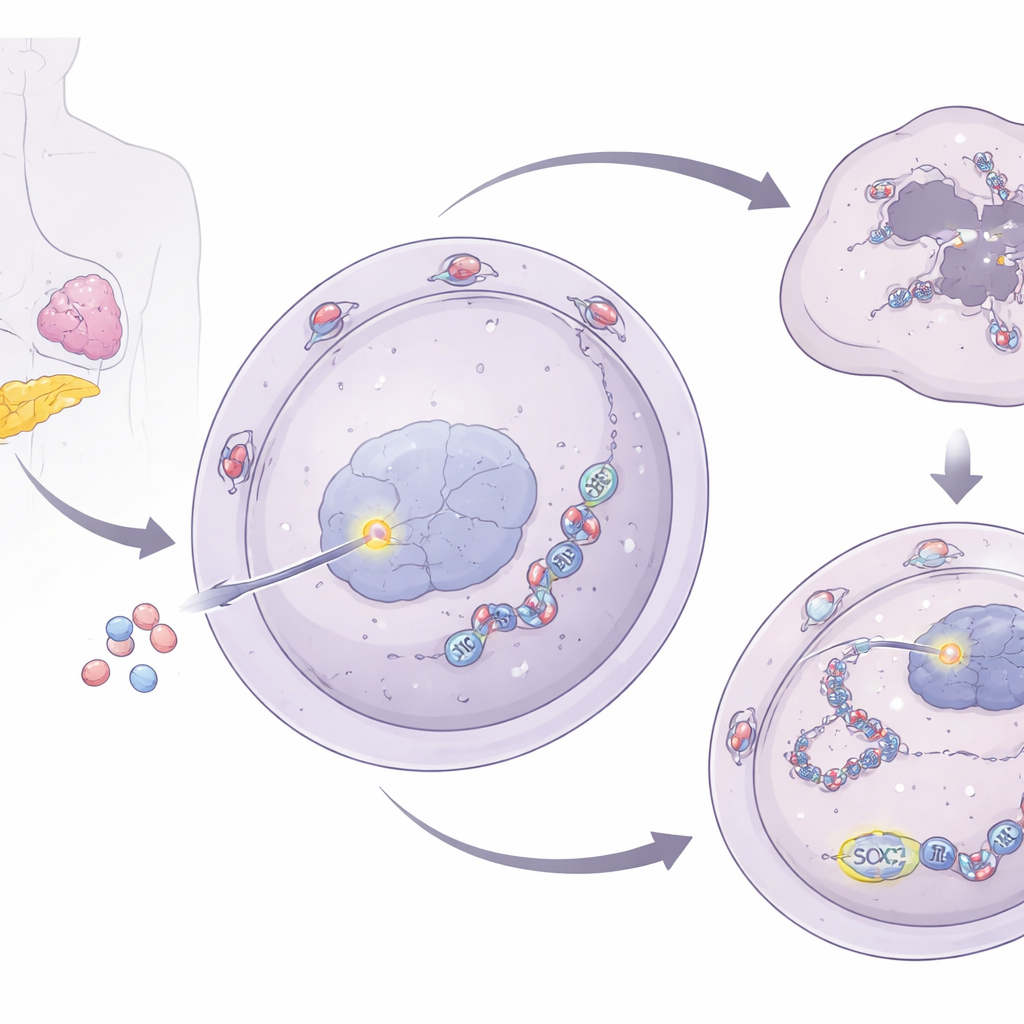
Um repasse do portão nuclear aos grânulos de estresse
Para entender como NUP93 fortalece o reparo do DNA, os pesquisadores investigaram suas conexões com os grânulos de estresse celulares—aglomerações temporárias de RNA e proteínas que ajudam as células a sobreviver a condições adversas. Eles descobriram que NUP93 aumenta os níveis de G3BP1, uma proteína central dos grânulos de estresse. Quando NUP93 foi aumentado, os níveis de G3BP1 subiram; quando NUP93 foi reduzido, G3BP1 caiu. Importante: a remoção de G3BP1 anulou a capacidade de NUP93 de promover o crescimento celular e a resistência à gemcitabina e restaurou o dano ao DNA após o tratamento. A equipe então rastreou o controle de G3BP1 até SOX2, um conhecido fator de transcrição que liga e desliga genes. NUP93 interage fisicamente com SOX2 no poro nuclear e ajuda a conduzi-lo para dentro do núcleo. Uma vez lá dentro, SOX2 se liga diretamente à região reguladora do gene G3BP1, aumentando sua expressão.
Da proteção de RNA ao reparo do DNA
A história não termina com G3BP1. Os pesquisadores mostraram que G3BP1, por sua vez, ajuda a estabilizar o RNA mensageiro de RAD51, um componente central de uma via de reparo de alta fidelidade chamada recombinação homóloga. G3BP1 se liga diretamente ao RNA de RAD51 e retarda sua degradação, levando a níveis maiores de proteína RAD51. Com mais RAD51 disponível, as células cancerosas ficam mais bem equipadas para consertar as quebras de DNA induzidas pela gemcitabina. Quando G3BP1 foi depletado, os níveis de RAD51 caíram, o RNA de RAD51 degradou-se mais rapidamente e o dano ao DNA se acumulou. Em modelos animais, bloquear SOX2 ou G3BP1 reduziu o crescimento tumoral e tornou a gemcitabina muito mais eficaz, confirmando a importância desse repasse em sistemas vivos.
Um novo alvo para ajudar a quimioterapia a funcionar
Juntando as peças, os autores propõem um caminho claro: NUP93 no poro nuclear conduz SOX2 para o núcleo, SOX2 ativa G3BP1, e G3BP1 preserva o RNA de RAD51, elevando por fim o reparo do DNA e ajudando as células do câncer de pâncreas a resistir à gemcitabina. Esse eixo NUP93–SOX2–G3BP1–RAD51 age como uma equipe de resgate interna que repara o dano que a quimioterapia deveria causar. Ao interromper uma ou mais etapas dessa cadeia, terapias futuras podem enfraquecer as defesas das células cancerosas e tornar os fármacos existentes mais potentes, oferecendo nova esperança para melhorar os desfechos nessa doença notoriamente difícil de tratar.
Citação: Sun, H., Yang, C., Du, J. et al. NUP93 facilitates the nuclear import of SOX2 to activate G3BP1 transcription and impairs gemcitabine response in pancreatic cancer. Cell Death Dis 17, 423 (2026). https://doi.org/10.1038/s41419-026-08586-4
Palavras-chave: câncer de pâncreas, resistência à gemcitabina, reparo de DNA, poros nucleares, granulos de estresse