Clear Sky Science · he
NUP93 מקל על היבוא הגרעיני של SOX2 להפעיל שעתוק של G3BP1 ופוגע בתגובה לגמציטאבין בסרטן הלבלב
מדוע מחקר זה חשוב
סרטן הלבלב הוא אחד הסרטנים הקטלניים ביותר, בין השאר כי לעתים קרובות הוא עמיד בפני תרופות כימותרפיות כגון גמציטאבין. במחקר זה חושפת שרשרת אירועים מולקולריים בתוך תאי סרטן הלבלב שעוזרת להם לתקן את נזק ה‑DNA שמטרת הגמציטאבין לגרום. במעקב אחר שרשרת זו מהגבול התאי אל ליבת הגנום, המחברים מגלים נקודת תורפה חדשה שייתכן שטיפולים עתידיים יוכלו לנצל כדי להפוך את הכימותרפיה ליעילה יותר.
שומרי סף על גבי הגרעין
כל תא שומר את ה‑DNA שלו בתוך מחיצת מגן שנקראת גרעין, שבו יש שערים קטנים הידועים כנקבים גרעיניים. חלבון NUP93 מהווה מרכיב מבני חשוב של השערים האלה. באמצעות כרייה של מאגרי נתונים גדולים על סרטן ובחינת דגימות של מטופלים, החוקרים מצאו שרמות NUP93 גבוהות באופן משמעותי בקרצינומה דוקטלית של הלבלב לעומת רקמה לבלבית נורמלית. מטופלים שבהם הגידולים הביטו יותר NUP93 נטו להישרדות גרועה יותר. תאי סרטן לבלב שעובדו במעבדה היו תלויים במיוחד ב‑NUP93: כאשר רמותיו ירדו, תאים אלה גדלו לאט יותר ויצרו פחות ארמונות — עדות לכך ש‑NUP93 קשור להתנהגות טומורלית אגרסיבית.
כיצד תאי סרטן מתחמקים מכימותרפיה
גמציטאבין פועל על ידי החדרה אל תוך ה‑DNA בזמן שכפולו, וגורם לשגיאות ושברים שמטרתם לעצור חלוקת תאים סרטניים. עם זאת, תאי סרטן יכולים להלחם בכך על ידי הפעלת מערכות תיקון DNA. בהשוואת גידולים עם רמות גבוהות ונמוכות של NUP93, הצוות ראה שגנים המעורבים בתיקון DNA פעילים יותר כאשר NUP93 שופע. בניסויים תאיים, דיכוי NUP93 הפך את תאי סרטן הלבלב לפגיעים בהרבה לגמציטאבין, בעוד שעודף NUP93 עשה אותם קשים יותר להריגה. סימני נזק ל‑DNA עלו כאשר NUP93 הוסר וירדו כאשר הוא הופרש בכמות גבוהה, ובבדיקת "קומטה" שמדגימה DNA שבור אושר שתאים חסרי NUP93 צברו יותר נזק לאחר הטיפול. בעכברים, גידולים חסרי NUP93 גדלו לאט יותר והגיבו הרבה יותר טוב לגמציטאבין.
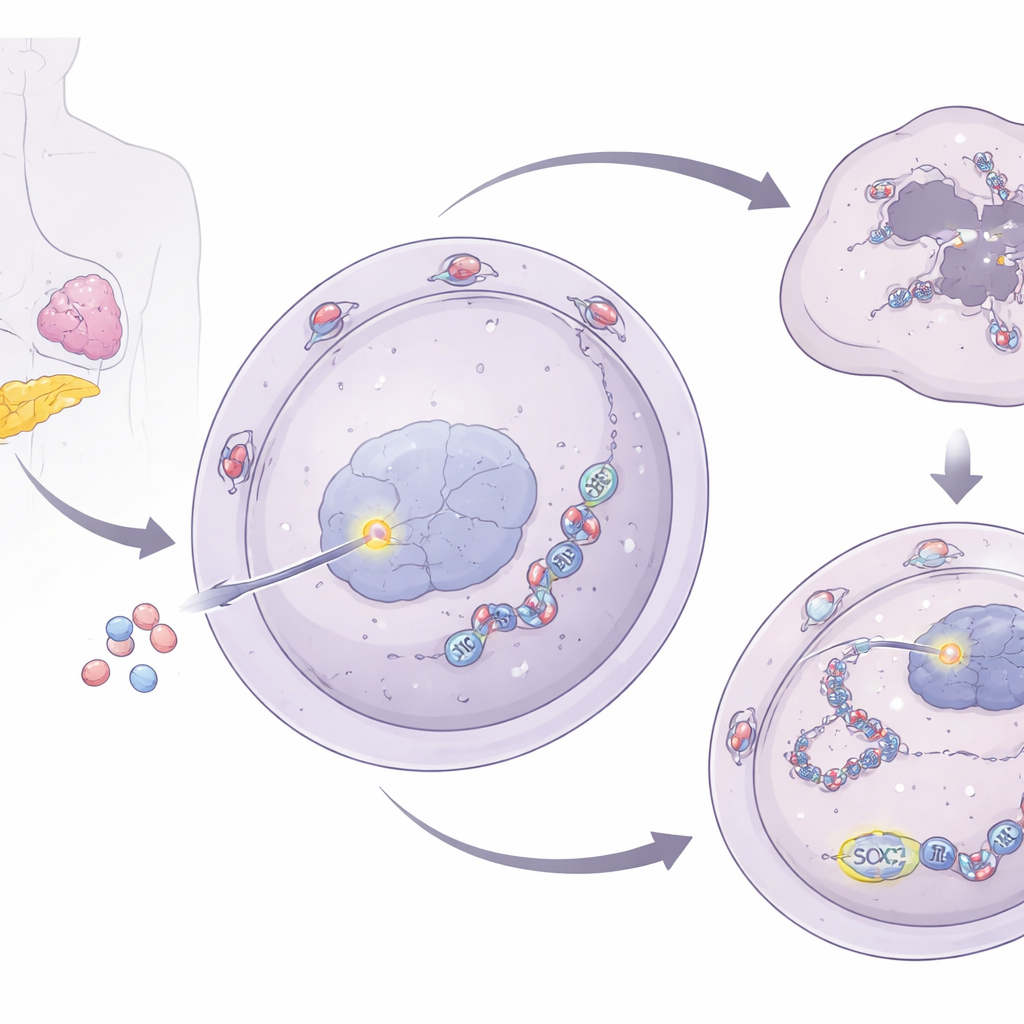
רצף אותות משער הגרעין אל גרעיני־המתח
כדי להבין כיצד NUP93 מחזק תיקון DNA, החוקרים בחנו את הקשר שלו לגרעיני מתחים — צברי RNA וחלבונים זמניים שעוזרים לתאים לשרוד תנאים קשים. הם גילו ש‑NUP93 מעלה את רמות G3BP1, חלבון מרכזי בגרעיני המתחים. כאשר NUP93 הוגבר, רמות G3BP1 עלו; כאשר NUP93 הוסרו, G3BP1 ירד. חשוב מכך, הסרת G3BP1 ביטלה את יכולתו של NUP93 לקדם גדילה של תאים ולעודד עמידות לגמציטאבין והשיבה את רמות נזק ה‑DNA לאחר הטיפול. הצוות עקב אחר בקרת G3BP1 בחזרה אל SOX2, פקטור שעתוק ידוע שמפעיל וכיבוי גנים. NUP93 יוצר אינטראקציה פיזית עם SOX2 בנקב הגרעיני ומסייע להוביל אותו לתוך הגרעין. כשהוא בפנים, SOX2 נקשר ישירות לאזור הבקרה של גן G3BP1 ומעלה את ביטויו.
מהגנה על RNA לתיקון DNA
הסיפור לא נגמר ב‑G3BP1. החוקרים הראו כי G3BP1 מסייע לייצוב mRNA של RAD51, שחקן מרכזי במסלול תיקון DNA מדויק הנקרא רקומבינציית הומולוגיה. G3BP1 נקשר ישירות ל‑RNA של RAD51 ומאט את קידת הידרדרותו, מה שמוביל לרמות חלבון RAD51 גבוהות יותר. עם עודף RAD51, תאי הסרטן מצוידים טוב יותר לתקן שברי DNA הנגרמים על ידי גמציטאבין. כאשר G3BP1 דוכא, רמות RAD51 ירדו, RNA של RAD51 התמוטט מהר יותר ונזק ל‑DNA הצטבר. במודלים של עכברים, חסימת SOX2 או G3BP1 צמצמה את גדילת הגידול ועשתה את הגמציטאבין ליעיל הרבה יותר, מה שאשר את חשיבותו של הרצף במערכות חיות.
יעד חדש לשיפור יעילות הכימותרפיה
בהרכבת החלקים, המחברים מציעים מסלול ברור: NUP93 בנקב הגרעיני מלווה את SOX2 לתוך הגרעין, SOX2 מפעיל את G3BP1, ו‑G3BP1 משמר את ה‑RAD51 RNA, מה שמגביר בסופו של דבר את תיקון ה‑DNA ועוזר לתאי סרטן הלבלב לעמוד בעמידות לגמציטאבין. ציר NUP93–SOX2–G3BP1–RAD51 פועל כמו צוות חילוץ פנימי שמתקן את הנזק שהכימותרפיה אמורה לגרום. על ידי פגיעה בשלב אחד או יותר בשרשרת הזו, טיפולים עתידיים עשויים להחליש את ההגנות של התאים הסרטניים ולהגביר את עוצמתן של התרופות הקיימות, ולהציע תקווה חדשה לשיפור התוצאות במחלה שמאופיינת בקושי רב לטיפול.
ציטוט: Sun, H., Yang, C., Du, J. et al. NUP93 facilitates the nuclear import of SOX2 to activate G3BP1 transcription and impairs gemcitabine response in pancreatic cancer. Cell Death Dis 17, 423 (2026). https://doi.org/10.1038/s41419-026-08586-4
מילות מפתח: סרטן הלבלב, עמידות לגמציטאבין, תיקון DNA, נקב גרעיני, גרעיני מתחים