Clear Sky Science · es
NUP93 facilita la importación nuclear de SOX2 para activar la transcripción de G3BP1 y reduce la respuesta a gemcitabina en el cáncer de páncreas
Por qué importa esta investigación
El cáncer de páncreas es uno de los más letales, en parte porque a menudo evade fármacos de quimioterapia como la gemcitabina. Este estudio descubre una cadena oculta de eventos moleculares dentro de las células de cáncer de páncreas que les ayuda a reparar el daño en el ADN que precisamente pretende causar la gemcitabina. Al rastrear esta cadena desde el límite celular hasta su núcleo genético, los autores revelan un nuevo punto débil que tratamientos futuros podrían explotar para mejorar la eficacia de la quimioterapia.
Un guardián en el núcleo celular
Cada célula mantiene su ADN dentro de un compartimento protegido llamado núcleo, que está salpicado de pequeñas puertas conocidas como poros nucleares. La proteína NUP93 es una parte estructural clave de esas puertas. Mediante el análisis de grandes conjuntos de datos oncológicos y el examen de muestras de pacientes, los investigadores hallaron que los niveles de NUP93 son significativamente más altos en el adenocarcinoma ductal pancreático que en el tejido pancreático normal. Los pacientes cuyos tumores tenían más NUP93 tendían a tener peor supervivencia. Las células de cáncer de páncreas cultivadas en laboratorio eran especialmente dependientes de NUP93: cuando se redujeron sus niveles, estas células crecieron más despacio y formaron menos colonias, lo que indica que NUP93 está ligado a un comportamiento tumoral más agresivo.
Cómo las células cancerosas eluden la quimioterapia
La gemcitabina actúa insertándose en el ADN durante su replicación, provocando errores y roturas que deberían detener la división de las células tumorales. Sin embargo, las células cancerosas pueden contraatacar activando sistemas de reparación del ADN. Al comparar tumores con niveles altos y bajos de NUP93, el equipo observó que los genes implicados en la reparación del ADN estaban más activos cuando NUP93 era abundante. En experimentos celulares, silenciar NUP93 hizo que las células de cáncer de páncreas fueran mucho más sensibles a la gemcitabina, mientras que un exceso de NUP93 las hacía más difíciles de eliminar. Los marcadores de daño en el ADN aumentaron cuando se perdió NUP93 y disminuyeron cuando se sobreexpresó; un ensayo de “cometa” que visualiza ADN roto confirmó que las células sin NUP93 acumulaban más daño tras el tratamiento. En ratones, los tumores carentes de NUP93 crecieron más despacio y respondieron mucho mejor a la gemcitabina.
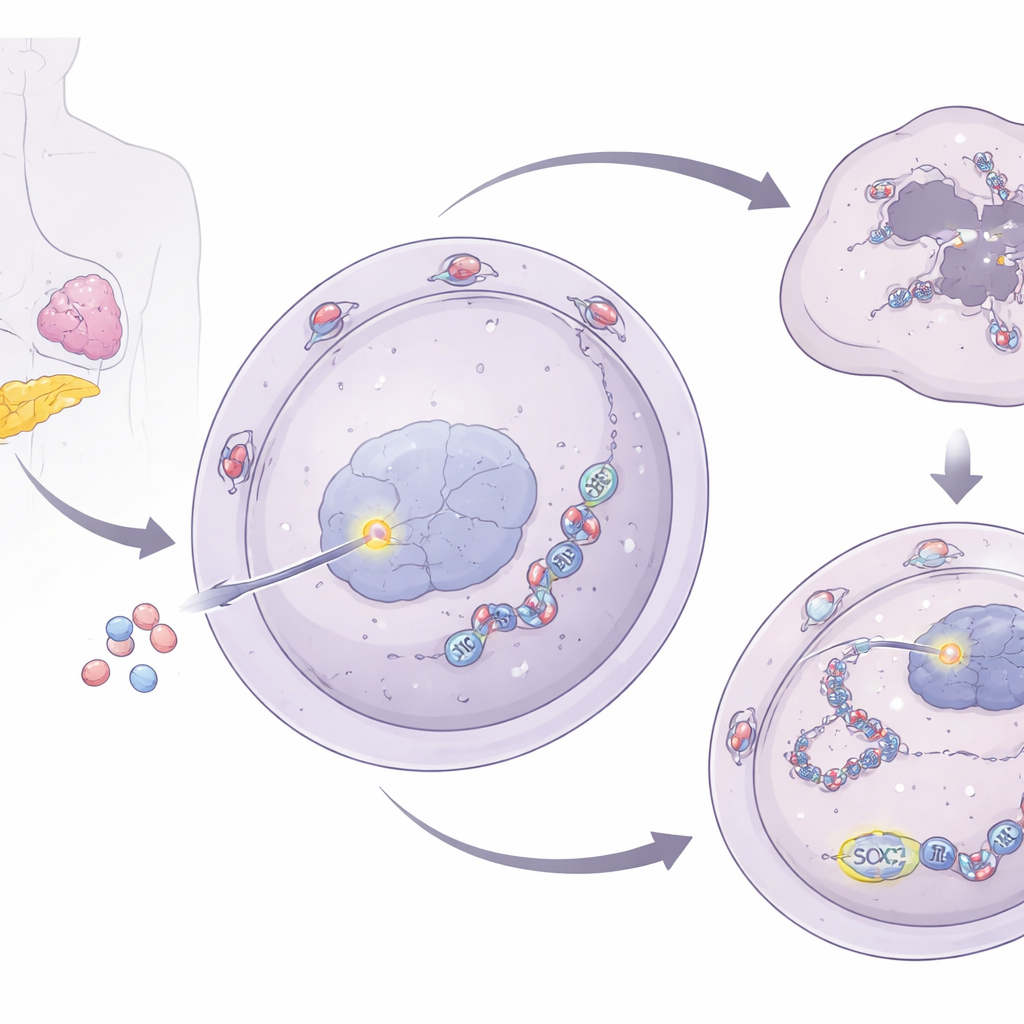
Un relevo desde la puerta nuclear hasta los gránulos de estrés
Para entender cómo NUP93 fortalece la reparación del ADN, los investigadores examinaron sus vínculos con los gránulos de estrés celulares: conjuntos temporales de ARN y proteínas que ayudan a las células a sobrevivir condiciones adversas. Descubrieron que NUP93 aumenta los niveles de G3BP1, una proteína central de los gránulos de estrés. Cuando NUP93 se incrementó, los niveles de G3BP1 subieron; cuando NUP93 se redujo, G3BP1 bajó. De manera importante, eliminar G3BP1 anuló la capacidad de NUP93 para promover el crecimiento celular y la resistencia a la gemcitabina y restituyó el daño en el ADN tras el tratamiento. El equipo rastreó el control de G3BP1 hasta SOX2, un factor de transcripción bien conocido que activa y desactiva genes. NUP93 interactúa físicamente con SOX2 en el poro nuclear y facilita su transporte al núcleo. Una vez dentro, SOX2 se une directamente a la región reguladora del gen G3BP1, aumentando su expresión.
De la protección del ARN a la reparación del ADN
La historia no termina con G3BP1. Los investigadores demostraron que G3BP1, a su vez, ayuda a estabilizar el ARN mensajero de RAD51, un actor central en una vía de reparación del ADN de alta fidelidad llamada recombinación homóloga. G3BP1 se une directamente al ARN de RAD51 y ralentiza su degradación, lo que conduce a niveles más elevados de la proteína RAD51. Con más RAD51 disponible, las células cancerosas están mejor equipadas para reparar las roturas de ADN inducidas por gemcitabina. Cuando se eliminó G3BP1, los niveles de RAD51 disminuyeron, el ARN de RAD51 se degradó más rápidamente y el daño en el ADN se acumuló. En modelos murinos, bloquear SOX2 o G3BP1 redujo el crecimiento tumoral e incrementó notablemente la eficacia de la gemcitabina, confirmando la importancia de este relevo en sistemas vivos.
Un nuevo objetivo para ayudar a que funcione la quimioterapia
Al reunir las piezas, los autores proponen una vía clara: NUP93 en el poro nuclear conduce a SOX2 al núcleo, SOX2 activa G3BP1 y G3BP1 preserva el ARN de RAD51, lo que en última instancia potencia la reparación del ADN y ayuda a las células de cáncer de páncreas a resistir la gemcitabina. Este eje NUP93–SOX2–G3BP1–RAD51 actúa como un equipo de rescate interno que repara el daño que la quimioterapia debería infligir. Al interrumpir uno o varios pasos de esta cadena, terapias futuras podrían debilitar las defensas de las células cancerosas y aumentar la potencia de los fármacos existentes, ofreciendo una nueva esperanza para mejorar los resultados en esta enfermedad notoriamente difícil de tratar.
Cita: Sun, H., Yang, C., Du, J. et al. NUP93 facilitates the nuclear import of SOX2 to activate G3BP1 transcription and impairs gemcitabine response in pancreatic cancer. Cell Death Dis 17, 423 (2026). https://doi.org/10.1038/s41419-026-08586-4
Palabras clave: cáncer de páncreas, resistencia a gemcitabina, reparación del ADN, poro nuclear, gránulos de estrés