Clear Sky Science · zh
HIF-1α通过调控线粒体动力学和指状突形成抑制SNPH表达以促进结直肠癌肝转移
这项研究为何重要
结直肠癌常见,约半数患者最终会在肝脏出现肿瘤,治疗困难且常致命。本研究深入探讨了癌细胞内的“微型发电站”——线粒体,试图弄清其行为改变如何帮助癌细胞从肠道脱离、在体内迁徙并在肝脏定植。通过揭示一个将缺氧、能量装置与细胞运动联系起来的隐性调控系统,这项工作指向了减缓或阻断结直肠癌扩散的新策略。
一个细胞内的“交通警察”消失了
研究人员聚焦于一种名为syntaphilin (SNPH) 的蛋白,它像线粒体的交通警察,帮助将线粒体固定并维持其融合状态。通过挖掘大型公共基因数据库并分析患者样本,发现SNPH在邻近健康组织中含量较高,在原发性结直肠肿瘤中下降,而在肝转移灶中最低。肿瘤中SNPH含量低的患者生存情况更差。在细胞系和小鼠模型中,提升SNPH可减少肝脏肿瘤的数量和体积,而低SNPH则与更具侵袭性的扩散相关。这些模式表明,失去这一线粒体“锚定器”是使癌细胞更易移动和更具危险性的关键步骤。
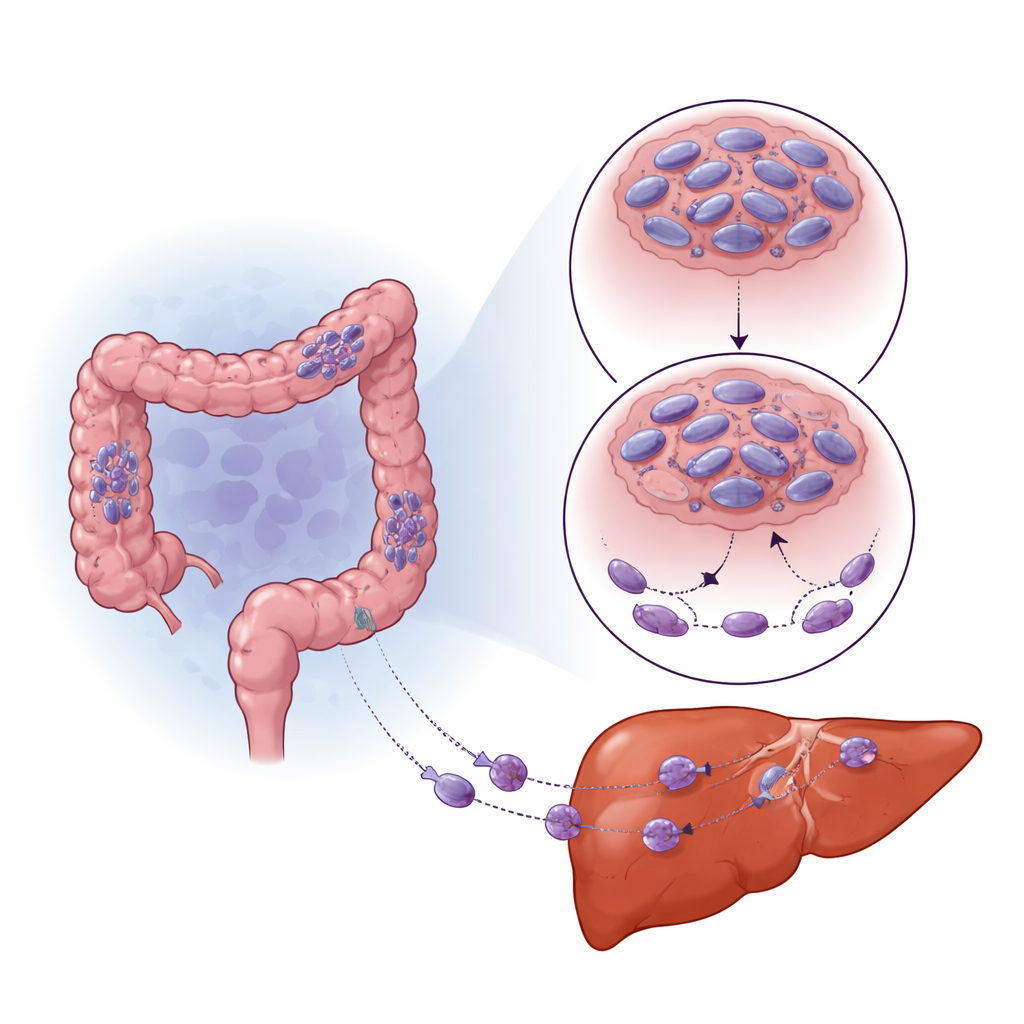
缺氧如何重塑肿瘤行为
实体瘤常常超过其血供,产生低氧(缺氧)区域。细胞通过一个主开关蛋白HIF-1α感知并适应这一环境。研究组注意到,结直肠肿瘤和肝转移灶中HIF-1α较高的区域,SNPH特别偏低。当他们在体外将癌细胞置于低氧环境时,SNPH水平随时间显著下降,细胞变得更具迁移性和侵袭性。抑制HIF-1α可部分恢复SNPH水平并减少这种运动性增加。HIF-1α并非直接关闭SNPH,而是上调了一种小型调控RNA miR-130a-3p,后者结合SNPH的信使RNA并阻止其表达。抑制miR-130a-3p保护了SNPH,抑制了细胞“指状突”的生长并减少了侵袭,即便在低氧条件下亦然。
从“发电站”到“抓钩”
SNPH的缺失不仅仅让线粒体更自由地移动。在正常情况下,线粒体多呈延长并聚集状态,但当SNPH减少时,线粒体碎裂并漂移到细胞边缘。此重排提高了活性氧(ROS)的产生,ROS是代谢的化学反应性副产物。这些ROS激活了以AKT和cdc42为中心的信号链,进而激活下游的PAK1和Cofilin。综合效应是细胞内骨架(肌动蛋白结构)的重塑,促进形成长而细的指状突(filopodia)。这些结构像抓钩一样,帮助细胞向前拉动并挤过周围组织。用ROS清除剂处理细胞可抑制该信号通路并减少指状突,而添加ROS模拟物则会增加指状突,除非同时恢复SNPH。
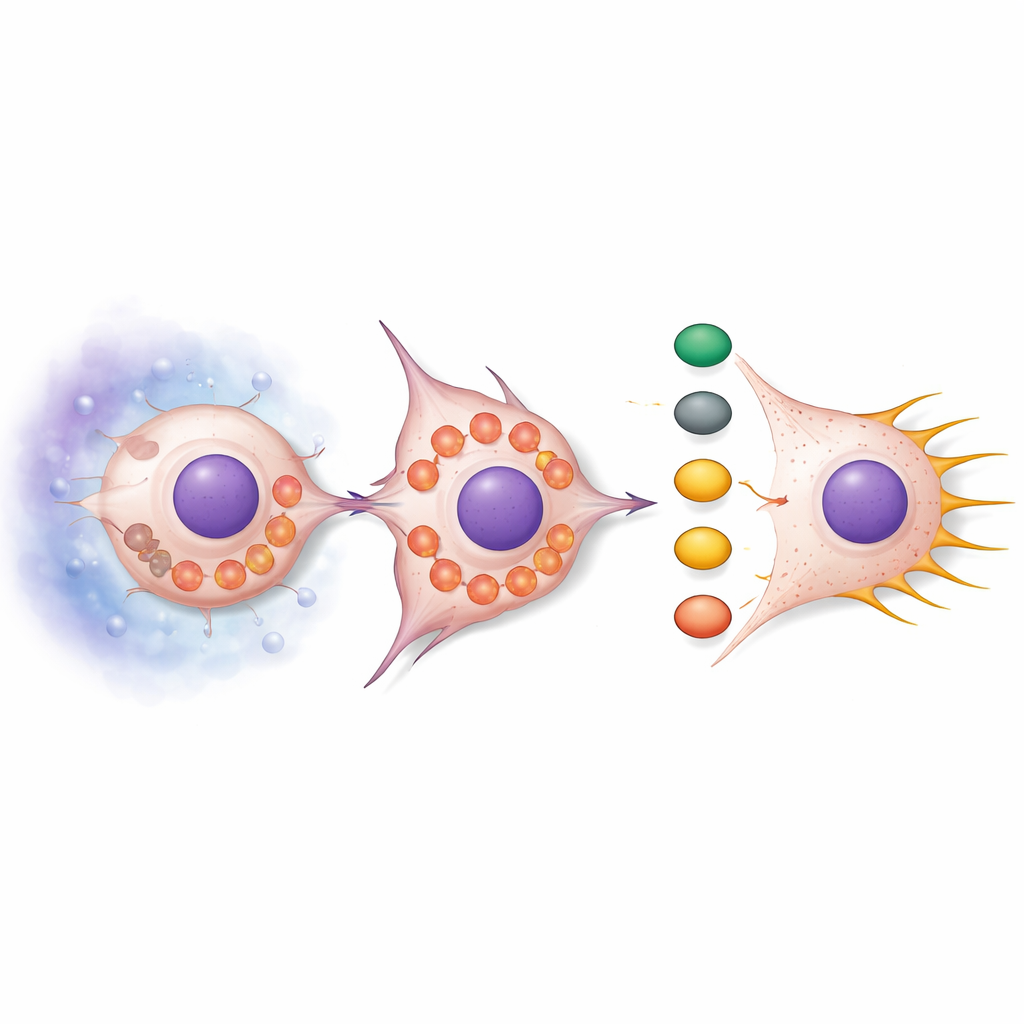
在活体动物中检验该机制
为验证这一通路是否确实影响肝脏扩散,研究人员将含或不含额外SNPH的结直肠癌细胞注入小鼠。接受SNPH富集细胞的动物产生的肝脏肿瘤显著更少且更小,尽管癌细胞的总体生长速度相似。对肝转移灶的显微观察显示,过表达SNPH的肿瘤线粒体更长、更融合,HIF-1α水平更低,PAK1/Cofilin信号轴的激活也更弱。换言之,恢复这一线粒体“锚定器”既改变了线粒体的形态,也将化学信号网络转回到较不易迁移的状态,从而使癌细胞更难在肝脏定殖。
对患者意味着什么
简而言之,这项研究揭示了一条连锁反应:肿瘤低氧激活HIF-1α,HIF-1α上调miR-130a-3p,后者沉默SNPH。失去SNPH后,线粒体碎裂并移向细胞边缘,产生更多ROS,进而开启促进移动的信号通路。该通路随后将细胞表面改造成有助于结直肠癌细胞迁移并在肝脏播种的指状突。针对该链条的任一环节——HIF-1α、miR-130a-3p、ROS产生或下游信号步骤——都有可能成为预防或限制肝转移的新策略,且SNPH本身可能作为评估患者癌症扩散风险的有用标志物。
引用: Zhan, L., Li, X., Li, X. et al. HIF-1α suppresses SNPH expression to facilitate liver metastasis of colorectal cancer through regulating mitochondrial dynamics and filopodia formation. Cell Death Dis 17, 380 (2026). https://doi.org/10.1038/s41419-026-08551-1
关键词: 结直肠癌转移, 线粒体动力学, 缺氧 HIF-1α, microRNA-130a-3p, 活性氧