Clear Sky Science · sv
HIF-1α undertrycker SNPH‑uttryck för att underlätta levermetastasering av kolorektal cancer genom att reglera mitokondriernas dynamik och filopodiebildning
Varför denna forskning är viktig
Kolorektal cancer är vanligt, och omkring hälften av patienterna utvecklar så småningom tumörer i levern, vilka är svåra att behandla och ofta livshotande. Denna studie gräver i de små kraftverken inne i cancercellerna — mitokondrierna — för att förstå hur förändringar i deras beteende hjälper cancerceller att lossna från tarmen, färdas genom kroppen och slå sig ner i levern. Genom att avslöja ett dolt kontrollsystem som kopplar samman lågt syre, energimaskineri och cellrörelse, pekar arbetet ut nya vägar för att bromsa eller blockera spridningen av kolorektal cancer.
En cellens trafikpolis försvinner
Forskarna fokuserade på ett protein som kallas syntaphilin (SNPH), som fungerar som en trafikpolis för mitokondrierna och hjälper till att hålla dem förankrade och sammanfogade. Genom att gräva i stora offentliga genbanker och analysera patientprover fann de att SNPH‑nivåerna är högre i närliggande frisk vävnad, lägre i primära kolorektala tumörer och lägst i levermetastaser. Patienter vars tumörer hade lite SNPH tenderade att få sämre överlevnad. I både cellinjer och musmodeller minskade en ökning av SNPH antalet och storleken på levertumörer, medan låg SNPH var kopplat till mer aggressiv spridning. Dessa mönster tyder på att förlusten av denna mitokondriella ”ankare” är ett nyckelsteg för att göra cancerceller mer rörliga och farliga.
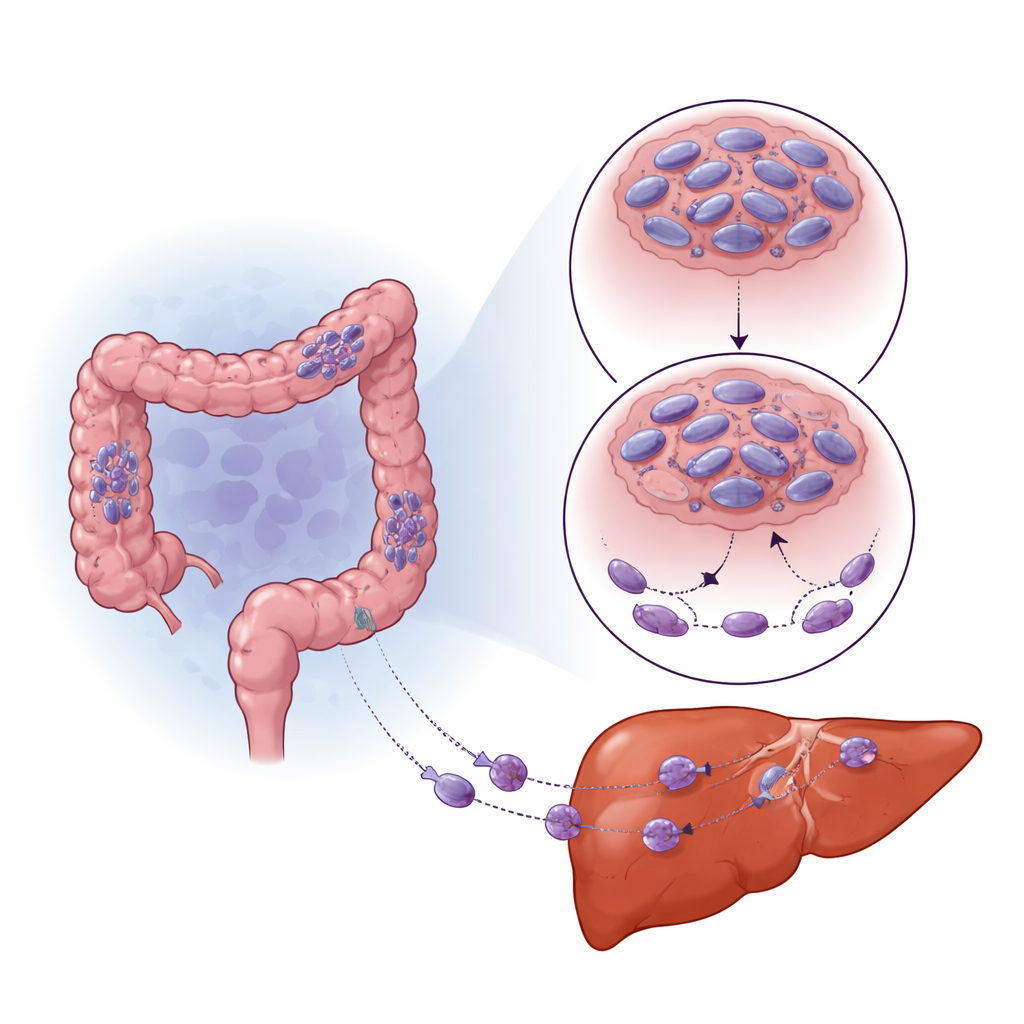
Hur lågt syre omprogrammerar tumörceller
Solida tumörer växer ofta snabbare än sin blodförsörjning, vilket skapar områden med lågt syre (hypoxi). Celler känner av detta via en huvudströmbrytare, proteinet HIF-1α, som hjälper dem att anpassa sig och överleva. Teamet noterade att områden i kolorektala tumörer och levermetastaser med hög HIF-1α hade särskilt låg SNPH. När de odlade cancerceller under låga syreförhållanden i labbet sjönk SNPH‑nivåerna kraftigt över tid och cellerna blev mer rörliga och invasiva. Att blockera HIF-1α återställde delvis SNPH‑nivåerna och minskade denna ökade rörlighet. Istället för att stänga av SNPH direkt ökade HIF-1α ett litet reglerande RNA, miR-130a-3p, som sedan band till SNPH:s budbärare och förhindrade att det producerades. Att hämma miR-130a-3p skyddade SNPH, begränsade tillväxten av tunna cell"fingrar" och minskade invasion även vid lågt syre.
Från kraftverk till "gripkrokar"
Förlust av SNPH gjorde mer än att bara frigöra mitokondrier att röra sig. Under normala förhållanden tenderar mitokondrier att vara förlängda och klustrade, men när SNPH minskade blev de fragmenterade och drev ut mot cellens yttre kant. Denna omplacering ökade produktionen av reaktiva syreföreningar (ROS), kemiskt reaktiva biprodukter av metabolismen. Dessa ROS slog på en signalväg centrerad kring proteinerna AKT och cdc42, vilka i sin tur aktiverade nedströmsaktörer PAK1 och Cofilin. Den samlade effekten var en ombyggnad av aktin-skelettet — cellens inre stomme — som främjade långa, tunna utskott kallade filopodier. Dessa strukturer fungerar som gripkrokar och hjälper celler att dra sig framåt och pressa sig igenom omgivande vävnad. Behandling med ROS‑upptagare dämpade denna signalering och minskade filopodier, medan tillsats av ROS‑mimikrar ökade antalet filopodier om inte SNPH återställdes.
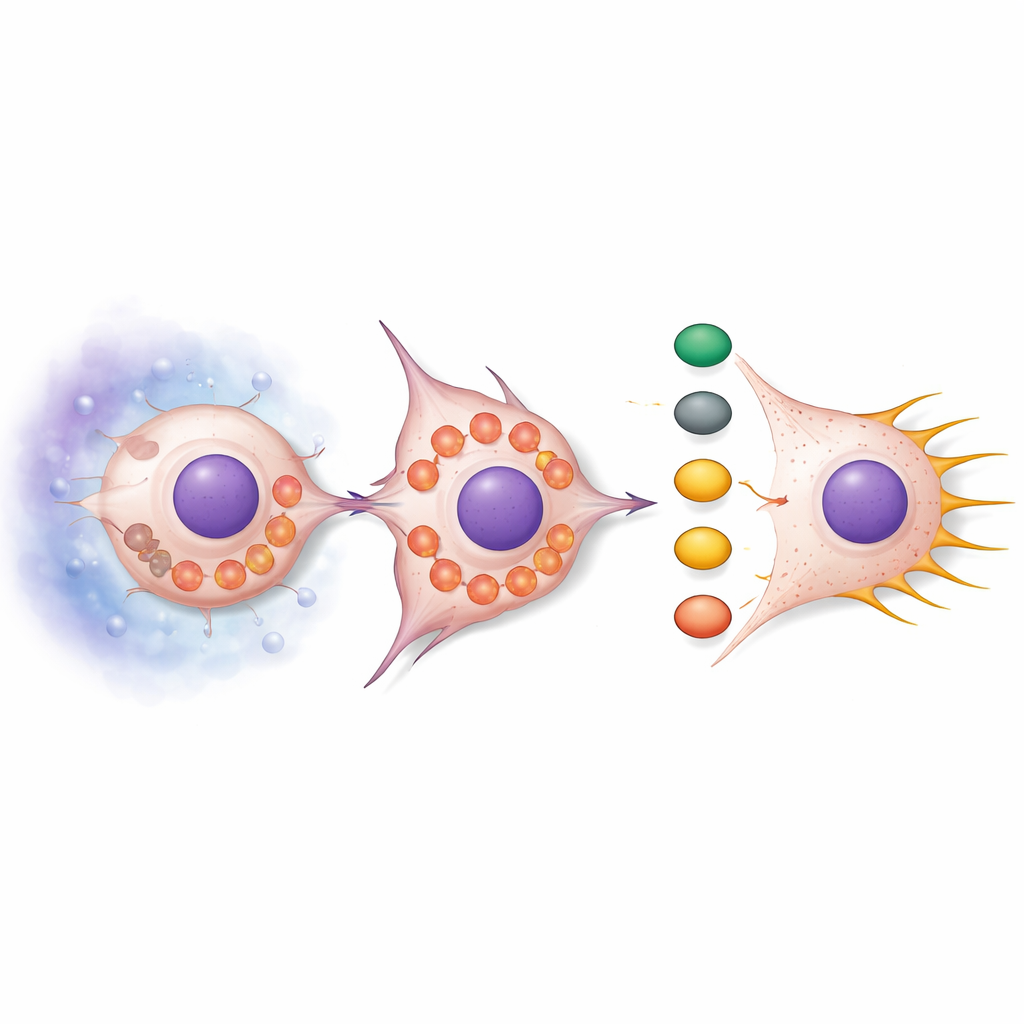
Test av mekanismen i levande djur
För att se om denna bana verkligen påverkar spridning till levern injicerade forskarna kolorektala cancerceller med eller utan extra SNPH i möss. Djur som fick SNPH‑rika celler utvecklade betydligt färre och mindre levertumörer, även om den övergripande tillväxthastigheten för cancercellerna var liknande. Mikroskopi av levermetastaser visade att tumörer som överuttryckte SNPH hade längre, mer sammansmälta mitokondrier, lägre nivåer av HIF-1α och svagare aktivering av PAK1/Cofilin‑grenen i signaleringen. Med andra ord, att återställa det mitokondriella "ankaret" försköt både mitokondriernas form och det kemiska signalnätverket mot ett mindre rörligt tillstånd, vilket gjorde det svårare för cancerceller att kolonisera levern.
Vad det betyder för patienter
Enkelt uttryckt avslöjar denna studie en kedjereaktion: lågt syre i tumörer aktiverar HIF-1α, som slår på miR-130a-3p, vilket i sin tur tystar SNPH. Utan SNPH fragmenteras mitokondrierna och rör sig mot cellekanten, vilket genererar mer ROS som aktiverar en rörelsefrämjande signalväg. Det omformar i sin tur cellens yta till filopodier som hjälper kolorektala cancerceller att migrera och så småningom etablera sig i levern. Att rikta in sig på någon del av denna kedja — HIF-1α, miR-130a-3p, ROS‑produktion eller de nedströms signalstegen — kan ge nya strategier för att förebygga eller begränsa levermetastasering, och SNPH i sig kan tjäna som en användbar markör för hur benägen en patients cancer är att sprida sig.
Citering: Zhan, L., Li, X., Li, X. et al. HIF-1α suppresses SNPH expression to facilitate liver metastasis of colorectal cancer through regulating mitochondrial dynamics and filopodia formation. Cell Death Dis 17, 380 (2026). https://doi.org/10.1038/s41419-026-08551-1
Nyckelord: metastasering av kolorektal cancer, mitokondriernas dynamik, hypoxi HIF-1α, mikroRNA-130a-3p, reaktiva syreföreningar