Clear Sky Science · pt
HIF-1α suprime a expressão de SNPH para facilitar a metástase hepática do câncer colorretal ao regular a dinâmica mitocondrial e a formação de filopódios
Por que esta pesquisa importa
O câncer colorretal é comum, e cerca de metade dos pacientes desenvolve eventualmente tumores no fígado, que são difíceis de tratar e frequentemente letais. Este estudo investiga as pequenas usinas de energia dentro das células cancerosas — as mitocôndrias — para entender como alterações em seu comportamento ajudam as células tumorais a se desprenderem do intestino, viajar pelo corpo e se estabelecerem no fígado. Ao desvendar um sistema de controle que conecta baixa oxigenação, a maquinaria energética e o movimento celular, o trabalho aponta caminhos novos para retardar ou bloquear a disseminação do câncer colorretal.
Um agente de controle celular desaparece
Os pesquisadores se concentraram em uma proteína chamada sintafnilina (SNPH), que atua como um agente de controle para as mitocôndrias, ajudando a mantê‑las ancoradas e fundidas. Ao explorar grandes bancos públicos de genes e analisar amostras de pacientes, eles descobriram que os níveis de SNPH são maiores no tecido saudável adjacente, menores nos tumores colorretais primários e mais baixos ainda nas metástases hepáticas. Pacientes cujos tumores apresentavam pouco SNPH tendiam a ter pior sobrevida. Em linhas celulares e em modelos murinos, aumentar SNPH reduziu o número e o tamanho dos tumores no fígado, enquanto níveis baixos de SNPH se associaram a uma disseminação mais agressiva. Esses padrões sugerem que a perda desse “âncora” mitocondrial é um passo chave para tornar as células cancerosas mais móveis e perigosas.
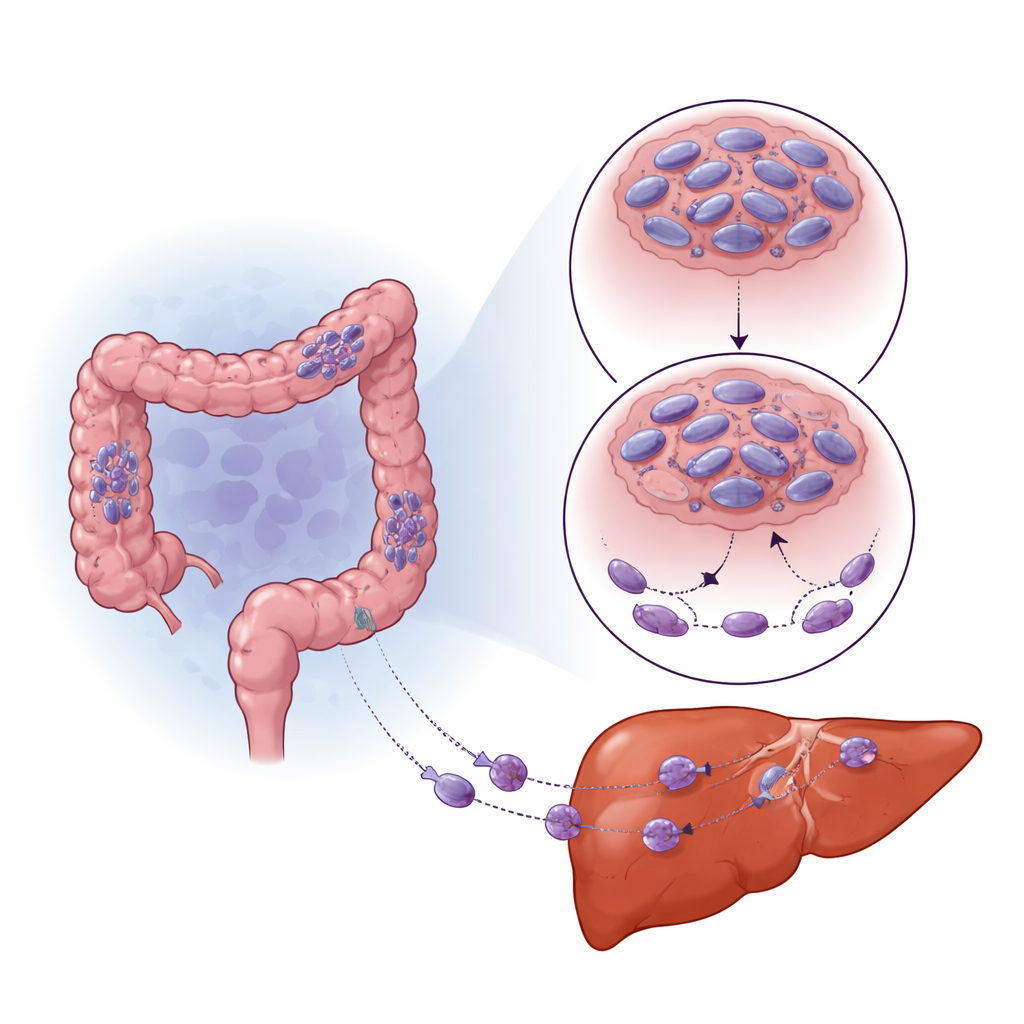
Como a baixa oxigenação reprograma o comportamento tumoral
Tumores sólidos frequentemente crescem além de seu suprimento sanguíneo, criando áreas de baixo oxigênio (hipóxia). As células percebem isso por meio de uma proteína chave chamada HIF-1α, que as ajuda a se adaptar e sobreviver. A equipe notou que regiões de tumores colorretais e metástases hepáticas com alto HIF-1α tinham SNPH especialmente baixo. Quando cultivaram células tumorais sob condições de baixa oxigenação no laboratório, os níveis de SNPH caíram acentuadamente com o tempo, e as células tornaram‑se mais móveis e invasivas. Bloquear HIF-1α resgatou em parte os níveis de SNPH e reduziu esse aumento de mobilidade. Em vez de desligar diretamente SNPH, HIF-1α elevou um pequeno RNA regulador, miR-130a-3p, que então se ligou à mensagem de SNPH e impediu sua tradução. Inibir miR-130a-3p protegeu SNPH, conteve o crescimento de “dedos” finos celulares e reduziu a invasão, mesmo em baixa oxigenação.
Das usinas de energia aos “ganchos de agarrar”
A perda de SNPH fez mais do que apenas liberar as mitocôndrias para se moverem. Em condições normais, as mitocôndrias tendem a ser alongadas e agrupadas, mas quando SNPH foi reduzida, elas se fragmentaram e migraram para a periferia da célula. Esse rearranjo aumentou a produção de espécies reativas de oxigênio (ROS), subprodutos quimicamente reativos do metabolismo. Essas ROS ativaram uma cascata de sinalização centrada nas proteínas AKT e cdc42, que por sua vez ativaram parceiros downstream PAK1 e Cofilina. O efeito combinado foi a remodelação do citoesqueleto de actina — o andaime interno da célula — promovendo protrusões longas e finas chamadas filopódios. Essas estruturas funcionam como ganchos de agarrar, ajudando as células a se puxarem para frente e a se espremerem pelo tecido circundante. Tratar as células com quelantes de ROS atenuou essa sinalização e reduziu os filopódios, enquanto adicionar miméticos de ROS aumentou os filopódios, salvo quando SNPH foi restaurada.
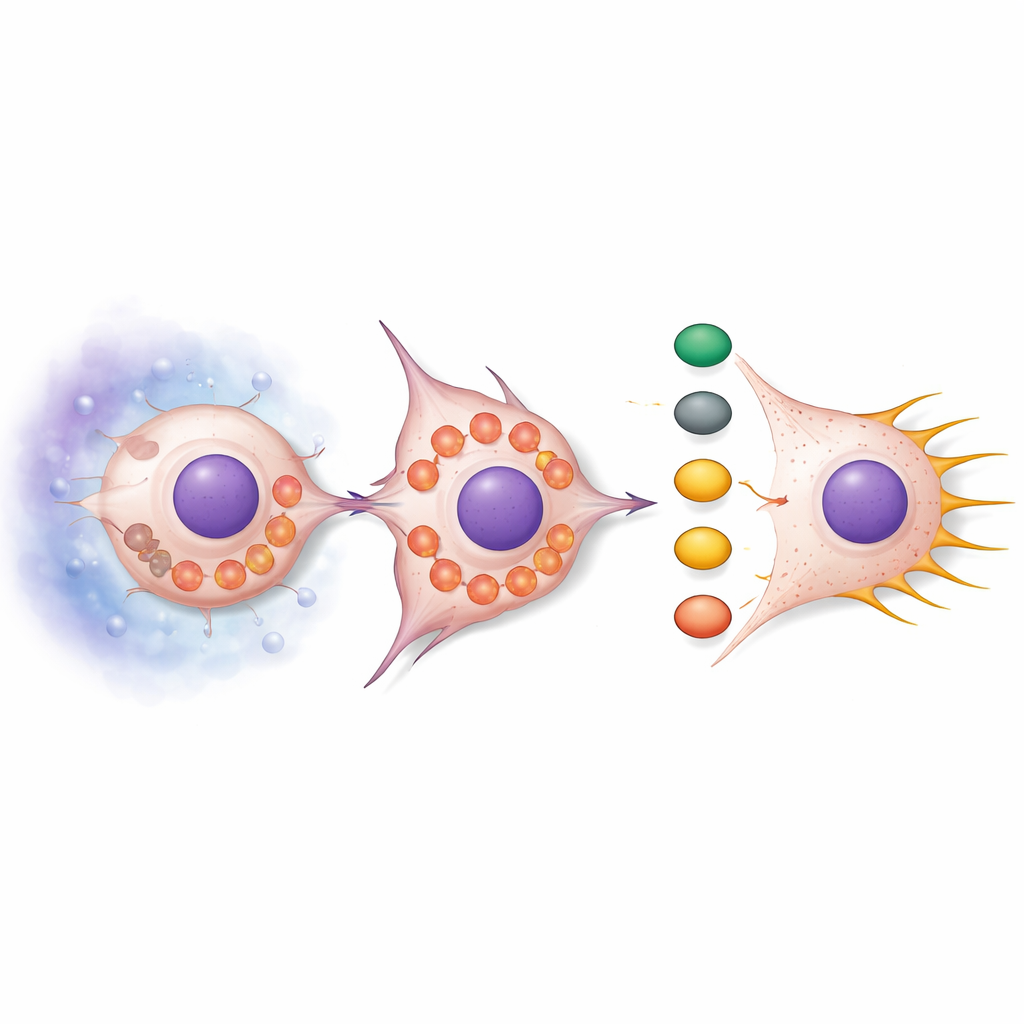
Testando o mecanismo em animais vivos
Para verificar se essa via realmente afeta a disseminação para o fígado, os pesquisadores injetaram células de câncer colorretal com ou sem SNPH adicional em camundongos. Animais que receberam células enriquecidas em SNPH desenvolveram bem menos e menores tumores hepáticos, mesmo que a taxa geral de crescimento das células tumorais fosse semelhante. Microscopia das metástases hepáticas mostrou que tumores superexpressando SNPH tinham mitocôndrias mais longas e fundidas, níveis menores de HIF-1α e ativação mais fraca do braço PAK1/Cofilina da cascata de sinalização. Em outras palavras, restaurar a “âncora” mitocondrial alterou tanto a forma mitocondrial quanto a rede de sinalização química de volta a um estado menos móvel, dificultando a colonização do fígado pelas células cancerosas.
O que isso significa para os pacientes
Em termos simples, este estudo revela uma reação em cadeia: baixa oxigenação nos tumores ativa HIF-1α, que aumenta o miR-130a-3p, que então silencia SNPH. Sem SNPH, as mitocôndrias se fragmentam e migram para a borda celular, gerando mais ROS que ativam uma via de sinalização promotora de movimento. Isso, por sua vez, remodela a superfície celular em filopódios que ajudam as células do câncer colorretal a migrar e a semear o fígado. Alvoar qualquer parte dessa cadeia — HIF-1α, miR-130a-3p, produção de ROS ou as etapas de sinalização a jusante — pode oferecer novas estratégias para prevenir ou limitar metástases hepáticas, e a própria SNPH pode servir como um marcador útil da propensão de um tumor a se disseminar.
Citação: Zhan, L., Li, X., Li, X. et al. HIF-1α suppresses SNPH expression to facilitate liver metastasis of colorectal cancer through regulating mitochondrial dynamics and filopodia formation. Cell Death Dis 17, 380 (2026). https://doi.org/10.1038/s41419-026-08551-1
Palavras-chave: metástase do câncer colorretal, dinâmica mitocondrial, hipóxia HIF-1α, microRNA-130a-3p, espécies reativas de oxigênio