Clear Sky Science · ru
HIF-1α подавляет экспрессию SNPH, способствуя печеночным метастазам колоректального рака через регуляцию митохондриальной динамики и формирования фило-подий
Почему это исследование важно
Колоректальный рак распространён, и примерно у половины пациентов со временем развиваются опухоли в печени, которые трудно лечить и которые часто оказываются смертельными. В этом исследовании внимание сосредоточено на «электростанциях» внутри раковых клеток — митохондриях — чтобы понять, как изменения в их поведении помогают клеткам отрываться от кишечника, путешествовать по организму и закрепляться в печени. Раскрывая скрытую систему управления, связывающую низкий уровень кислорода, энергетическое оборудование и подвижность клеток, работа указывает на новые подходы для замедления или блокирования распространения колоректального рака.
Клеточный регулировщик исчезает
Исследователи сосредоточились на белке синтафилине (SNPH), который действует как регулировщик трафика для митохондрий, помогая им оставаться прикреплёнными и слитыми в сеть. Анализ больших публичных геномных баз данных и образцов пациентов показал: уровни SNPH выше в прилежащей здоровой ткани, ниже в первичных опухолях толстой кишки и наименьшие в печёночных метастазах. У пациентов с низким содержанием SNPH выживаемость была хуже. В клеточных линиях и мышиных моделях повышение уровня SNPH сокращало число и размер печёночных опухолей, тогда как низкий SNPH ассоциировался с более агрессивным метастазированием. Эти закономерности указывают на то, что потеря «якоря» для митохондрий является ключевым шагом, делающим раковые клетки более подвижными и опасными.
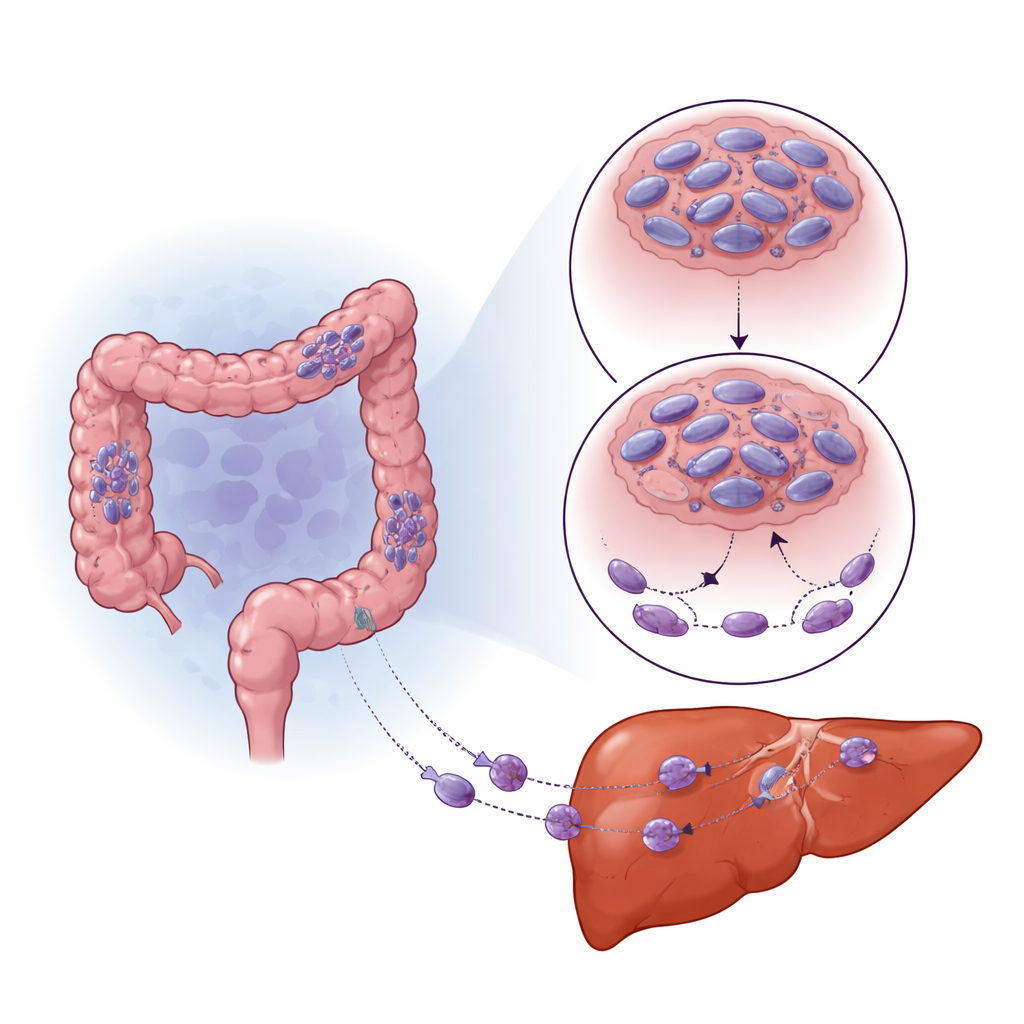
Как низкий уровень кислорода перестраивает поведение опухоли
Твёрдые опухоли часто перерастают кровоснабжение, создавая участки с низким содержанием кислорода (гипоксию). Клетки воспринимают это через главный переключатель — белок HIF-1α, который помогает им адаптироваться и выживать. Учёные заметили, что участки колоректальных опухолей и печёночных метастаз с высоким HIF-1α особенно бедны SNPH. При выращивании раковых клеток в условиях низкого кислорода в лаборатории уровни SNPH резко падали со временем, и клетки становились более подвижными и инвазивными. Блокада HIF-1α частично восстанавливала уровни SNPH и уменьшала прирост подвижности. HIF-1α не выключал SNPH напрямую, а усиливал производство небольшой регуляторной РНК — miR-130a-3p, которая связывалась с матрицей для SNPH и препятствовала его синтезу. Ингибирование miR-130a-3p защищало SNPH, сдерживало рост тонких клеточных «пальцев» и снижало инвазию даже при низком уровне кислорода.
От энергетических станций к «кошкам-ловцам»
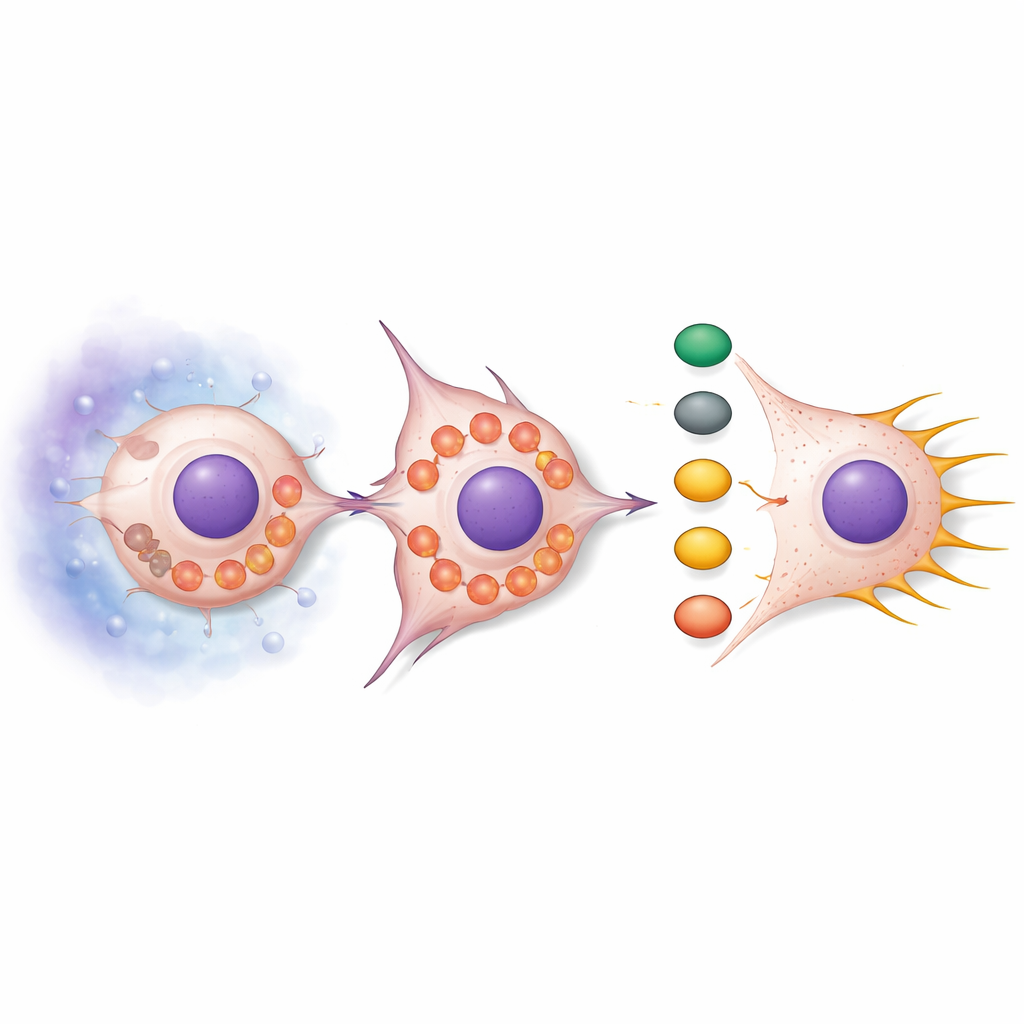
Потеря SNPH делала не только митохондрии более свободными. В норме митохондрии имеют удлинённую и скупчённую форму, но при снижении SNPH они фрагментировались и смещались к периферии клетки. Эта перестройка увеличивала образование активных форм кислорода (ROS) — химически реактивных побочных продуктов метаболизма. ROS запускали сигнальную цепочку, в центре которой стояли белки AKT и cdc42, что в свою очередь активировало downstream-партнёров PAK1 и Cofilin. В результате перестраивался актиновый скелет — внутренний каркас клетки — и появлялись длинные тонкие выросты, называемые фило-подиями. Эти структуры действуют как «кошки-ловцы», помогая клеткам подтягиваться вперёд и протискиваться через окружающие ткани. Обработка клеток антиоксидантами ослабляла эту сигнализацию и уменьшала число фило-подий, тогда как добавление имитаторов ROS делало фило-подии более многочисленными, если только уровень SNPH не восстанавливали.
Проверка механизма в живых животных
Чтобы выяснить, действительно ли этот путь влияет на метастазирование в печень, исследователи вводили колоректальные раковые клетки с повышенным или без повышения SNPH мышам. У животных, получавших клетки с высоким SNPH, развивалось значительно меньше и меньшего размера печёночных опухолей, хотя общий темп роста клеток был похож. Микроскопия печёночных метастаз показала, что опухоли с переэкспрессией SNPH имели более длинные, более слитные митохондрии, более низкий уровень HIF-1α и слабее активированную ветвь PAK1/Cofilin сигнальной каскады. Иными словами, восстановление «якоря» для митохондрий смещало и форму митохондрий, и сеть химических сигналов в сторону менее мобильного состояния, затрудняя колонизацию печени раковыми клетками.
Что это значит для пациентов
Проще говоря, исследование выявляет цепную реакцию: низкий уровень кислорода в опухолях активирует HIF-1α, который повышает уровень miR-130a-3p, и та затем заглушает SNPH. При отсутствии SNPH митохондрии фрагментируются и перемещаются к периферии клетки, увеличивая образование ROS, которые включают сигнальный путь, способствующий подвижности. Это, в свою очередь, преобразует поверхность клетки в фило-подии, помогающие колоректальным раковым клеткам мигрировать и оседать в печени. Таргетирование любой части этой цепочки — HIF-1α, miR-130a-3p, продукции ROS или последующих сигнальных шагов — может предложить новые стратегии для предотвращения или ограничения печёночных метастаз, а сам SNPH может служить полезным маркером склонности рака пациента к распространению.
Цитирование: Zhan, L., Li, X., Li, X. et al. HIF-1α suppresses SNPH expression to facilitate liver metastasis of colorectal cancer through regulating mitochondrial dynamics and filopodia formation. Cell Death Dis 17, 380 (2026). https://doi.org/10.1038/s41419-026-08551-1
Ключевые слова: метастазирование колоректального рака, митохондриальная динамика, гипоксия HIF-1α, микроРНК-130a-3p, активные формы кислорода