Clear Sky Science · de
HIF-1α unterdrückt die SNPH-Expression, um Lebermetastasen von kolorektalem Krebs durch Regulierung der mitochondrialen Dynamik und Filopodienbildung zu erleichtern
Warum diese Forschung wichtig ist
Kolorektaler Krebs ist weit verbreitet, und etwa die Hälfte der Patientinnen und Patienten entwickelt im Verlauf Lebertumoren, die schwer zu behandeln und oft tödlich sind. Diese Studie untersucht die kleinen Kraftwerke in Krebszellen – die Mitochondrien – um zu verstehen, wie Veränderungen ihres Verhaltens Krebszellen helfen, sich aus dem Darm zu lösen, durch den Körper zu wandern und sich in der Leber anzusiedeln. Indem sie ein zuvor verborgenes Kontrollsystem aufdecken, das niedrigen Sauerstoff, Energiemaschinen und Zellbewegung verbindet, weist die Arbeit auf neue Ansätze hin, die Ausbreitung von kolorektalem Krebs zu verlangsamen oder zu blockieren.
Ein zellulärer Verkehrspolizist verschwindet
Die Forschenden konzentrierten sich auf ein Protein namens Syntaphilin (SNPH), das wie ein Verkehrspolizist für Mitochondrien wirkt und hilft, sie zu verankern und miteinander verbunden zu halten. Durch Auswertung großer öffentlicher Gen-Datenbanken und Analyse von Patientenproben stellten sie fest, dass die SNPH-Spiegel im umgebenden gesunden Gewebe höher, in primären kolorektalen Tumoren niedriger und in Lebermetastasen am niedrigsten sind. Patientinnen und Patienten, deren Tumoren wenig SNPH aufwiesen, hatten tendenziell eine schlechtere Überlebensprognose. Sowohl in Zelllinien als auch in Mausmodellen verringerte eine Erhöhung von SNPH die Anzahl und Größe der Lebertumoren, während niedrige SNPH-Werte mit aggressiverer Ausbreitung einhergingen. Diese Muster deuten darauf hin, dass der Verlust dieses mitochondrialen „Ankers“ ein wichtiger Schritt ist, der Krebszellen mobiler und gefährlicher macht.
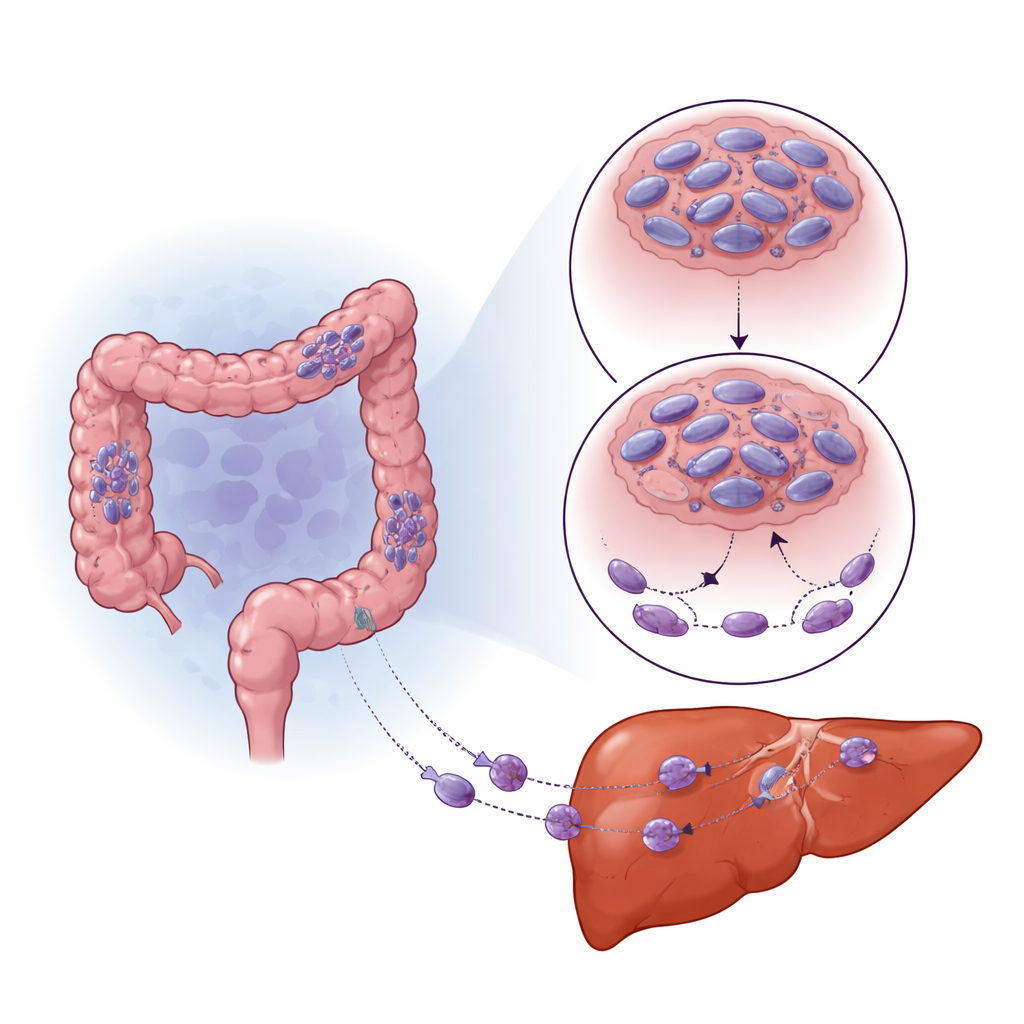
Wie niedriger Sauerstoff das Tumorverhalten umbaut
Feste Tumoren wachsen oft schneller als ihre Blutversorgung, wodurch Bereiche mit niedrigem Sauerstoffgehalt (Hypoxie) entstehen. Zellen erkennen dies über ein Schaltprotein namens HIF-1α, das ihnen hilft, sich anzupassen und zu überleben. Das Team bemerkte, dass Bereiche von kolorektalen Tumoren und Lebermetastasen mit hohem HIF-1α besonders niedrige SNPH-Werte aufwiesen. Wenn sie Krebszellen im Labor unter niedrigen Sauerstoffbedingungen kultivierten, sanken die SNPH-Spiegel im Zeitverlauf stark und die Zellen wurden beweglicher und invasiver. Die Blockade von HIF-1α führte teilweise zu einer Wiederherstellung der SNPH-Spiegel und reduzierte diesen Anstieg der Beweglichkeit. Statt SNPH direkt herunterzuregulieren, erhöhte HIF-1α ein kleines regulatorisches RNA-Molekül, miR-130a-3p, das sich an die SNPH-Botschaft band und deren Proteinproduktion verhinderte. Die Hemmung von miR-130a-3p schützte SNPH, verringerte das Wachstum dünner Zell»finger« und reduzierte die Invasion, selbst unter Niedrigsauerstoffbedingungen.
Von Kraftwerken zu »Greifhaken«
Der Verlust von SNPH bewirkte mehr, als die Mitochondrien nur beweglicher zu machen. Unter normalen Bedingungen sind Mitochondrien oft langgestreckt und in Klumpen angeordnet; bei reduziertem SNPH fragmentierten sie jedoch und drifteten an den Zellrand. Diese Umorganisation steigerte die Produktion reaktiver Sauerstoffspezies (ROS), chemisch reaktive Nebenprodukte des Stoffwechsels. Diese ROS schalteten eine Signalkette um, die AKT und cdc42 in den Mittelpunkt stellt und wiederum die nachgeschalteten Partner PAK1 und Cofilin aktivierte. Die kombinierte Wirkung war eine Umgestaltung des Aktin-Skeletts – des inneren Gerüsts der Zelle – die lange, dünne Fortsätze, sogenannte Filopodien, förderte. Diese Strukturen wirken wie Greifhaken, helfen den Zellen, sich voranzuziehen und sich durch das umgebende Gewebe zu zwängen. Die Behandlung der Zellen mit ROS-Fängern dämpfte diese Signalübertragung und verringerte die Filopodien, während das Zuführen von ROS-Analoga die Filopodienbildung verstärkte, sofern SNPH nicht wiederhergestellt wurde.
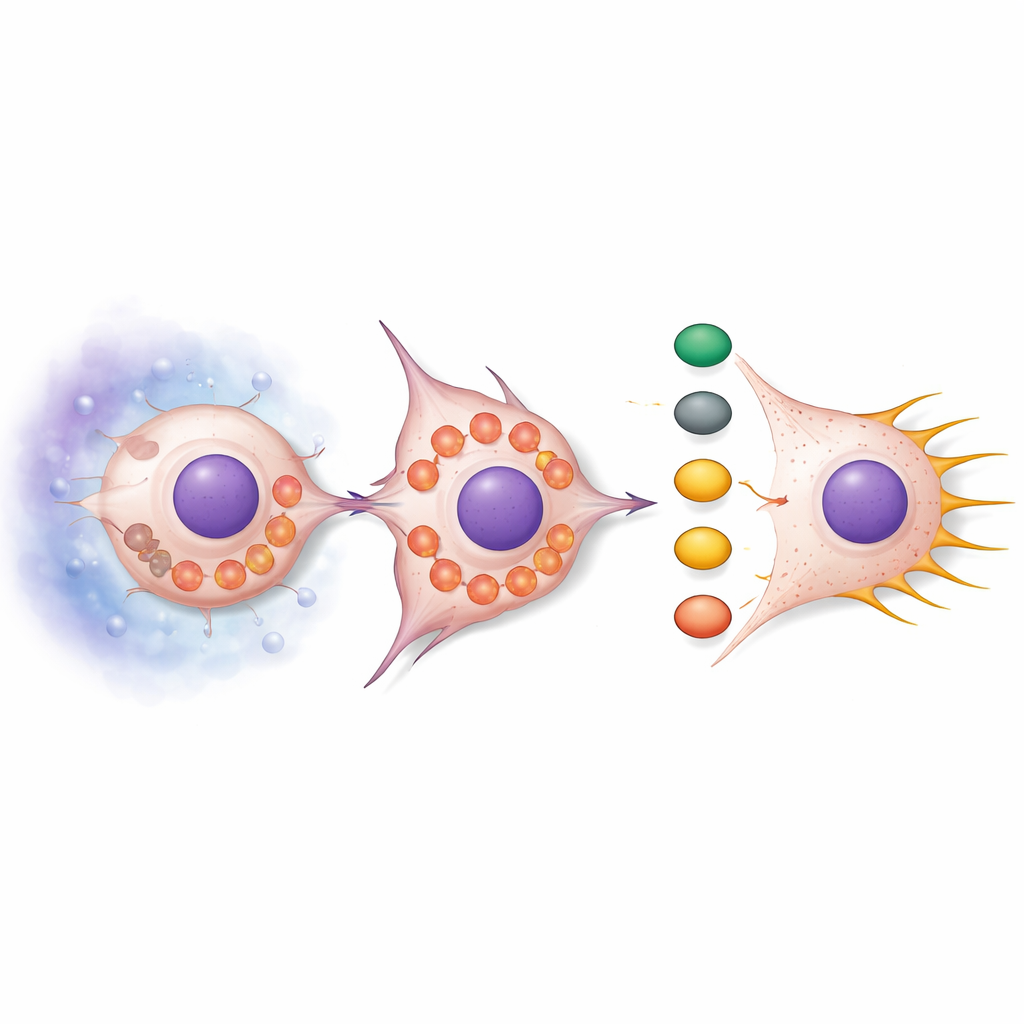
Prüfung des Mechanismus in lebenden Tieren
Um zu prüfen, ob dieser Signalweg tatsächlich die Ausbreitung in die Leber beeinflusst, injizierten die Forschenden kolorektale Krebszellen mit oder ohne zusätzliches SNPH in Mäuse. Tiere, die SNPH-reiche Zellen erhielten, entwickelten deutlich weniger und kleinere Lebertumoren, obwohl die allgemeine Wachstumsrate der Krebszellen ähnlich war. Die Mikroskopie von Lebermetastasen zeigte, dass SNPH-überexprimierende Tumoren längere, stärker verbundene Mitochondrien, niedrigere HIF-1α-Werte und eine schwächere Aktivierung des PAK1/Cofilin-Arms der Signalkaskade aufwiesen. Anders ausgedrückt: Die Wiederherstellung des mitochondrialen „Ankers“ veränderte sowohl die Mitochondrienform als auch das chemische Signalnetzwerk zurück in einen weniger mobilen Zustand und erschwerte es den Krebszellen, die Leber zu besiedeln.
Was das für Patientinnen und Patienten bedeutet
Kurz gesagt zeigt diese Studie eine Kettenreaktion: Niedriger Sauerstoff in Tumoren aktiviert HIF-1α, das miR-130a-3p hochreguliert, welches seinerseits SNPH stilllegt. Ohne SNPH fragmentieren die Mitochondrien und wandern an den Zellrand, wodurch mehr ROS entstehen, die einen bewegungsfördernden Signalweg einschalten. Dies formt die Zelloberfläche zu Filopodien um, die kolorektalen Krebszellen bei der Migration und der Bildung von Lebermetastasen helfen. Die gezielte Beeinflussung eines Glieds dieser Kette – HIF-1α, miR-130a-3p, ROS-Produktion oder die nachgeschalteten Signalschritte – könnte neue Strategien bieten, um Lebermetastasen zu verhindern oder zu begrenzen. Zudem könnte SNPH selbst als nützlicher Marker dafür dienen, wie wahrscheinlich eine Ausbreitung des Tumors ist.
Zitation: Zhan, L., Li, X., Li, X. et al. HIF-1α suppresses SNPH expression to facilitate liver metastasis of colorectal cancer through regulating mitochondrial dynamics and filopodia formation. Cell Death Dis 17, 380 (2026). https://doi.org/10.1038/s41419-026-08551-1
Schlüsselwörter: Metastasierung von kolorektalem Krebs, mitochondriale Dynamik, Hypoxie HIF-1α, microRNA-130a-3p, reaktive Sauerstoffspezies