Clear Sky Science · nl
HIF-1α onderdrukt SNPH-expressie om levermetastasen van colorectale kanker te bevorderen via regulatie van mitochondriale dynamiek en filopodiavorming
Waarom dit onderzoek ertoe doet
Colorectale kanker komt veel voor en ongeveer de helft van de patiënten ontwikkelt uiteindelijk tumoren in de lever, die moeilijk te behandelen en vaak dodelijk zijn. Deze studie onderzoekt de kleine energiecentrales binnen kankercellen — de mitochondriën — om te begrijpen hoe veranderingen in hun gedrag helpen dat kankercellen losraken van de darm, door het lichaam reizen en zich in de lever vestigen. Door een verborgen regelsysteem bloot te leggen dat lage zuurstof, energiemachinerie en celbeweging verbindt, wijst het werk op nieuwe manieren om de verspreiding van colorectale kanker te vertragen of te blokkeren.
Een cellulaire verkeersregelaar raakt zoek
De onderzoekers concentreerden zich op een eiwit genaamd syntaphilin (SNPH), dat als een verkeersagent voor mitochondriën fungeert en helpt ze verankerd en gefuseerd te houden. Door grote openbare genenbanken te doorzoeken en patiëntmonsters te analyseren, vonden ze dat SNPH-niveaus hoger zijn in nabijgelegen gezond weefsel, lager in primaire colorectale tumoren en het laagst in levermetastasen. Patiënten waarvan de tumoren weinig SNPH hadden, hadden doorgaans een slechtere overleving. In celkweken en muismodellen verminderde het verhogen van SNPH het aantal en de grootte van levertumoren, terwijl lage SNPH samenhing met agressievere verspreiding. Deze patronen suggereren dat het verliezen van dit mitochondriale “anker” een sleutelstap is om kankercellen mobieler en gevaarlijker te maken.
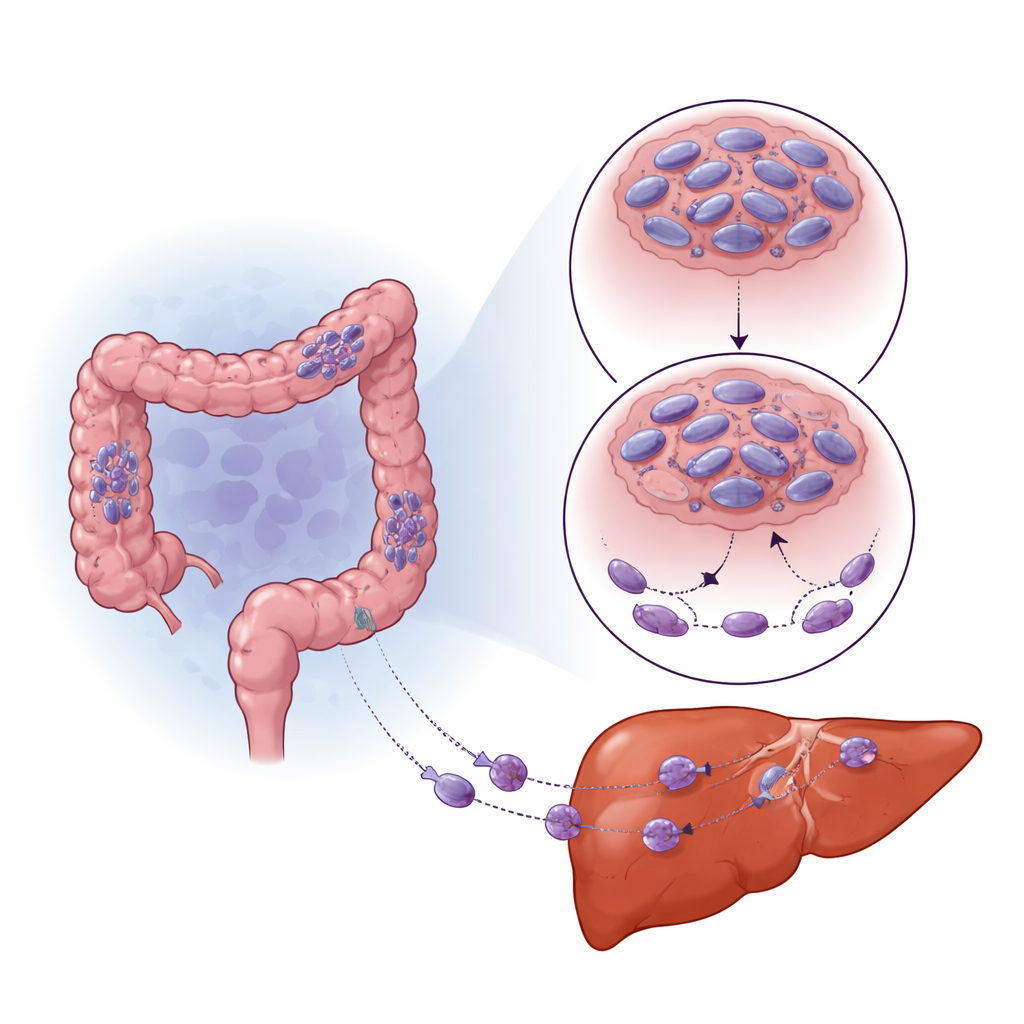
Hoe lage zuurstof het tumorgedrag herschakelt
Vaste tumoren groeien vaak sneller dan hun bloedvoorziening kan bijbenen, waardoor zones met lage zuurstof (hypoxie) ontstaan. Cellen voelen dit via een hoofdschakelaar-eiwit genaamd HIF-1α, dat hen helpt zich aan te passen en te overleven. Het team merkte dat gebieden van colorectale tumoren en levermetastasen met hoge HIF-1α bijzonder lage SNPH hadden. Wanneer ze kankercellen onder lage-zuurstofcondities in het laboratorium kweekten, daalden de SNPH-niveaus scherp in de tijd en werden de cellen beweeglijker en invasiever. Het blokkeren van HIF-1α herstelde SNPH deels en verminderde deze toename in beweging. In plaats van SNPH direct uit te schakelen, verhoogde HIF-1α een kleine regulerende RNA, miR-130a-3p, die vervolgens aan het boodschapper-RNA van SNPH bond en verhinderde dat het eiwit werd gemaakt. Het remmen van miR-130a-3p beschermde SNPH, beperkte de groei van dunne cel "vingers" en verminderde invasie, zelfs bij lage zuurstof.
Van energiecentrales naar "grijphaakjes"
Het verlies van SNPH deed meer dan alleen mitochondriën vrijer laten bewegen. Onder normale omstandigheden zijn mitochondriën vaak verlengd en geclusterd, maar wanneer SNPH werd verminderd, raakten ze gefragmenteerd en verschilden ze naar de rand van de cel. Deze herschikking verhoogde de productie van reactieve zuurstofsoorten (ROS), chemisch reactieve bijproducten van de stofwisseling. Deze ROS schakelden een signaalroute in rondom de eiwitten AKT en cdc42, die op hun beurt downstream-partners PAK1 en Cofilin activeerden. Het gecombineerde effect was een herstructurering van het actine-skelet — het interne geraamte van de cel — wat de vorming van lange, dunne uitstulpingen genaamd filopodia bevorderde. Deze structuren functioneren als grijphaakjes en helpen cellen zichzelf vooruit te trekken en door omliggend weefsel te persen. Behandeling van cellen met ROS-opschoners dempte deze signalering en verminderde filopodia, terwijl het toevoegen van ROS-analogen leidde tot meer filopodia tenzij SNPH werd hersteld.
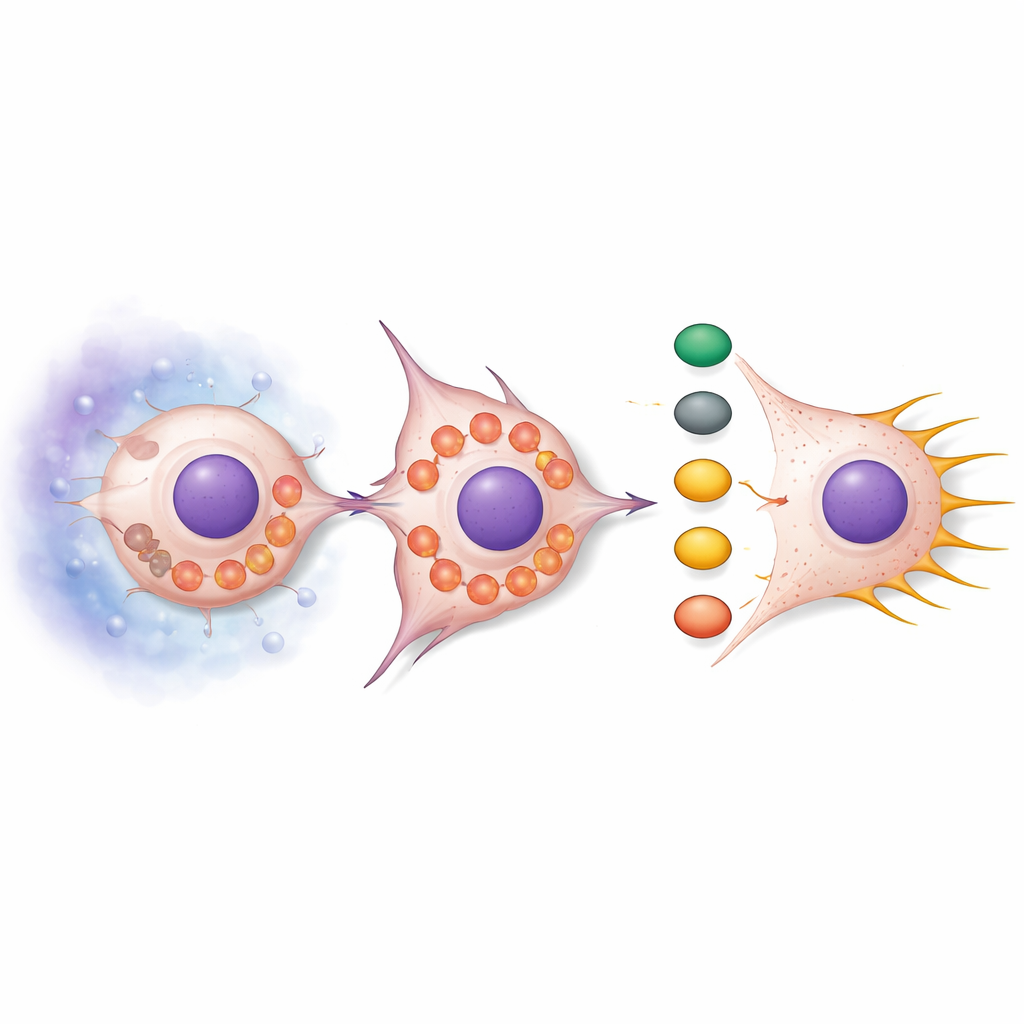
Het mechanisme testen in levende dieren
Om te zien of deze route daadwerkelijk de verspreiding naar de lever beïnvloedt, injecteerden de onderzoekers colorectale kankercellen met of zonder extra SNPH in muizen. Dieren die SNPH-rijke cellen ontvingen, ontwikkelden veel minder en kleinere levertumoren, hoewel het algemene groeitempo van de kankercellen vergelijkbaar was. Microscopen van levermetastasen toonden dat SNPH-overexpressieve tumoren langere, meer gefuseerde mitochondriën hadden, lagere HIF-1α-niveaus en zwakkere activatie van de PAK1/Cofilin-arm van de signaalcascade. Met andere woorden, het herstellen van het mitochondriale "anker" verschuift zowel de mitochondriale vorm als het chemische boodschapsnetwerk terug naar een minder mobiel stadium, waardoor het voor kankercellen moeilijker wordt de lever te koloniseren.
Wat het betekent voor patiënten
Kort gezegd onthult deze studie een kettingreactie: lage zuurstof in tumoren activeert HIF-1α, dat miR-130a-3p inschakelt, dat vervolgens SNPH stillegt. Zonder SNPH fragmenteren mitochondriën en verplaatsen ze zich naar de celrand, waarbij meer ROS wordt gegenereerd die een beweging-bevorderende signaalroute inschakelen. Dat herschikt het celoppervlak in filopodia die colorectale kankercellen helpen migreren en de lever in te zaaien. Het richten op elk deel van deze keten — HIF-1α, miR-130a-3p, ROS-productie of de downstream signaalstappen — kan nieuwe strategieën bieden om levermetastasen te voorkomen of te beperken, en SNPH zelf kan dienen als een nuttige marker voor hoe waarschijnlijk het is dat de kanker van een patiënt zal uitzaaien.
Bronvermelding: Zhan, L., Li, X., Li, X. et al. HIF-1α suppresses SNPH expression to facilitate liver metastasis of colorectal cancer through regulating mitochondrial dynamics and filopodia formation. Cell Death Dis 17, 380 (2026). https://doi.org/10.1038/s41419-026-08551-1
Trefwoorden: metastase van colorectale kanker, mitochondriale dynamiek, hypoxie HIF-1α, microRNA-130a-3p, reactieve zuurstofsoorten