Clear Sky Science · it
HIF-1α sopprime l'espressione di SNPH per facilitare la metastasi epatica del cancro colorettale regolando la dinamica mitocondriale e la formazione di filopodi
Perché questa ricerca è importante
Il cancro colorettale è comune e circa la metà dei pazienti sviluppa infine tumori nel fegato, che sono difficili da trattare e spesso letali. Questo studio esplora le piccole centrali energetiche all'interno delle cellule tumorali — i mitocondri — per capire come i cambiamenti nel loro comportamento aiutino le cellule tumorali a staccarsi dall'intestino, viaggiare attraverso il corpo e insediarsi nel fegato. Svelando un sistema di controllo nascosto che collega la bassa ossigenazione, la macchina energetica e il movimento cellulare, il lavoro indica nuovi modi per rallentare o bloccare la diffusione del cancro colorettale.
Un vigile del traffico cellulare che scompare
I ricercatori si sono concentrati su una proteina chiamata syntaphilin (SNPH), che funziona come un vigile del traffico per i mitocondri, aiutandoli a rimanere ancorati e fusi insieme. Analizzando ampi database genici pubblici e campioni di pazienti, hanno scoperto che i livelli di SNPH sono più alti nei tessuti sani circostanti, più bassi nei tumori colorettali primari e più bassi ancora nelle metastasi epatiche. I pazienti i cui tumori presentavano pochi SNPH tendevano ad avere una sopravvivenza peggiore. Sia nelle linee cellulari sia nei modelli murini, aumentare SNPH ha ridotto il numero e le dimensioni dei tumori epatici, mentre bassi livelli di SNPH erano associati a una diffusione più aggressiva. Questi schemi suggeriscono che la perdita di questo “ancoraggio” mitocondriale è un passo chiave che rende le cellule tumorali più mobili e pericolose.
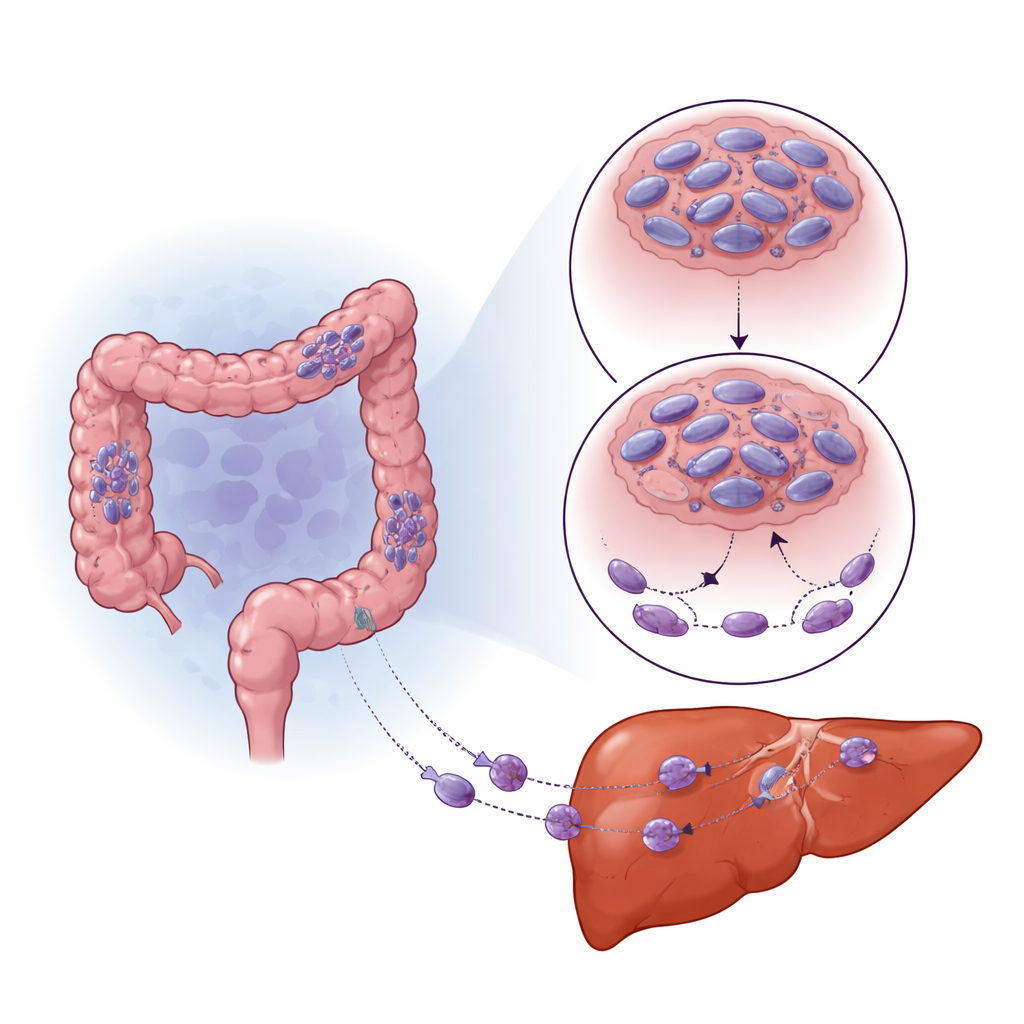
Come la bassa ossigenazione riorganizza il comportamento del tumore
I tumori solidi spesso superano il loro apporto di sangue, creando aree a bassa ossigenazione (ipossia). Le cellule percepiscono questo attraverso una proteina chiave chiamata HIF-1α, che le aiuta ad adattarsi e sopravvivere. Il gruppo ha osservato che le aree dei tumori colorettali e delle metastasi epatiche con alti livelli di HIF-1α avevano particolarmente bassi livelli di SNPH. Quando hanno coltivato le cellule tumorali in condizioni di basso ossigeno in laboratorio, i livelli di SNPH sono diminuiti rapidamente nel tempo e le cellule sono diventate più mobili e invasive. Bloccare HIF-1α ha parzialmente ristabilito i livelli di SNPH e ridotto questo aumento del movimento. Piuttosto che spegnere SNPH direttamente, HIF-1α ha aumentato un piccolo RNA regolatorio, miR-130a-3p, che si lega al messaggio di SNPH impedendone la traduzione. Inibire miR-130a-3p ha protetto SNPH, limitato la crescita di sottili “dita” cellulari e ridotto l'invasione, anche in condizioni di bassa ossigenazione.
Dalle centrali elettriche ai “grappini”
La perdita di SNPH ha fatto più che liberare i mitocondri per spostarsi. In condizioni normali i mitocondri tendono a essere allungati e raggruppati, ma quando SNPH è stato ridotto si sono frammentati e sono migrati verso il bordo cellulare. Questa riorganizzazione ha aumentato la produzione di specie reattive dell'ossigeno (ROS), sottoprodotti chimicamente reattivi del metabolismo. Queste ROS hanno attivato una cascata di segnalazione incentrata sulle proteine AKT e cdc42, che a loro volta hanno attivato partner a valle come PAK1 e Cofilin. L'effetto combinato è stato un rimodellamento del citoscheletro di actina — l'impalcatura interna della cellula — promuovendo protrusioni lunghe e sottili chiamate filopodi. Queste strutture funzionano come grappini, aiutando le cellule a tirarsi in avanti e a farsi strada attraverso i tessuti circostanti. Il trattamento delle cellule con spazzini di ROS ha attenuato questa segnalazione e ridotto i filopodi, mentre l'aggiunta di simulacri di ROS ha aumentato i filopodi a meno che SNPH non venisse ripristinato.
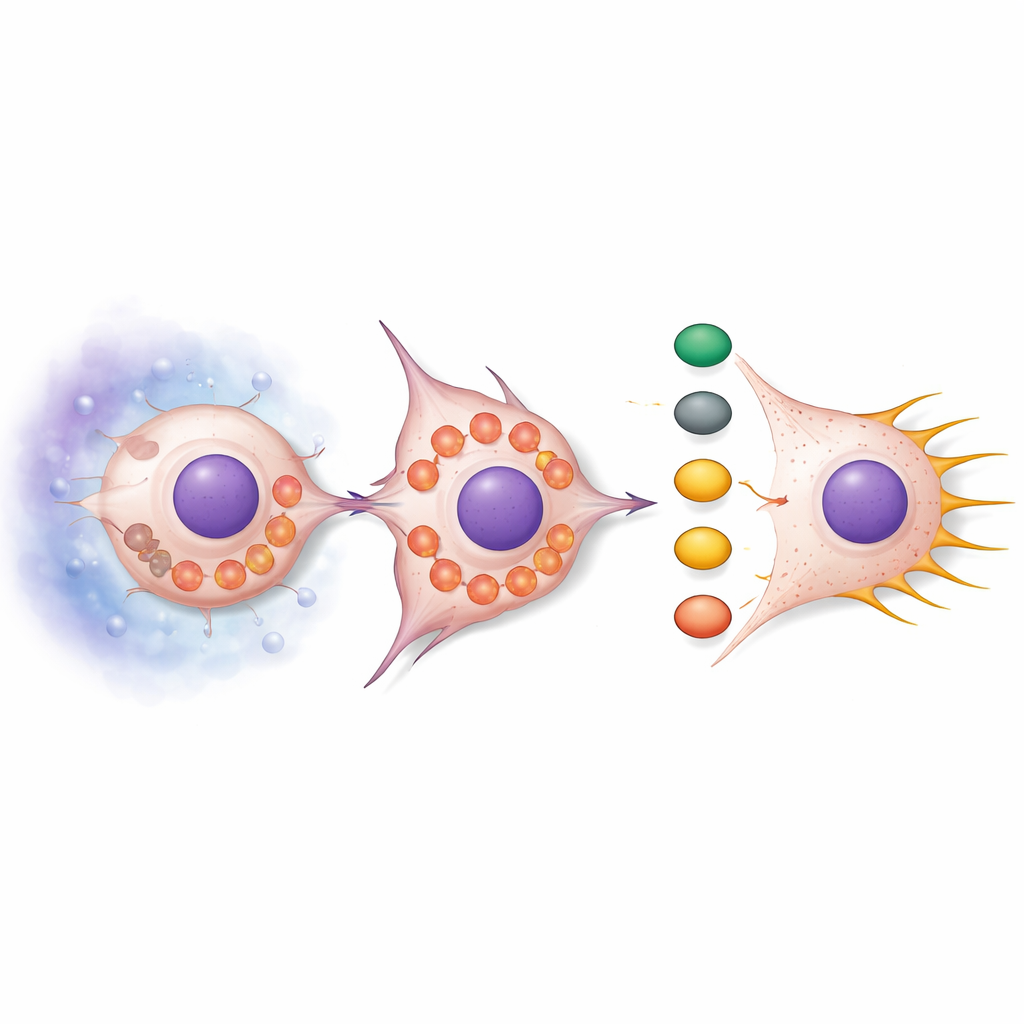
Testare il meccanismo in animali vivi
Per verificare se questa via influenzasse davvero la diffusione al fegato, i ricercatori hanno iniettato cellule di cancro colorettale con o senza SNPH supplementare in topi. Gli animali che hanno ricevuto cellule ricche di SNPH hanno sviluppato molti meno e più piccoli tumori epatici, nonostante il tasso di crescita complessivo delle cellule tumorali fosse simile. La microscopia delle metastasi epatiche ha mostrato che i tumori sovraesprimenti di SNPH avevano mitocondri più lunghi e fusi, livelli più bassi di HIF-1α e una minore attivazione del braccio PAK1/Cofilin della cascata di segnalazione. In altre parole, ripristinare l’“ancora” mitocondriale ha spostato sia la forma mitocondriale sia la rete di segnali chimici verso uno stato meno mobile, rendendo più difficile alle cellule tumorali colonizzare il fegato.
Cosa significa per i pazienti
In termini semplici, questo studio rivela una reazione a catena: la bassa ossigenazione nei tumori attiva HIF-1α, che aumenta miR-130a-3p, il quale poi silenzia SNPH. Senza SNPH, i mitocondri si frammentano e migrano verso il bordo cellulare, generando più ROS che attivano una via di segnalazione che favorisce il movimento. Questo rimodella la superficie cellulare in filopodi che aiutano le cellule del cancro colorettale a migrare e impiantarsi nel fegato. Mirare a uno qualsiasi degli anelli di questa catena — HIF-1α, miR-130a-3p, la produzione di ROS o i passaggi di segnalazione a valle — potrebbe offrire nuove strategie per prevenire o limitare le metastasi epatiche, e lo stesso SNPH potrebbe servire come un utile marcatore della probabilità che il cancro di un paziente si diffonda.
Citazione: Zhan, L., Li, X., Li, X. et al. HIF-1α suppresses SNPH expression to facilitate liver metastasis of colorectal cancer through regulating mitochondrial dynamics and filopodia formation. Cell Death Dis 17, 380 (2026). https://doi.org/10.1038/s41419-026-08551-1
Parole chiave: metastasi del cancro colorettale, dinamica mitocondriale, ipossia HIF-1α, microRNA-130a-3p, specie reattive dell'ossigeno