Clear Sky Science · pl
HIF-1α tłumi ekspresję SNPH, ułatwiając przerzuty raka jelita grubego do wątroby przez regulację dynamiki mitochondriów i formowania filopodiów
Dlaczego to badanie ma znaczenie
Rak jelita grubego jest powszechny, a około połowa pacjentów w końcu rozwija guzy w wątrobie, które są trudne do leczenia i często śmiertelne. Badanie to zagląda do drobnych elektrowni wewnątrz komórek nowotworowych — mitochondriów — aby zrozumieć, jak zmiany w ich zachowaniu pomagają komórkom nowotworowym oderwać się od jelita, przemieszczać przez organizm i osiedlać się w wątrobie. Odkrywając ukryty system kontroli łączący niski poziom tlenu, maszynerię energetyczną i ruch komórek, praca ta wskazuje nowe sposoby spowolnienia lub zablokowania rozprzestrzeniania się raka jelita grubego.
Komórkowy „policjant ruchu” znika
Naukowcy skupili się na białku zwanym syntaphilinem (SNPH), które działa jak policjant kierujący mitochondriami, pomagając utrzymać je zakotwiczone i zespalane. Analizując duże publiczne bazy danych genowych i próbki pacjentów, stwierdzili, że poziomy SNPH są wyższe w przylegającej zdrowej tkance, niższe w pierwotnych guzach jelita grubego i najniższe w przerzutach do wątroby. Pacjenci, których guzy miały niewiele SNPH, mieli skłonność do gorszego przeżycia. W liniach komórkowych i modelach mysich zwiększenie SNPH zmniejszało liczbę i rozmiar guzów wątroby, podczas gdy niski poziom SNPH wiązał się z bardziej agresywnym rozsiewem. Te wzorce sugerują, że utrata tego mitochondrialnego „kotwicznego” białka jest kluczowym krokiem upośledzającym mobilność i zwiększającym zjadliwość komórek nowotworowych.
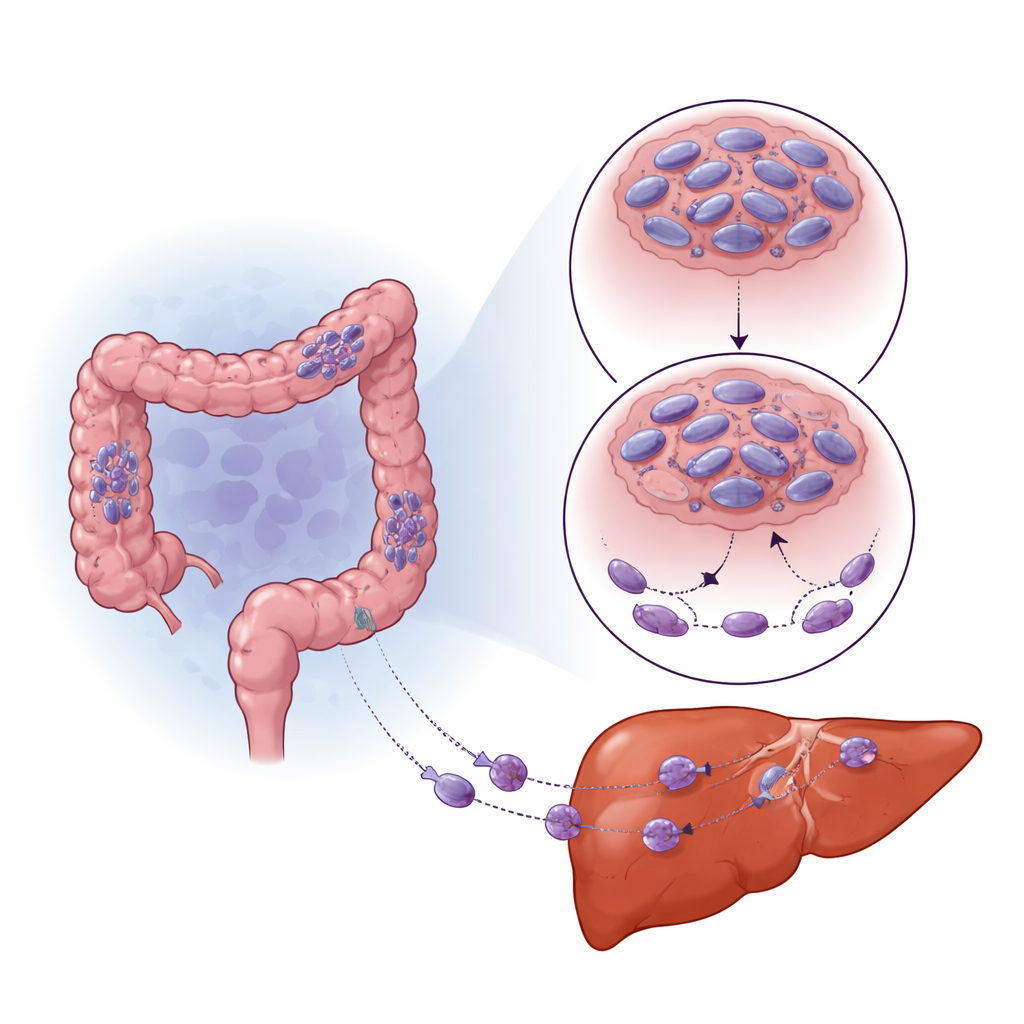
Jak niski tlen przestawia zachowanie guza
Guzy lite często przerastają dopływ krwi, tworząc obszary o niskim poziomie tlenu (hipoksję). Komórki wykrywają to przez główny przełącznik białkowy HIF-1α, który pomaga im adaptować się i przetrwać. Zespół zauważył, że obszary guzów jelita grubego i przerzutów do wątroby z wysokim HIF-1α miały szczególnie niski SNPH. Kiedy hodowali komórki nowotworowe w warunkach niskiego tlenu, poziomy SNPH gwałtownie spadały w czasie, a komórki stawały się bardziej ruchliwe i inwazyjne. Zablokowanie HIF-1α częściowo przywracało poziomy SNPH i ograniczało wzrost ruchliwości. Zamiast wyłączać SNPH bezpośrednio, HIF-1α zwiększał poziom małego regulatorowego RNA, miR-130a-3p, który następnie wiązał się z informacją dla SNPH i hamował jego produkcję. Hamowanie miR-130a-3p chroniło SNPH, ograniczało wzrost cienkich „palców” komórek i zmniejszało inwazję, nawet w warunkach niskiego tlenu.
Od elektrowni do „haków chwytających”
Utrata SNPH robiła więcej niż tylko uwalniała mitochondria do przemieszczania się. W normalnych warunkach mitochondria mają tendencję do wydłużania i skupiania się, ale gdy SNPH był zmniejszony, ulegały fragmentacji i przesuwały się na obwód komórki. Ta reorganizacja zwiększała produkcję reaktywnych form tlenu (ROS), reaktywnych chemicznie produktów ubocznych metabolizmu. ROS uruchamiały łańcuch sygnałowy skoncentrowany wokół białek AKT i cdc42, które z kolei aktywowały dalszych partnerów PAK1 i Cofilin. Efekt końcowy to przebudowa cytoszkieletu aktynowego — wewnętrznej rusztowania komórki — sprzyjająca długim, cienkim wypustkom zwanym filopodiami. Struktury te działają jak haki chwytające, pomagając komórkom przesuwać się naprzód i wciskać przez otaczającą tkankę. Leczenie komórek środkami wychwytującymi ROS tłumiło to sygnalizowanie i zmniejszało liczbę filopodiów, podczas gdy dodanie mimików ROS zwiększało filopodia, chyba że SNPH został przywrócony.
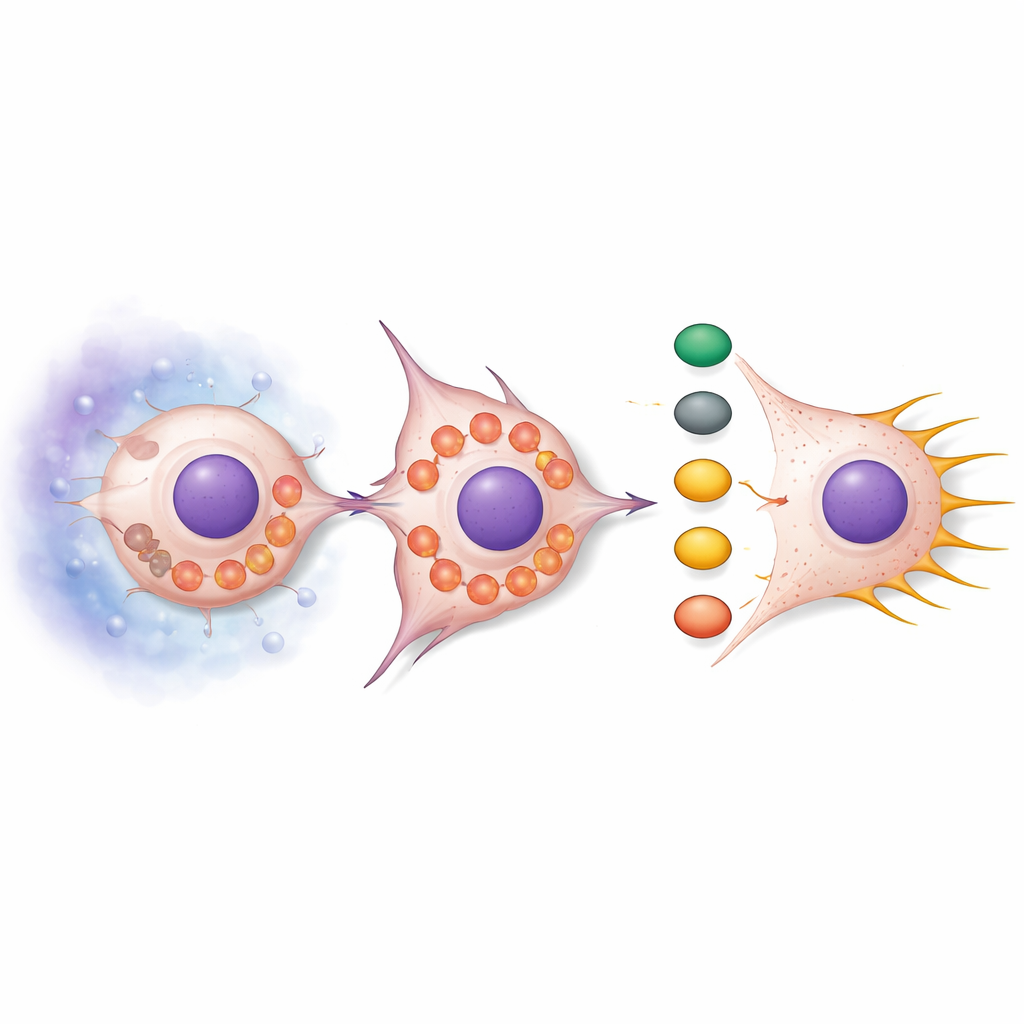
Testowanie mechanizmu u żywych zwierząt
Aby sprawdzić, czy ta ścieżka naprawdę wpływa na przerzuty do wątroby, badacze wstrzyknęli komórki raka jelita grubego z dodatkiem lub bez dodatkowego SNPH do myszy. Zwierzęta otrzymujące komórki bogate w SNPH rozwijały znacznie mniej i mniejsze guzy wątroby, mimo że ogólny wskaźnik wzrostu komórek nowotworowych był podobny. Mikroskopia przerzutów w wątrobie pokazała, że guzy nadekspresyjne SNPH miały dłuższe, bardziej zespolone mitochondria, niższe poziomy HIF-1α i słabszą aktywację odgałęzienia sygnałowego PAK1/Cofilin. Innymi słowy, przywrócenie mitochondrialnej „kotwicy” przestawiło zarówno kształt mitochondriów, jak i sieć sygnałową z powrotem w kierunku mniej ruchliwego stanu, utrudniając komórkom nowotworowym kolonizację wątroby.
Co to oznacza dla pacjentów
Mówiąc wprost, badanie ujawnia reakcję łańcuchową: niski tlen w guzach aktywuje HIF-1α, który zwiększa miR-130a-3p, a ten wycisza SNPH. Bez SNPH mitochondria ulegają fragmentacji i przesuwają się na obrzeże komórki, generując więcej ROS, które uruchamiają ścieżkę sygnałową sprzyjającą ruchowi. To z kolei przekształca powierzchnię komórki w filopodie, które pomagają komórkom raka jelita grubego migrować i osiadać w wątrobie. Celowanie w dowolny element tego łańcucha — HIF-1α, miR-130a-3p, produkcję ROS lub dalsze kroki sygnalizacyjne — może dać nowe strategie zapobiegania lub ograniczania przerzutów do wątroby, a sam SNPH może służyć jako użyteczny marker prawdopodobieństwa rozsiewu nowotworu u pacjenta.
Cytowanie: Zhan, L., Li, X., Li, X. et al. HIF-1α suppresses SNPH expression to facilitate liver metastasis of colorectal cancer through regulating mitochondrial dynamics and filopodia formation. Cell Death Dis 17, 380 (2026). https://doi.org/10.1038/s41419-026-08551-1
Słowa kluczowe: przerzuty raka jelita grubego, dynamika mitochondriów, hipoksja HIF-1α, microRNA-130a-3p, reaktywne formy tlenu