Clear Sky Science · tr
HIF-1α, mitokondriyal dinamikleri ve filopodi oluşumunu düzenleyerek kolorektal kanserin karaciğer metastazını kolaylaştırmak için SNPH ekspresyonunu baskılar
Bu araştırma neden önemli
Kolorektal kanser yaygın bir hastalıktır ve hastaların yaklaşık yarısı sonunda karaciğerde tümör gelişimi yaşar; bu tümörler tedavisi zor ve sık sık ölümcül olur. Bu çalışma, kanser hücrelerinin içindeki küçük enerji santralleri olan mitokondrileri inceliyor ve mitokondri davranışındaki değişikliklerin kanser hücrelerinin bağırsaktan kopup vücutta yolculuk ederek karaciğerde yerleşmesine nasıl yardımcı olduğunu anlamaya çalışıyor. Düşük oksijen, enerji makineleri ve hücre hareketini birbirine bağlayan gizli bir kontrol sistemini açığa çıkararak kolorektal kanserin yayılmasını yavaşlatma veya engelleme için yeni yollar öneriyor.
Hücre trafiğinin düzenleyicisi kayboluyor
Araştırmacılar, mitokondriler için bir trafik polisi gibi davranan ve onların sabitlenmesine ve birleşik kalmasına yardımcı olan syntaphilin (SNPH) adlı bir proteine odaklandı. Büyük kamu gen veri tabanlarını tarayarak ve hasta örneklerini analiz ederek SNPH düzeylerinin çevre sağlıklı dokuda daha yüksek, primer kolorektal tümörlerde daha düşük ve karaciğer metastazlarında en düşük olduğunu buldular. Tümörlerinde az SNPH olan hastaların hayatta kalma oranları genellikle daha kötüydü. Hem hücre dizilerinde hem de fare modellerinde SNPH artırıldığında karaciğerdeki tümörlerin sayısı ve boyutu azaldı; düşük SNPH ise daha agresif yayılma ile ilişkilendirildi. Bu desenler, mitokondriyal “çapa”nın kaybının kanser hücrelerini daha hareketli ve tehlikeli hale getiren kilit bir adım olduğunu öne sürüyor.
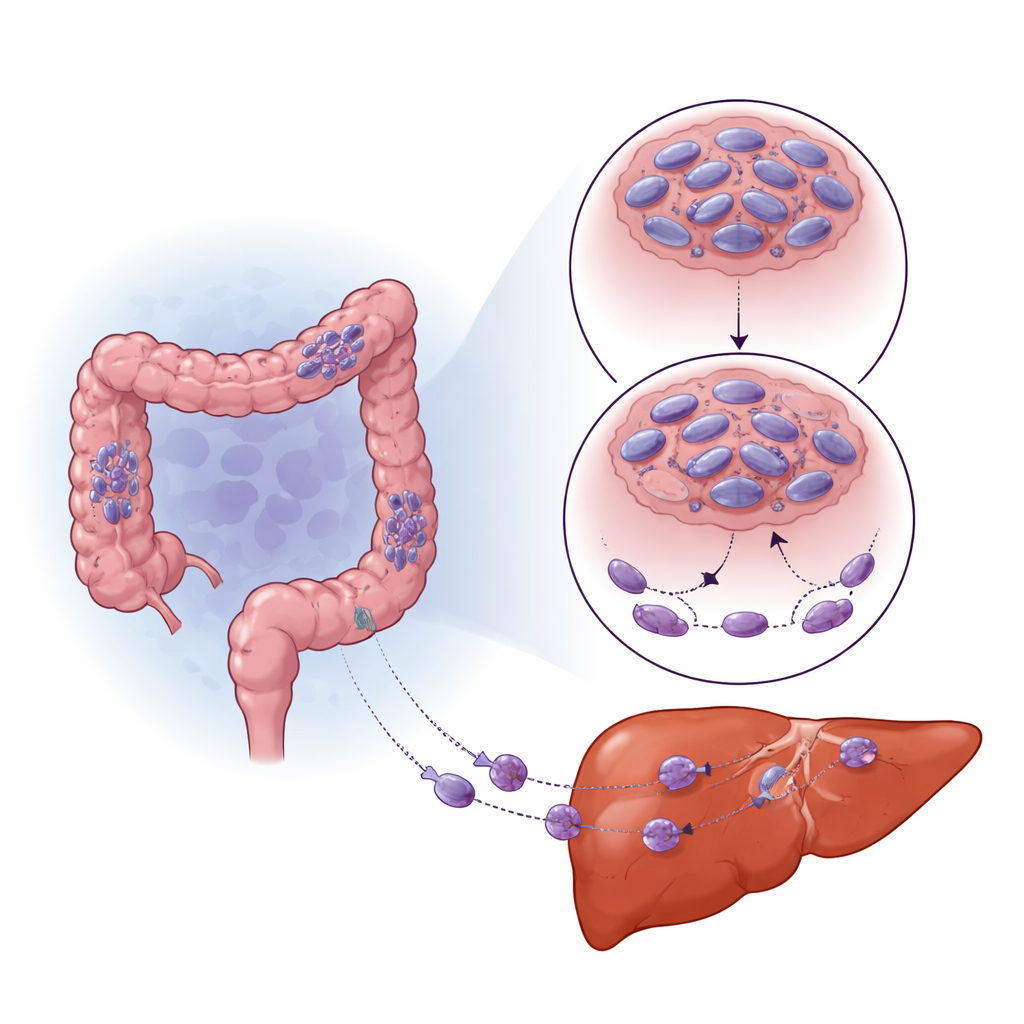
Düşük oksijen tümör davranışını nasıl yeniden kablolar
Katı tümörler sıklıkla kanlanmalarını aşar ve düşük oksijen (hipoksi) cepleri oluşturur. Hücreler bunu HIF-1α adlı anahtar bir anahtar protein aracılığıyla algılar; bu protein onların uyum sağlamasına ve hayatta kalmasına yardım eder. Ekip, kolorektal tümörler ve karaciğer metastazlarının HIF-1α düzeyi yüksek bölgelerinde özellikle düşük SNPH olduğunu fark etti. Laboratuvarda kanser hücrelerini düşük oksijen koşullarında yetiştirdiklerinde, SNPH düzeyleri zaman içinde hızla düştü ve hücreler daha hareketli ve invaziv hale geldi. HIF-1α'yı engellemek SNPH düzeylerini kısmen geri getirdi ve bu hareket artışını azalttı. HIF-1α doğrudan SNPH’yi kapatmak yerine küçük bir düzenleyici RNA olan miR-130a-3p'yi artırdı; bu RNA da SNPH’nin mesajına bağlanıp onun üretilmesini engelledi. miR-130a-3p'yi inhibe etmek SNPH’yi korudu, ince hücre “parmakları”nın büyümesini azalttı ve hipoksi altında bile invazyonu kısıtladı.
Enerji santrallerinden “çengel”lere
SNPH kaybı, mitokondrileri serbest bırakmanın ötesinde etkiler yarattı. Normal koşullarda mitokondriler genellikle uzamış ve kümelenmiş haldeyken, SNPH azaldığında parçalandılar ve hücrenin dış kenarına doğru sürüklendiler. Bu yeniden düzenleme, metabolizmanın kimyasal olarak reaktif yan ürünleri olan reaktif oksijen türleri (ROS) üretimini artırdı. Bu ROS’lar AKT ve cdc42 proteinleri etrafında merkezlenen bir sinyal zincirini açığa çıkardı; bu zincir daha sonra PAK1 ve Cofilin gibi aşağı akış ortaklarını etkinleştirdi. Birleşik etki, hücrenin iç iskelesi olan aktin iskeletinin yeniden şekillenmesi oldu ve uzun, ince çıkıntılar olan filopodilerin oluşumunu teşvik etti. Bu yapılar çengel gibi davranarak hücrelerin kendilerini ileri çekmesine ve çevre doku arasından sıkışarak geçmesine yardımcı olur. Hücrelere ROS temizleyiciler uygulamak bu sinyali zayıflattı ve filopodileri azalttı; ROS taklitçileri eklemek ise SNPH geri getirilmediği sürece filopodileri arttırdı.
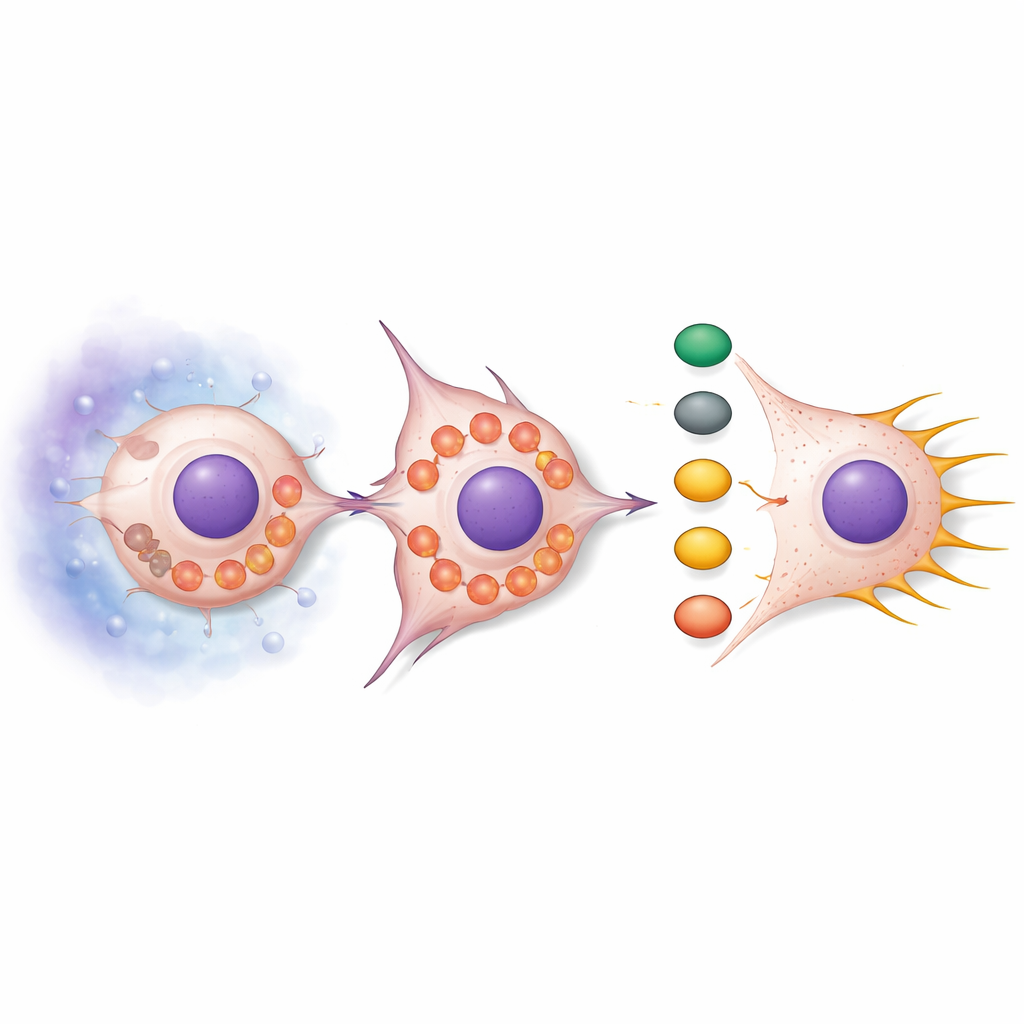
Mekanizmayı canlı hayvanlarda test etmek
Bu yolun gerçekten karaciğere yayılmayı etkileyip etkilemediğini görmek için araştırmacılar, ekstra SNPH içeren veya içermeyen kolorektal kanser hücrelerini farelere enjekte ettiler. SNPH açısından zengin hücreleri alan hayvanlarda çok daha az ve küçük karaciğer tümörü gelişti; bu arada kanser hücrelerinin genel büyüme hızı benzerdi. Karaciğer metastazlarının mikroskobik incelemesi, SNPH fazla eksprese edilmiş tümörlerin daha uzun, daha birleşik mitokondrilere, daha düşük HIF-1α düzeylerine ve sinyal kaskadının PAK1/Cofilin kolunun daha zayıf aktivasyonuna sahip olduğunu gösterdi. Başka bir deyişle, mitokondriyal “çapa”yı geri getirmek hem mitokondri şekli hem de kimyasal haberleşme ağını daha az hareketli bir duruma kaydırarak kanser hücrelerinin karaciğeri kolonize etmesini zorlaştırdı.
Hastalar için ne anlama geliyor
Basitçe söylemek gerekirse, bu çalışma bir zincirleme reaksiyonu ortaya koyuyor: tümörlerdeki düşük oksijen HIF-1α’yı aktive ediyor, HIF-1α miR-130a-3p’yi açıyor ve bu da SNPH’yi susturuyor. SNPH olmadan mitokondriler parçalanıp hücre kenarına hareket ediyor, daha fazla ROS üretiyor ve hareketi teşvik eden bir sinyal yolunu yakıyor. Bu yol da hücre yüzeyini filopodiler halinde yeniden şekillendirerek kolorektal kanser hücrelerinin göç etmesine ve karaciğeri tohumlamasına yardımcı oluyor. Bu zincirin herhangi bir parçasını — HIF-1α, miR-130a-3p, ROS üretimi veya aşağı akış sinyal adımlarını — hedeflemek karaciğer metastazını önlemek veya sınırlamak için yeni stratejiler sunabilir ve SNPH kendisi de bir hastanın kanserinin yayılma olasılığını gösteren yararlı bir belirteç olarak hizmet edebilir.
Atıf: Zhan, L., Li, X., Li, X. et al. HIF-1α suppresses SNPH expression to facilitate liver metastasis of colorectal cancer through regulating mitochondrial dynamics and filopodia formation. Cell Death Dis 17, 380 (2026). https://doi.org/10.1038/s41419-026-08551-1
Anahtar kelimeler: kolorektal kanser metastazı, mitokondriyal dinamikler, hipoksi HIF-1α, mikroRNA-130a-3p, reaktif oksijen türleri