Clear Sky Science · fr
HIF-1α supprime l'expression de SNPH pour faciliter les métastases hépatiques du cancer colorectal en régulant la dynamique mitochondriale et la formation de filopodes
Pourquoi cette recherche est importante
Le cancer colorectal est fréquent et environ la moitié des patients finissent par développer des tumeurs au foie, difficiles à traiter et souvent mortelles. Cette étude examine les petites centrales énergétiques des cellules cancéreuses — les mitochondries — pour comprendre comment des modifications de leur comportement aident les cellules tumorales à se détacher de l’intestin, voyager dans l’organisme et s’implanter dans le foie. En révélant un système de régulation qui relie faible oxygénation, machinerie énergétique et mobilité cellulaire, ce travail ouvre la voie à de nouvelles stratégies pour ralentir ou bloquer la dissémination du cancer colorectal.
Un « policier du trafic » cellulaire qui disparaît
Les chercheurs se sont concentrés sur une protéine appelée syntaphiline (SNPH), qui joue le rôle d’un « policier du trafic » pour les mitochondries, contribuant à les ancrer et à les maintenir fusionnées. En exploitant de larges bases de données publiques et en analysant des prélèvements de patients, ils ont constaté que les niveaux de SNPH sont plus élevés dans les tissus sains adjacents, plus faibles dans les tumeurs colorectales primaires et les plus bas dans les métastases hépatiques. Les patients dont les tumeurs présentaient peu de SNPH avaient tendance à avoir une survie plus mauvaise. Dans des lignées cellulaires et des modèles murins, augmenter SNPH réduisait le nombre et la taille des tumeurs hépatiques, tandis qu’un faible SNPH était associé à une dissémination plus agressive. Ces observations suggèrent que la perte de cet « ancrage » mitochondrial est une étape clé qui rend les cellules cancéreuses plus mobiles et plus dangereuses.
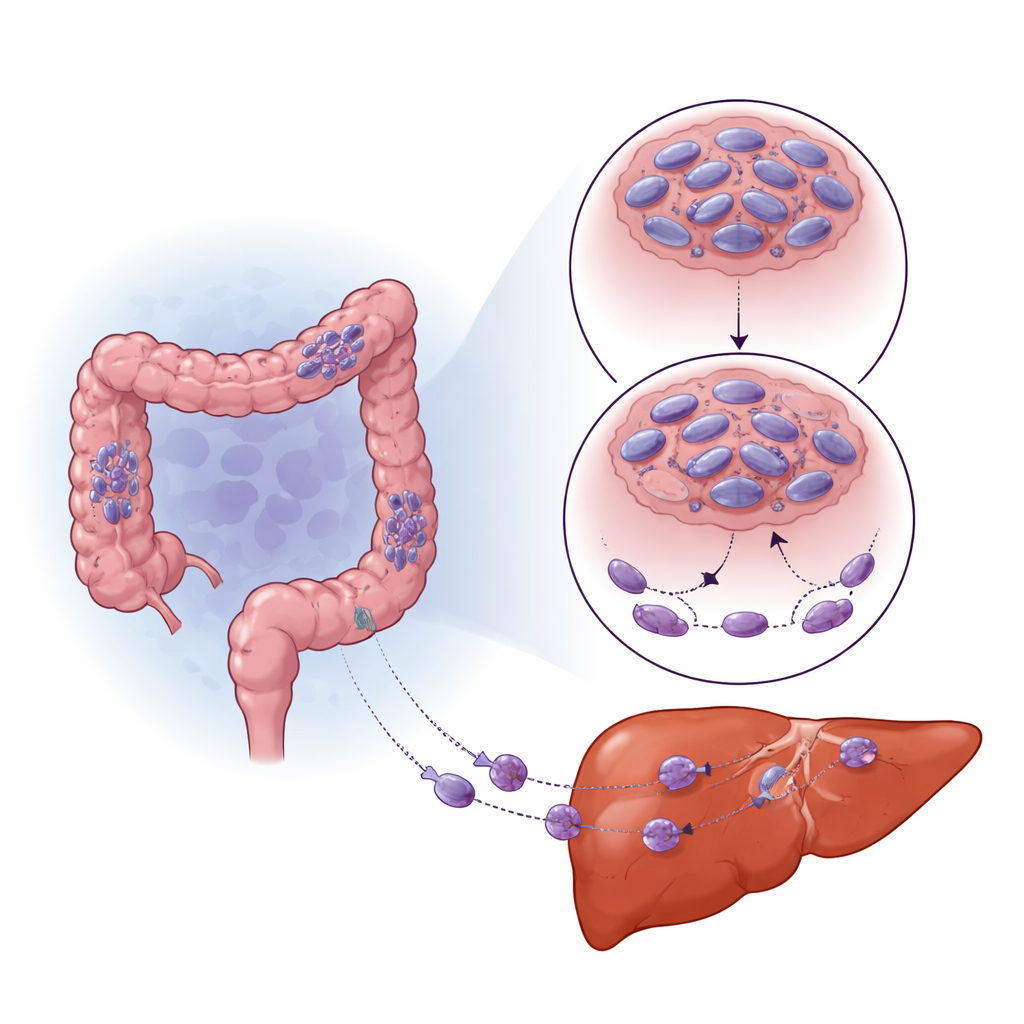
Comment le manque d’oxygène reprogramme le comportement tumoral
Les tumeurs solides dépassent souvent leur apport sanguin, créant des zones pauvrement oxygénées (hypoxie). Les cellules détectent cela via un interrupteur maître, la protéine HIF-1α, qui les aide à s’adapter et à survivre. L’équipe a observé que les zones des tumeurs colorectales et des métastases hépatiques présentant une forte expression de HIF-1α affichaient particulièrement peu de SNPH. Lorsqu’ils ont cultivé des cellules cancéreuses en conditions de faible oxygénation en laboratoire, les niveaux de SNPH chutaient rapidement au fil du temps et les cellules devenaient plus mobiles et invasives. Bloquer HIF-1α restaurait en partie les niveaux de SNPH et réduisait cette augmentation de mobilité. Plutôt que d’éteindre directement SNPH, HIF-1α augmentait un petit ARN régulateur, miR-130a-3p, qui se liait au message de SNPH et empêchait sa traduction. Inhiber miR-130a-3p protégeait SNPH, limitait la formation de fins « doigts » cellulaires et réduisait l’invasion, même en condition d’hypoxie.
Des centrales énergétiques aux « grappins »
La perte de SNPH ne faisait pas que libérer le déplacement des mitochondries. En conditions normales, les mitochondries sont allongées et regroupées, mais lorsque SNPH était réduit, elles se fragmentaient et migraient vers la périphérie cellulaire. Cette réorganisation augmentait la production d’espèces réactives de l’oxygène (ROS), sous-produits chimiques réactifs du métabolisme. Ces ROS activaient une chaîne de signalisation centrée sur les protéines AKT et cdc42, qui à leur tour activaient des effecteurs en aval tels que PAK1 et la cofiline. L’effet combiné remodelait le cytosquelette d’actine — l’armature interne de la cellule — favorisant de longues protrusions fines appelées filopodes. Ces structures fonctionnent comme des grappins, aidant les cellules à se propulser et à se frayer un chemin à travers les tissus environnants. Traiter les cellules avec des piégeurs de ROS atténuait cette signalisation et réduisait la formation de filopodes, tandis qu’ajouter des analogues de ROS augmentait les filopodes, sauf si SNPH était rétabli.
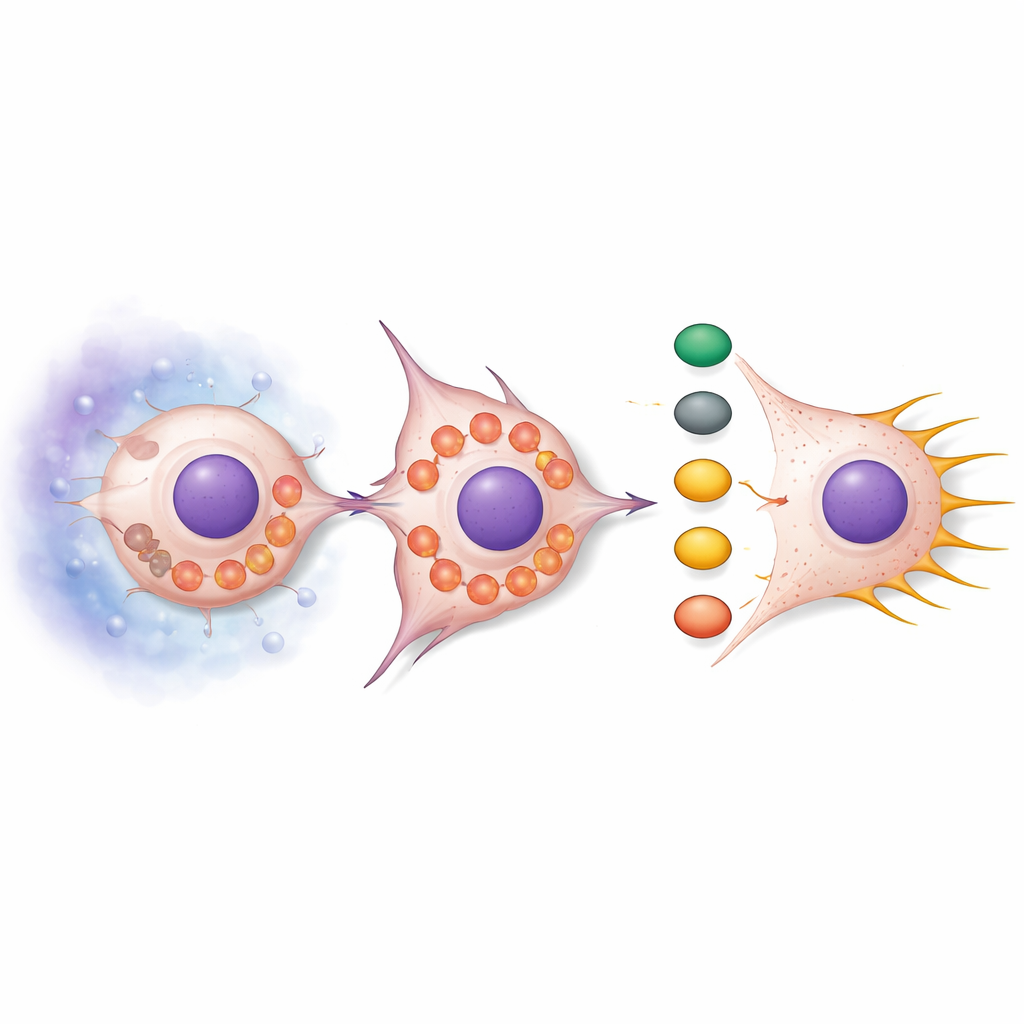
Tester le mécanisme chez l’animal vivant
Pour vérifier si cette voie affecte réellement la dissémination vers le foie, les chercheurs ont injecté des cellules de cancer colorectal avec ou sans surexpression de SNPH chez des souris. Les animaux recevant des cellules riches en SNPH développaient beaucoup moins de tumeurs hépatiques et plus petites, bien que le taux de croissance global des cellules cancéreuses soit comparable. L’examen microscopique des métastases hépatiques montrait que les tumeurs surexprimant SNPH présentaient des mitochondries plus longues et plus fusionnées, des niveaux plus faibles de HIF-1α et une activation moindre du bras PAK1/Cofilin de la cascade de signalisation. En d’autres termes, restaurer cet « ancrage » mitochondrial modifiait à la fois la morphologie mitochondriale et le réseau de signalisation chimique vers un état moins mobile, rendant plus difficile pour les cellules cancéreuses de coloniser le foie.
Ce que cela signifie pour les patients
En résumé, cette étude révèle une réaction en chaîne : la faible oxygénation active HIF-1α, qui induit miR-130a-3p, lequel silencie SNPH. Sans SNPH, les mitochondries se fragmentent et migrent vers le bord cellulaire, générant davantage de ROS qui activent une voie de signalisation favorisant le mouvement. Cela remodèle ensuite la surface cellulaire en filopodes qui aident les cellules du cancer colorectal à migrer et à coloniser le foie. Cibler n’importe quelle étape de cette chaîne — HIF-1α, miR-130a-3p, la production de ROS ou les étapes de signalisation en aval — pourrait offrir de nouvelles stratégies pour prévenir ou limiter les métastases hépatiques, et SNPH lui‑même pourrait servir de marqueur utile de la propension d’un cancer à se disséminer.
Citation: Zhan, L., Li, X., Li, X. et al. HIF-1α suppresses SNPH expression to facilitate liver metastasis of colorectal cancer through regulating mitochondrial dynamics and filopodia formation. Cell Death Dis 17, 380 (2026). https://doi.org/10.1038/s41419-026-08551-1
Mots-clés: métastases du cancer colorectal, dynamique mitochondriale, hypoxie HIF-1α, microARN-130a-3p, espèces réactives de l'oxygène