Clear Sky Science · es
HIF-1α suprime la expresión de SNPH para facilitar la metástasis hepática del cáncer colorrectal regulando la dinámica mitocondrial y la formación de filopodios
Por qué importa esta investigación
El cáncer colorrectal es frecuente y aproximadamente la mitad de los pacientes acaba desarrollando tumores en el hígado, que son difíciles de tratar y a menudo letales. Este estudio se adentra en las pequeñas centrales energéticas de las células cancerosas —las mitocondrias— para entender cómo los cambios en su comportamiento ayudan a las células tumorales a desprenderse del intestino, viajar por el organismo y establecerse en el hígado. Al descubrir un sistema de control oculto que conecta la baja oxigenación, la maquinaria energética y el movimiento celular, el trabajo apunta a nuevas maneras de ralentizar o bloquear la diseminación del cáncer colorrectal.
Un agente de tráfico celular desaparece
Los investigadores se centraron en una proteína llamada sintafinal (SNPH), que actúa como un agente de tráfico para las mitocondrias, ayudando a mantenerlas ancladas y fusionadas. Al explorar grandes bases de datos genéticos públicas y analizar muestras de pacientes, hallaron que los niveles de SNPH son más altos en el tejido sano adyacente, más bajos en los tumores colorrectales primarios y mínimos en las metástasis hepáticas. Los pacientes cuyos tumores presentaban poca SNPH tendían a tener una supervivencia peor. En líneas celulares y modelos de ratón, aumentar SNPH redujo el número y el tamaño de los tumores hepáticos, mientras que la baja expresión de SNPH se asoció con una diseminación más agresiva. Estos patrones sugieren que la pérdida de este “ancla” mitocondrial es un paso clave para que las células cancerosas se vuelvan más móviles y peligrosas.
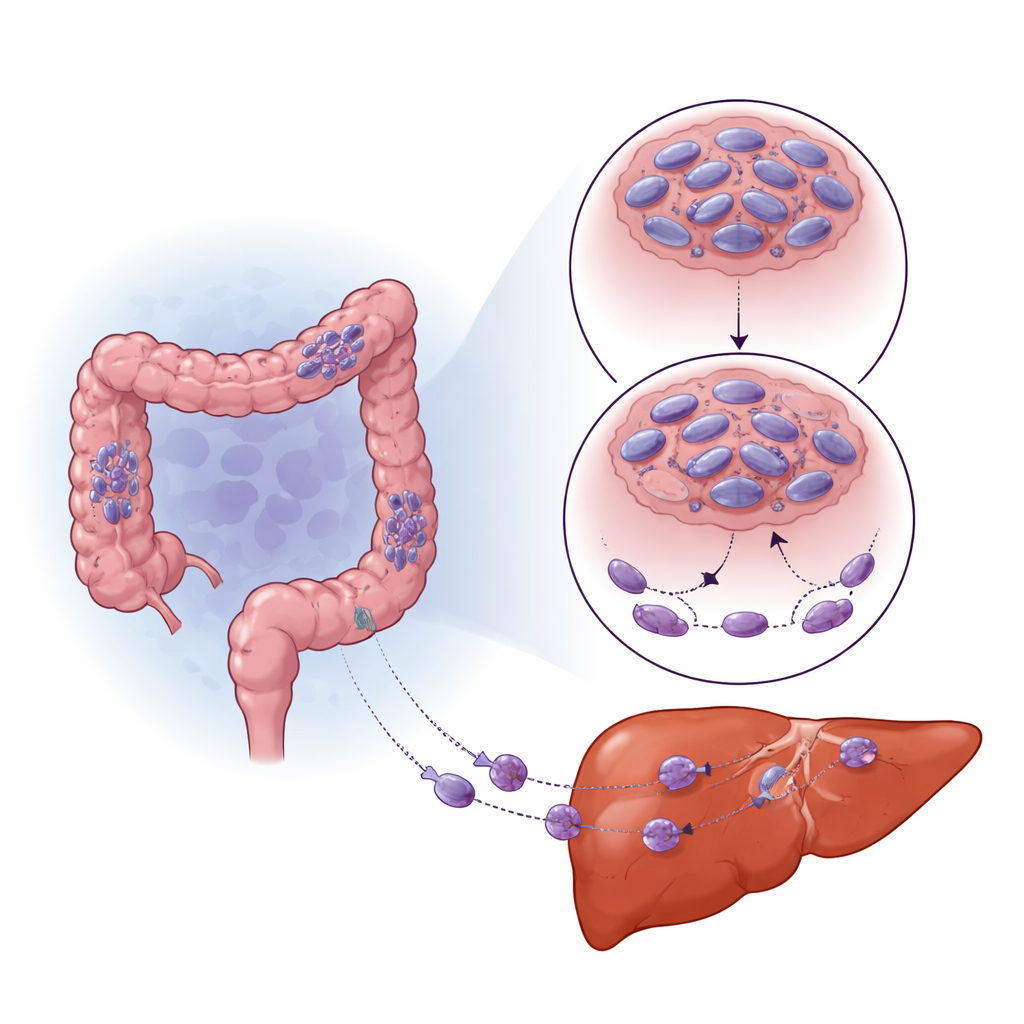
Cómo la baja oxigenación reconfigura el comportamiento tumoral
Los tumores sólidos a menudo crecen más rápido que su suministro sanguíneo, creando zonas de baja oxigenación (hipoxia). Las células lo perciben mediante una proteína reguladora maestra llamada HIF-1α, que les ayuda a adaptarse y sobrevivir. El equipo observó que las áreas de tumores colorrectales y de metástasis hepáticas con alto HIF-1α tenían niveles especialmente bajos de SNPH. Cuando cultivaron células cancerosas en condiciones de poca oxigenación en el laboratorio, los niveles de SNPH cayeron drásticamente con el tiempo y las células se hicieron más móviles e invasivas. Bloquear HIF-1α rescató en parte los niveles de SNPH y redujo este aumento de movilidad. En lugar de apagar SNPH directamente, HIF-1α aumentó un pequeño ARN regulador, miR-130a-3p, que luego se unió al mensajero de SNPH e impidió su traducción. Inhibir miR-130a-3p protegió a SNPH, frenó el crecimiento de las delgadas “yemas” celulares y redujo la invasión, incluso en condiciones de baja oxigenación.
De las centrales energéticas a los “garfios”
La pérdida de SNPH hizo más que liberar a las mitocondrias para que se movieran. En condiciones normales, las mitocondrias suelen ser alargadas y agrupadas, pero cuando SNPH se redujo se fragmentaron y desplazaron hacia el borde celular. Esta reorganización aumentó la producción de especies reactivas de oxígeno (ROS), subproductos químicamente reactivos del metabolismo. Estas ROS activaron una cadena de señalización centrada en las proteínas AKT y cdc42, que a su vez activaron a socios aguas abajo como PAK1 y Cofilina. El efecto combinado fue una remodelación del andamiaje de actina —el esqueleto interno de la célula— que promovió protrusiones largas y delgadas llamadas filopodios. Estas estructuras actúan como garfios, ayudando a las células a avanzar y a abrirse paso a través del tejido circundante. Tratar las células con captadores de ROS atenuó esta señalización y redujo los filopodios, mientras que añadir miméticos de ROS incrementó los filopodios salvo cuando SNPH fue restaurado.
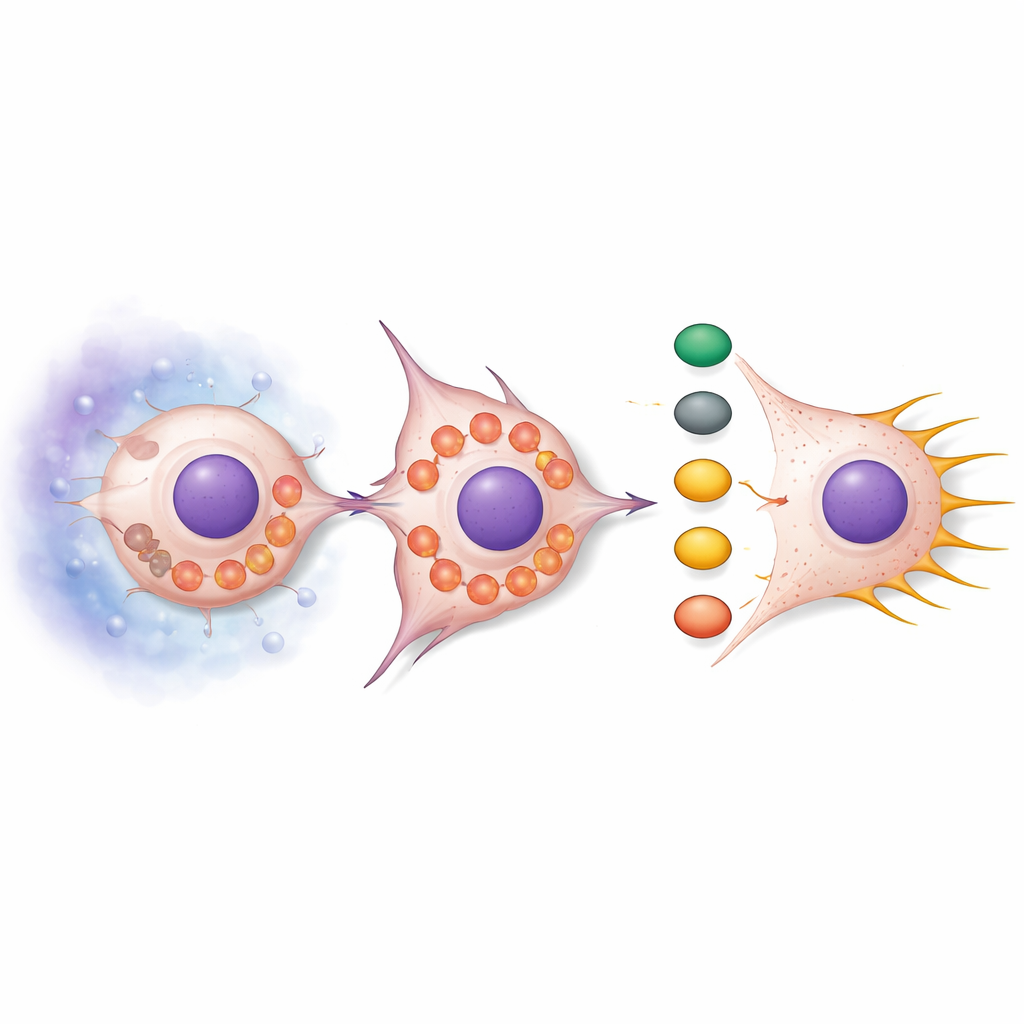
Poner a prueba el mecanismo en animales vivos
Para comprobar si esta vía afecta realmente la diseminación hacia el hígado, los investigadores inyectaron en ratones células de cáncer colorrectal con o sin exceso de SNPH. Los animales que recibieron células ricas en SNPH desarrollaron muchos menos y más pequeños tumores hepáticos, pese a que la tasa de crecimiento general de las células cancerosas fue similar. La microscopía de las metástasis hepáticas mostró que los tumores que sobreexpresaban SNPH tenían mitocondrias más largas y fusionadas, niveles más bajos de HIF-1α y una activación menor del brazo PAK1/Cofilina de la cascada señalizadora. En otras palabras, restaurar el “ancla” mitocondrial desplazó tanto la morfología mitocondrial como la red de señalización química hacia un estado menos móvil, dificultando que las células cancerosas colonizaran el hígado.
Qué significa para los pacientes
En pocas palabras, este estudio revela una reacción en cadena: la baja oxigenación en los tumores activa HIF-1α, que induce miR-130a-3p, el cual silencia SNPH. Sin SNPH, las mitocondrias se fragmentan y se desplazan al borde celular, generando más ROS que activan una vía de señalización promotora del movimiento. Eso, a su vez, remodela la superficie celular en filopodios que ayudan a las células del cáncer colorrectal a migrar y sembrar el hígado. Apuntar a cualquiera de los eslabones de esta cadena —HIF-1α, miR-130a-3p, la producción de ROS o los pasos señalizadores posteriores— podría ofrecer nuevas estrategias para prevenir o limitar la metástasis hepática, y SNPH mismo puede servir como un marcador útil de la probabilidad de que el cáncer de un paciente se disemine.
Cita: Zhan, L., Li, X., Li, X. et al. HIF-1α suppresses SNPH expression to facilitate liver metastasis of colorectal cancer through regulating mitochondrial dynamics and filopodia formation. Cell Death Dis 17, 380 (2026). https://doi.org/10.1038/s41419-026-08551-1
Palabras clave: metástasis del cáncer colorrectal, dinámica mitocondrial, hipoxia HIF-1α, microARN-130a-3p, especies reactivas de oxígeno