Clear Sky Science · zh
APOE4通过线粒体功能障碍加剧糖皮质激素应激激素诱导的tau病理
为何应激与记忆相关基因对我们都很重要
许多人担心长期应激会增加日后出现记忆问题的风险。与此同时,一种常见的基因变体APOE4已知会显著提高阿尔茨海默病的风险。本研究将这两条线索结合起来,探讨应激激素与APOE4在脑细胞内如何相互作用,以及这种相互作用是否可能指向保护老化大脑的新途径。
常见风险基因如何遇上日常应激
研究者聚焦于APOE4,这是一种参与胆固醇处理的蛋白质变体,全球数百万人携带。团队将这一遗传背景与糖皮质激素暴露相结合,糖皮质激素是慢性心理压力下释放的主要应激激素。他们使用被改造以携带人类APOE3(更中性的版本)或APOE4的小鼠,以及来源于这些小鼠大脑的神经细胞,聚焦到海马体——一个对压力和阿尔茨海默病都特别敏感的记忆中枢。研究目标是观察APOE4是否使这些神经元更易受到应激激素的有害影响。
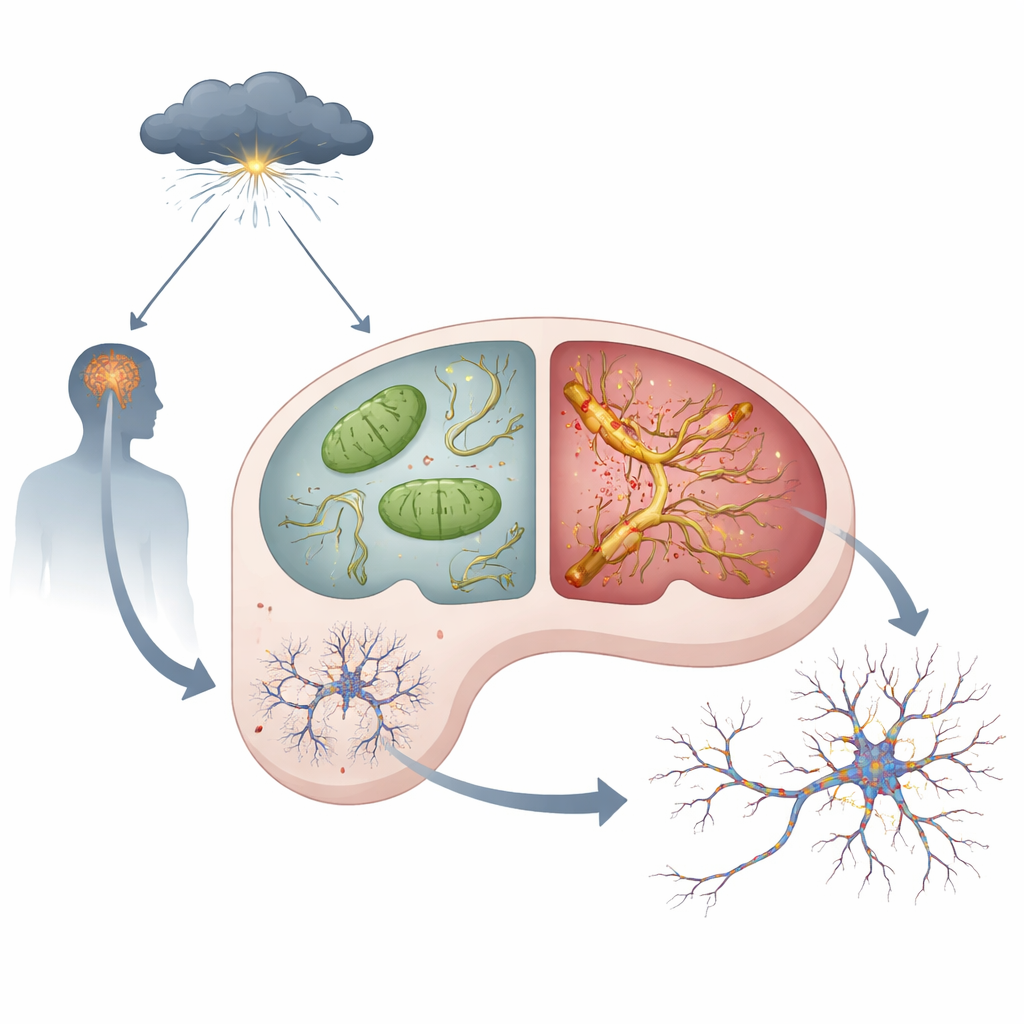
应激激素、失灵的“发电厂”和有毒的tau
每个神经元内都有线粒体,这些微小的“发电厂”为思考和记忆提供能量。研究团队发现,即便在平静条件下,APOE4小鼠在海马中就显示出线粒体方面的问题:更多的活性氧副产物、关键能量生成复合体活性减弱以及ATP(细胞能量货币)含量降低。当动物接受模拟慢性应激的合成糖皮质激素高剂量处理时,这些问题在APOE4小鼠中比在APOE3小鼠中更为严重。与此同时,一种叫tau的蛋白——通常帮助稳定细胞内“轨道”——开始积累、过度修饰、聚集并在神经元之间传播。这些通常称为tau病理的变化,在暴露于应激激素的APOE4大脑中更强且传播更广。
在脆弱大脑中过度活跃的应激信号
研究还检视了脑细胞对压力信号的反应强度。糖皮质激素通过本来位于细胞质中的受体发挥作用,受体被激活后会转入细胞核和线粒体。在APOE4小鼠中,这些受体在基线时就已更活跃,并更容易转移到细胞核和线粒体中,尽管血液中整体激素水平与APOE3动物相似。支持这一点的是,APOE4动物和神经元显示出促进受体激活的辅助手蛋白水平更高,以及与更强应激激素信号一致的基因表达模式。在细胞培养中,极低剂量的应激激素——对APOE3神经元几乎无影响——就足以损害APOE4神经元的线粒体并触发tau的积累与释放,表明这种遗传背景降低了应激相关损伤的阈值。
线粒体中的关键孔道与可能的干预方式
进一步深入研究时,研究者锁定了线粒体通透性转换孔(mPTP),这是可能在内线粒体膜上打开的通道。该孔一旦打开,线粒体会失去电位、排放有害的反应性分子,并可能推动细胞走向功能障碍。在APOE4神经元中,即便适度的应激激素暴露也足以提高环孢素D(cyclophilin D,一种关键孔道调节蛋白)的水平并触发孔道开放。用两种不同药物阻断该孔——一种直接干扰环孢素D,另一种降低线粒体氧化物产生(mito-apocynin)——可保护APOE4神经元免受能量丧失、过量活性分子和tau改变的侵害。
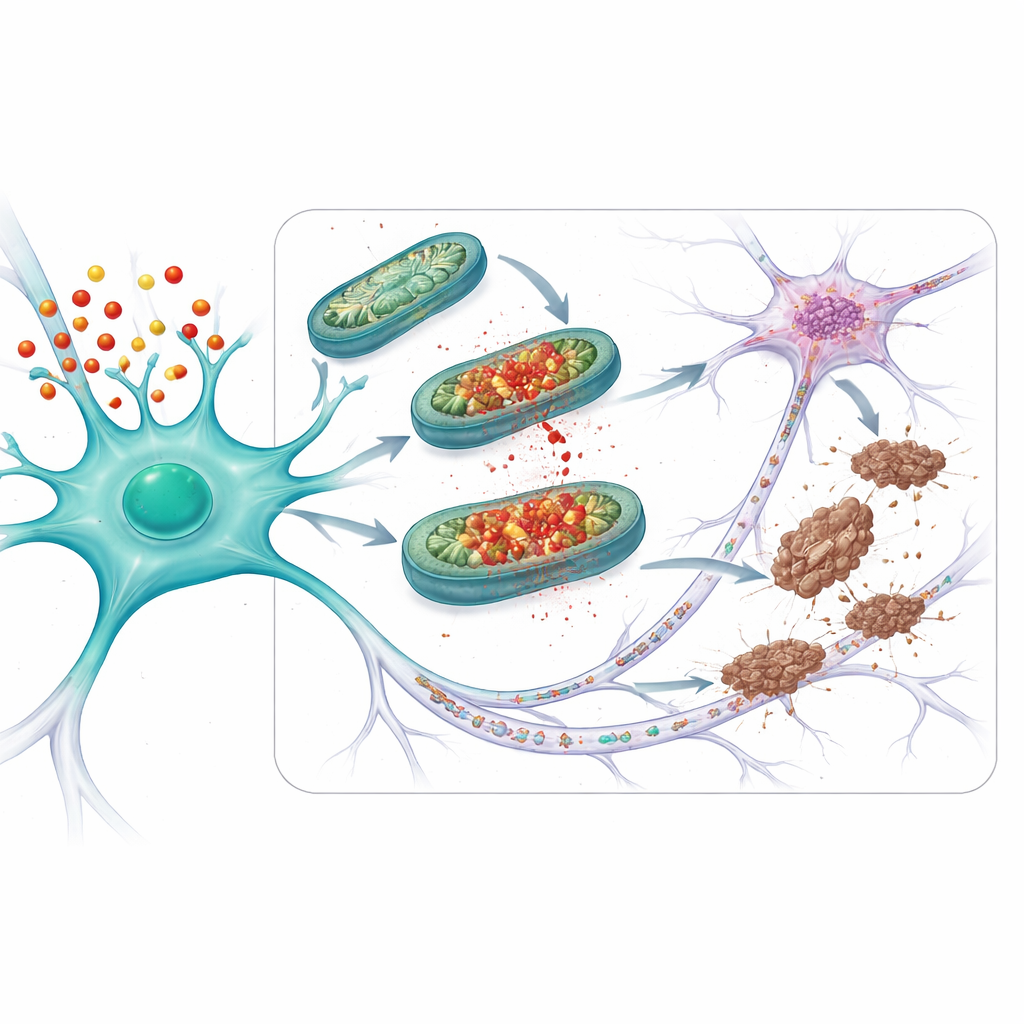
保护突触和老化大脑
接着,团队询问这种保护策略在更类似疾病的情境中是否有效。他们研究了不仅携带APOE4且还产生易形成缠结的突变型tau的小鼠。在这些动物中,线粒体问题、异常tau和突触——神经元之间的连接点——的丧失都比携带较安全APOE3版本的小鼠更为严重。对APOE4小鼠进行mito-apocynin治疗,从明显症状出现之前开始,可减少线粒体损伤、tau改变和突触丧失。在自然出现tau问题的年长APOE4小鼠(即使没有额外加入突变tau)中,短期的mito-apocynin治疗同样恢复了线粒体功能、减少了异常tau并限制了tau在神经元间的传播范围。
这对有风险的人意味着什么
简单来说,这项工作表明APOE4使脑细胞的“发电厂”更脆弱、应激响应开关更容易被触发。当慢性应激激素加入后,这种组合会加速从线粒体损伤到有毒tau积累、传播及脑连接丧失的级联过程。关键是,研究显示阻断一个特定的线粒体孔道可以在APOE4模型中中断这一级联反应。尽管在任何治疗进入临床之前还需大量工作,但以该孔道为靶点——以及对携带APOE4者特别注意管理慢性应激——可能成为未来减缓或预防阿尔茨海默相关损伤的策略之一。
引用: Yu, Q., Du, F., Puerta-Alvarado, V. et al. APOE4 exacerbates glucocorticoid stress hormone-induced tau pathology via mitochondrial dysfunction. Cell Death Dis 17, 419 (2026). https://doi.org/10.1038/s41419-026-08543-1
关键词: APOE4, 慢性应激, 线粒体, tau病理, 阿尔茨海默病