Clear Sky Science · es
APOE4 agrava la patología tau inducida por la hormona del estrés glucocorticoide a través de la disfunción mitocondrial
Por qué importan a todos el estrés y los genes de la memoria
Mucha gente se preocupa de que periodos prolongados de estrés puedan aumentar sus probabilidades de desarrollar problemas de memoria en el futuro. Al mismo tiempo, una variante genética común llamada APOE4 se sabe que incrementa de forma notable el riesgo de enfermedad de Alzheimer. Este estudio une esos dos hilos, preguntando cómo interactúan las hormonas del estrés y APOE4 dentro de las células cerebrales, y si esa interacción podría señalar nuevas formas de proteger el cerebro envejecido.
Cómo un gen de riesgo común se encuentra con el estrés cotidiano
Los investigadores se centraron en APOE4, una versión de una proteína encargada del manejo del colesterol que portan millones de personas en todo el mundo. Combinando este trasfondo genético con la exposición a glucocorticoides, las principales hormonas del estrés liberadas durante la presión psicológica crónica, utilizaron ratones diseñados para portar APOE3 humano (la versión más neutra) o APOE4, y neuronas cultivadas a partir de sus cerebros, y se fijaron en el hipocampo, un centro de la memoria especialmente sensible tanto al estrés como a la enfermedad de Alzheimer. Su objetivo era ver si APOE4 hace que estas neuronas sean más vulnerables a los efectos nocivos de las hormonas del estrés.
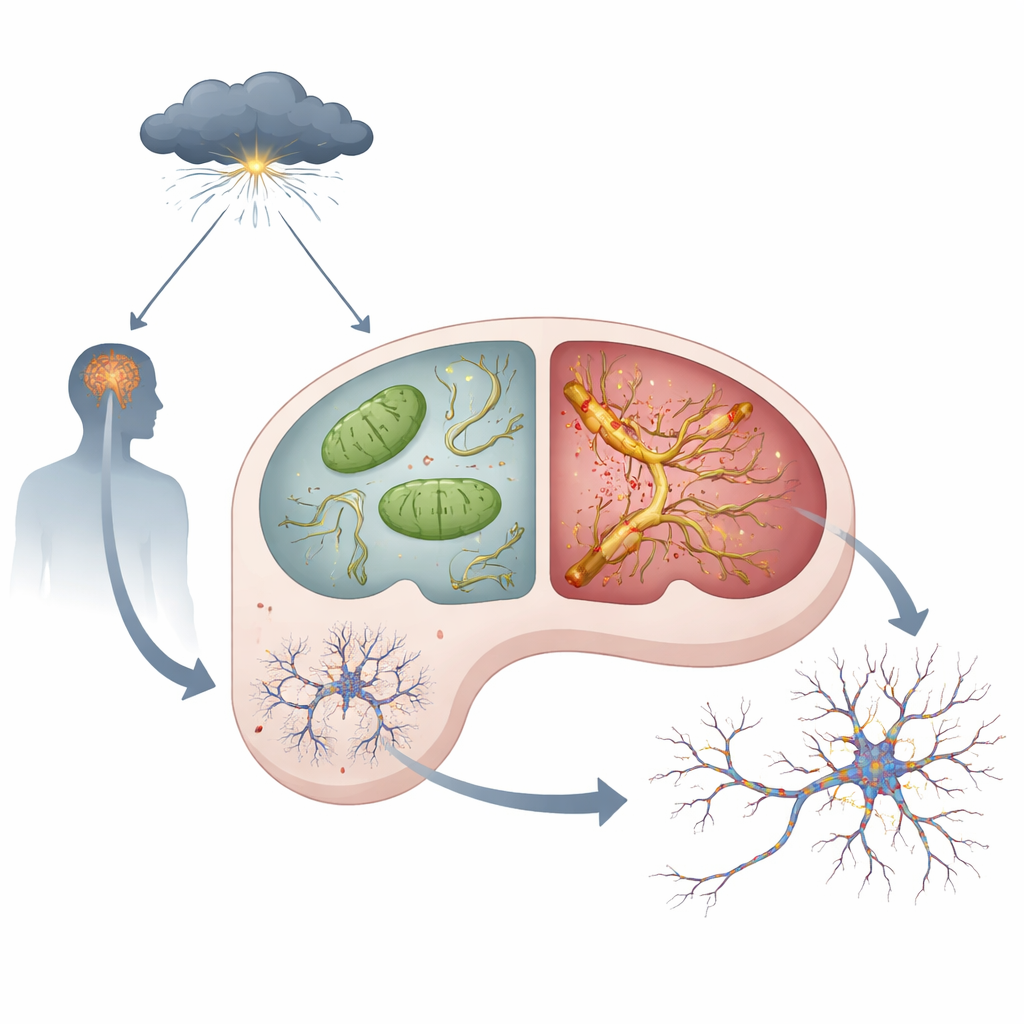
Hormonas del estrés, centrales energéticas defectuosas y tau tóxico
Dentro de cada neurona residen las mitocondrias, pequeñas centrales que generan la energía necesaria para pensar y recordar. El equipo encontró que incluso en condiciones de calma, los ratones APOE4 mostraban signos de problemas mitocondriales en el hipocampo: más subproductos reactivos del oxígeno, menor actividad de un complejo clave productor de energía y niveles reducidos de ATP, la moneda energética de la célula. Cuando los animales fueron tratados con dosis altas de una hormona sintética del estrés que imita el estrés crónico, estos problemas empeoraron en los ratones APOE4 más que en los APOE3. Al mismo tiempo, una proteína llamada tau —que normalmente ayuda a estabilizar las “vías” internas de la célula— comenzó a acumularse, modificarse en exceso, agregarse y propagarse de neurona a neurona. Estos cambios en la tau, a menudo denominados patología tau, fueron mucho más intensos y se extendieron más en cerebros APOE4 expuestos a hormonas del estrés.
Señalización del estrés sobreactivada en cerebros vulnerables
El estudio también examinó cuán intensamente respondían las células cerebrales a las señales de estrés. Los glucocorticoides actúan a través de receptores que normalmente se encuentran en el fluido celular y se trasladan al núcleo y a las mitocondrias cuando se activan. En los ratones APOE4, estos receptores ya estaban más activos en reposo y se movían con mayor facilidad al núcleo y a las mitocondrias, a pesar de que los niveles hormonales en sangre eran similares a los de los animales APOE3. En consonancia con esto, los animales y las neuronas APOE4 mostraron niveles más altos de proteínas auxiliares que favorecen la activación del receptor y patrones de expresión génica compatibles con una señalización por hormonas del estrés más intensa. En cultivos celulares, dosis muy bajas de hormona del estrés que apenas afectaban a las neuronas APOE3 fueron suficientes para dañar mitocondrias y desencadenar acumulación y liberación de tau en neuronas APOE4, lo que demuestra que este trasfondo genético reduce el umbral para el daño relacionado con el estrés.
Un poro crítico en las mitocondrias y una posible forma de intervención
Indagando más, los investigadores se centraron en el poro de transición de permeabilidad mitocondrial (mPTP), un canal que puede abrirse en la membrana interna mitocondrial. Cuando este poro se abre, las mitocondrias pierden su carga eléctrica, bombean moléculas reactivas dañinas y pueden empujar a las células hacia la disfunción. En las neuronas APOE4, incluso una exposición moderada a hormonas del estrés fue suficiente para aumentar los niveles de ciclophilina D, un regulador clave del poro, y para desencadenar la apertura del mismo. Bloquear este poro con dos fármacos diferentes —uno que interfiere directamente con la ciclophilina D y otro que reduce la producción mitocondrial de especies reactivas (mito-apocynin)— protegió a las neuronas APOE4 de la pérdida de energía, del exceso de moléculas reactivas y de los cambios en la tau.
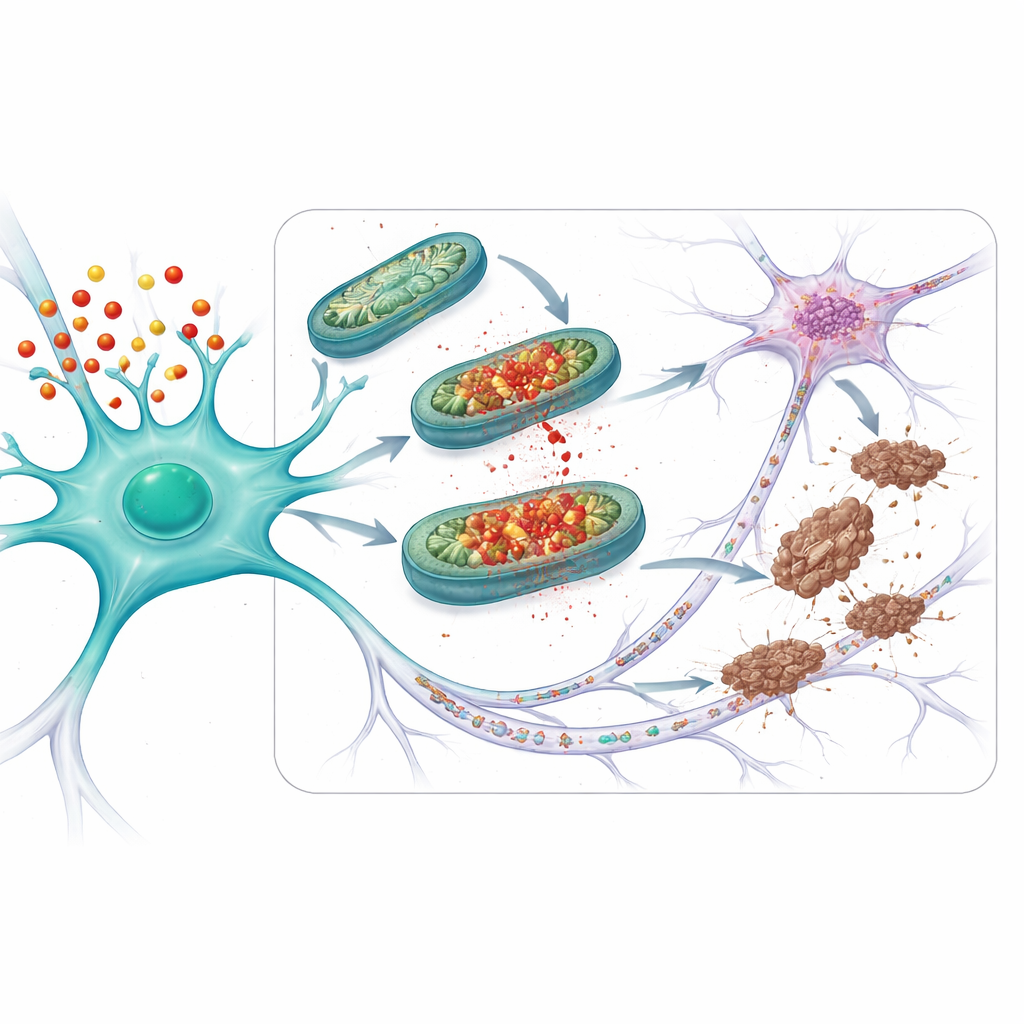
Protegiendo conexiones y cerebros envejecidos
El equipo se preguntó entonces si esta estrategia protectora sería útil en escenarios más parecidos a la enfermedad. Estudiaron ratones que no solo portaban APOE4, sino que además producían una forma mutante de tau que forma enredos con facilidad. En estos animales, los problemas mitocondriales, la tau anormal y la pérdida de sinapsis —los puntos de conexión entre neuronas— fueron todos peores que en ratones con la versión más segura APOE3. Tratar a los ratones APOE4 con mito-apocynin, comenzando antes de que aparecieran síntomas evidentes, redujo el daño mitocondrial, los cambios en la tau y la pérdida de sinapsis. En ratones APOE4 de mayor edad con problemas de tau que surgían de forma natural (incluso sin tau mutante añadida), un tratamiento de corta duración con mito-apocynin restauró de manera similar la función mitocondrial, redujo la tau anómala y limitó la propagación de la tau entre neuronas.
Qué significa esto para las personas en riesgo
En términos sencillos, este trabajo sugiere que APOE4 hace que las centrales energéticas de las células cerebrales sean más frágiles y que sus interruptores de respuesta al estrés se activen con mayor facilidad. Cuando se suman hormonas del estrés crónico, esta combinación acelera la cascada que va del daño mitocondrial a la acumulación tóxica de tau, su propagación y la pérdida de conexiones cerebrales. De forma crucial, el estudio muestra que bloquear un poro mitocondrial específico puede interrumpir esta cascada en modelos APOE4. Aunque hace falta mucha más investigación antes de que cualquier tratamiento llegue a los pacientes, dirigir este poro —y manejar el estrés crónico, especialmente en portadores de APOE4— podría formar parte de futuras estrategias para frenar o prevenir el daño relacionado con el Alzheimer.
Cita: Yu, Q., Du, F., Puerta-Alvarado, V. et al. APOE4 exacerbates glucocorticoid stress hormone-induced tau pathology via mitochondrial dysfunction. Cell Death Dis 17, 419 (2026). https://doi.org/10.1038/s41419-026-08543-1
Palabras clave: APOE4, estrés crónico, mitocondrias, patología tau, enfermedad de Alzheimer