Clear Sky Science · pl
APOE4 nasila patologię tau wywołaną glukokortykoidowymi hormonami stresu poprzez dysfunkcję mitochondriów
Dlaczego stres i geny pamięci dotyczą nas wszystkich
Wiele osób obawia się, że długotrwały stres może zwiększać ryzyko wystąpienia problemów z pamięcią w późniejszym życiu. Jednocześnie powszechny wariant genetyczny zwany APOE4 jest dobrze znany z silnego podwyższania ryzyka choroby Alzheimera. To badanie łączy te dwa wątki, pytając, jak hormony stresu i APOE4 wchodzą w interakcje wewnątrz komórek mózgu i czy ta interakcja może wskazywać nowe sposoby ochrony starzejącego się mózgu.
Jak powszechny gen ryzyka spotyka codzienny stres
Naukowcy skupili się na APOE4, wersji białka zaangażowanego w gospodarkę cholesterolu, którą noszą miliony ludzi na świecie. Połączyli ten wariant genetyczny z ekspozycją na glukokortykoidy — główne hormony stresu uwalniane podczas przewlekłego napięcia psychicznego. Używając myszy zaprojektowanych tak, by niosły ludzkie APOE3 (wariant bardziej obojętny) lub APOE4, oraz neuronów hodowanych z ich mózgów, przyjrzeli się hipokampowi — ośrodkowi pamięci szczególnie wrażliwemu zarówno na stres, jak i chorobę Alzheimera. Celem było sprawdzenie, czy APOE4 czyni te neurony bardziej podatnymi na szkodliwe działanie hormonów stresu.
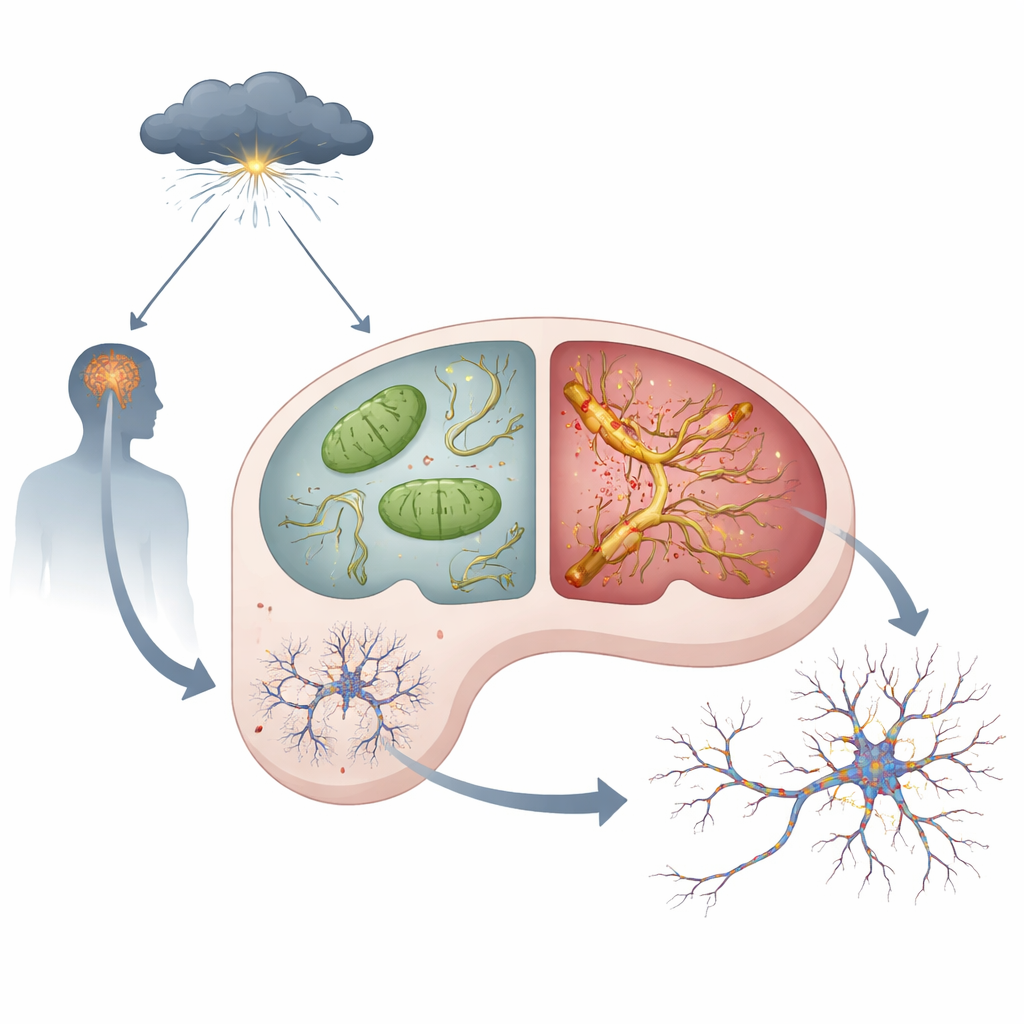
Hormony stresu, wadliwe elektrownie i toksyczna tau
W każdym neuronie znajdują się mitochondria — maleńkie elektrownie wytwarzające energię potrzebną do myślenia i zapamiętywania. Zespół stwierdził, że nawet w warunkach spokoju myszy z APOE4 wykazywały oznaki problemów mitochondrialnych w hipokampie: więcej reaktywnych produktów ubocznych tlenu, słabszą aktywność kluczowego kompleksu odpowiedzialnego za produkcję energii oraz niższe poziomy ATP — waluty energetycznej komórki. Kiedy zwierzęta otrzymały duże dawki syntetycznego hormonu stresu naśladującego przewlekły stres, problemy te pogłębiły się u myszy APOE4 bardziej niż u myszy APOE3. Równocześnie białko zwane tau — które normalnie stabilizuje „tory” wewnątrzkomórkowe — zaczęło się gromadzić, nadmiernie modyfikować, zlepiać i rozprzestrzeniać z neuronu na neuron. Te zmiany tau, określane często jako patologia tau, były znacznie silniejsze i rozprzestrzeniały się dalej w mózgach APOE4 poddanych działaniu hormonów stresu.
Nadmierna aktywacja sygnalizacji stresowej w podatnych mózgach
Badanie zbadało też, jak silnie komórki mózgowe reagują na sygnały stresowe. Glukokortykoidy działają przez receptory, które zwykle znajdują się w płynie komórkowym i po aktywacji przemieszczają się do jądra oraz mitochondriów. U myszy APOE4 te receptory były już bardziej aktywne w warunkach wyjściowych i łatwiej przemieszczały się do jądra i mitochondriów, mimo że ogólne poziomy hormonów we krwi były podobne do zwierząt z APOE3. Potwierdza to fakt, że zwierzęta i neurony APOE4 wykazywały wyższe poziomy białek pomocniczych sprzyjających aktywacji receptorów oraz wzorce ekspresji genów zgodne z silniejszą sygnalizacją hormonów stresu. W hodowlach komórkowych bardzo niskie dawki hormonu stresu, które miały niewielki wpływ na neurony APOE3, wystarczyły, by uszkodzić mitochondria oraz wywołać gromadzenie się i uwalnianie tau w neuronach APOE4, co pokazuje, że ten profil genetyczny obniża próg szkodliwego działania stresu.
Krytyczny por w mitochondriach i możliwa droga interwencji
Zagłębiając się dalej, badacze skupili się na mitochondrialnym porze przejściowym (mPTP) — kanale, który może się otwierać w wewnętrznej błonie mitochondrialnej. Gdy por ten się otwiera, mitochondria tracą ładunek elektryczny, pompują na zewnątrz szkodliwe reaktywne cząsteczki i mogą popychać komórki w kierunku dysfunkcji. W neuronach APOE4 już umiarkowana ekspozycja na hormony stresu wystarczała, by zwiększyć poziomy cyklofiliny D — kluczowego regulatora poru — i wywołać jego otwarcie. Zablokowanie tego poru dwoma różnymi lekami — jednym bezpośrednio ingerującym w cyklofilinę D, a drugim tłumiącym produkcję mitochondrialnych oksydantów (mito-apocyryna) — chroniło neurony APOE4 przed utratą energii, nadmiarem reaktywnych cząsteczek i zmianami tau.
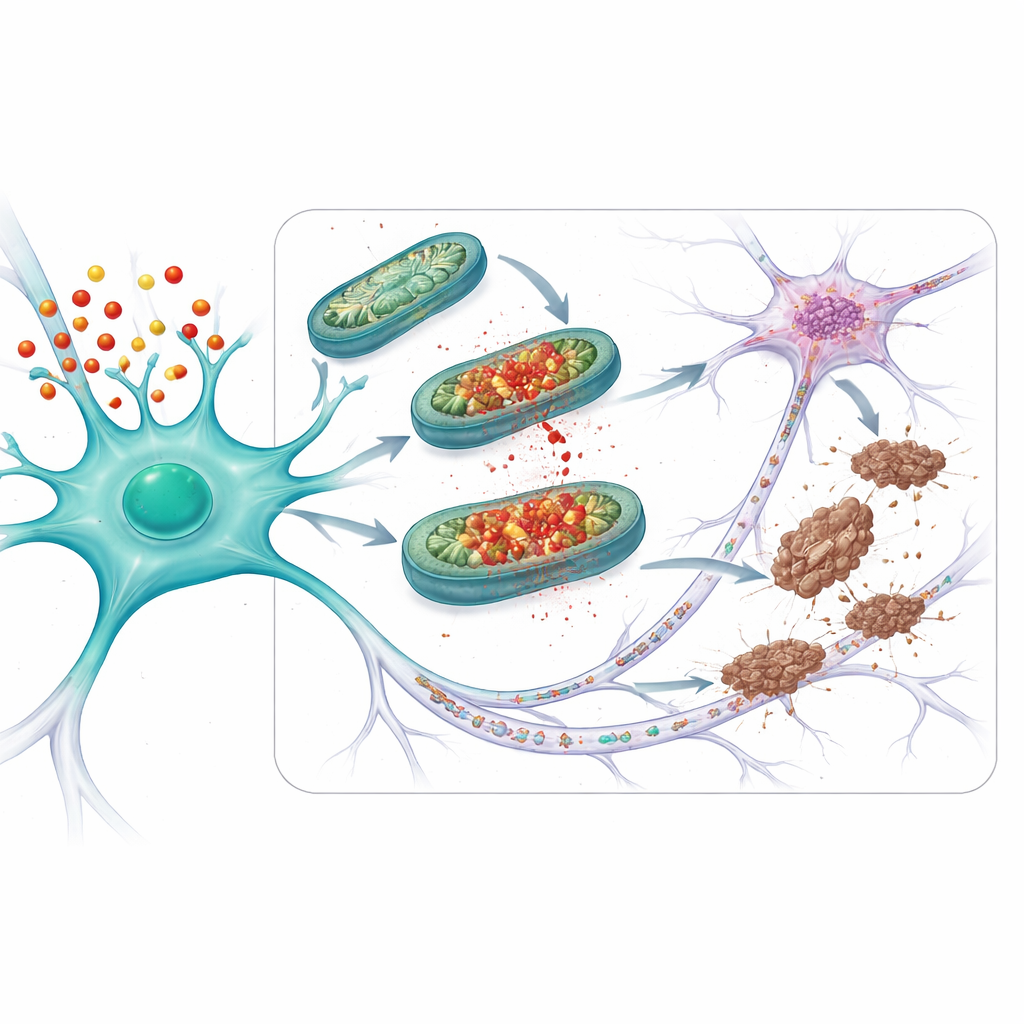
Ochrona połączeń i starzejących się mózgów
Zespół zapytał następnie, czy ta strategia ochronna zadziała w warunkach bardziej przypominających chorobę. Badali myszy, które nie tylko niosły APOE4, ale też produkowały zmutowaną formę tau, która łatwo tworzy splątania. U tych zwierząt problemy mitochondrialne, nieprawidłowa tau i utrata synaps — miejsc połączeń między neuronami — były gorsze niż u myszy z bezpieczniejszą wersją APOE3. Leczenie myszy APOE4 mito-apocyryną, rozpoczęte zanim pojawiły się oczywiste objawy, zmniejszało uszkodzenia mitochondriów, zmiany tau i utratę synaps. U starszych myszy APOE4 z naturalnie pojawiającymi się problemami z tau (nawet bez dodatkowej zmutowanej tau) krótkotrwałe leczenie mito-apocyryną podobnie przywróciło funkcję mitochondrialną, zmniejszyło nieprawidłową tau i ograniczyło zasięg rozprzestrzeniania się tau między neuronami.
Co to znaczy dla osób zagrożonych
W prostych słowach, praca ta sugeruje, że APOE4 powoduje, iż „elektrownie” komórek mózgowych są bardziej kruche, a przełączniki reakcji na stres łatwiej ulegają aktywacji. Gdy dołożymy do tego przewlekłe hormony stresu, kombinacja ta przyspiesza kaskadę prowadzącą od uszkodzenia mitochondriów do toksycznego nagromadzenia tau, jego rozprzestrzeniania się i utraty połączeń mózgowych. Co istotne, badanie pokazuje, że zablokowanie konkretnego mitochondrialnego poru może przerwać tę kaskadę w modelach APOE4. Choć przed wprowadzeniem jakiegokolwiek leczenia u pacjentów potrzebne są jeszcze liczne badania, ukierunkowanie na ten por — oraz zarządzanie przewlekłym stresem, szczególnie u nosicieli APOE4 — może stać się częścią przyszłych strategii spowalniania lub zapobiegania uszkodzeniom związanym z chorobą Alzheimera.
Cytowanie: Yu, Q., Du, F., Puerta-Alvarado, V. et al. APOE4 exacerbates glucocorticoid stress hormone-induced tau pathology via mitochondrial dysfunction. Cell Death Dis 17, 419 (2026). https://doi.org/10.1038/s41419-026-08543-1
Słowa kluczowe: APOE4, przewlekły stres, mitochondria, patologia tau, choroba Alzheimera