Clear Sky Science · ar
APOE4 يزيد من تفاقم اعتلال تاو الناتج عن هرمونات الإجهاد الجلوكوكورتيكويدية عبر خلل الميتوكوندريا
لماذا تهمنا جينات الضغط والذاكرة جميعًا
يخشى كثير من الناس أن فترات طويلة من التوتر قد تزيد من احتمال تعرضهم لمشاكل في الذاكرة لاحقًا. وفي الوقت نفسه، من المعروف أن متغيّرًا شائعًا في الجين يدعى APOE4 يزيد بشكل قوي من خطر الإصابة بمرض الزهايمر. تجمع هذه الدراسة هذين الخيطين معًا، مستفسرةً كيف تتفاعل هرمونات الإجهاد وAPOE4 داخل خلايا الدماغ، وما إذا كانت هذه التفاعلات تشير إلى طرق جديدة لحماية الدماغ المسن.
كيف يلتقي جين شائع للخطورة مع ضغوط الحياة اليومية
تركز الباحثون على APOE4، نسخة من بروتين يتعامل مع الكوليسترول ويحمله ملايين الأشخاص حول العالم. جمعوا هذا الخلفية الجينية مع التعرض للجلوكوكورتيكويدات، وهي الهرمونات الرئيسية للإجهاد التي تُفرز أثناء الضغط النفسي المزمن. باستخدام فئران مهندسة لتحمل APOE3 البشري (النسخة الأكثر حيادية) أو APOE4، وخلايا عصبية نمت من أدمغتها، ركزوا على الحُصين، مركز الذاكرة الحساس بشكل خاص لكل من الإجهاد ومرض الزهايمر. كان هدفهم معرفة ما إذا كانت APOE4 تجعل هذه الخلايا العصبية أكثر عرضة للتأثيرات الضارة لهرمونات الإجهاد.
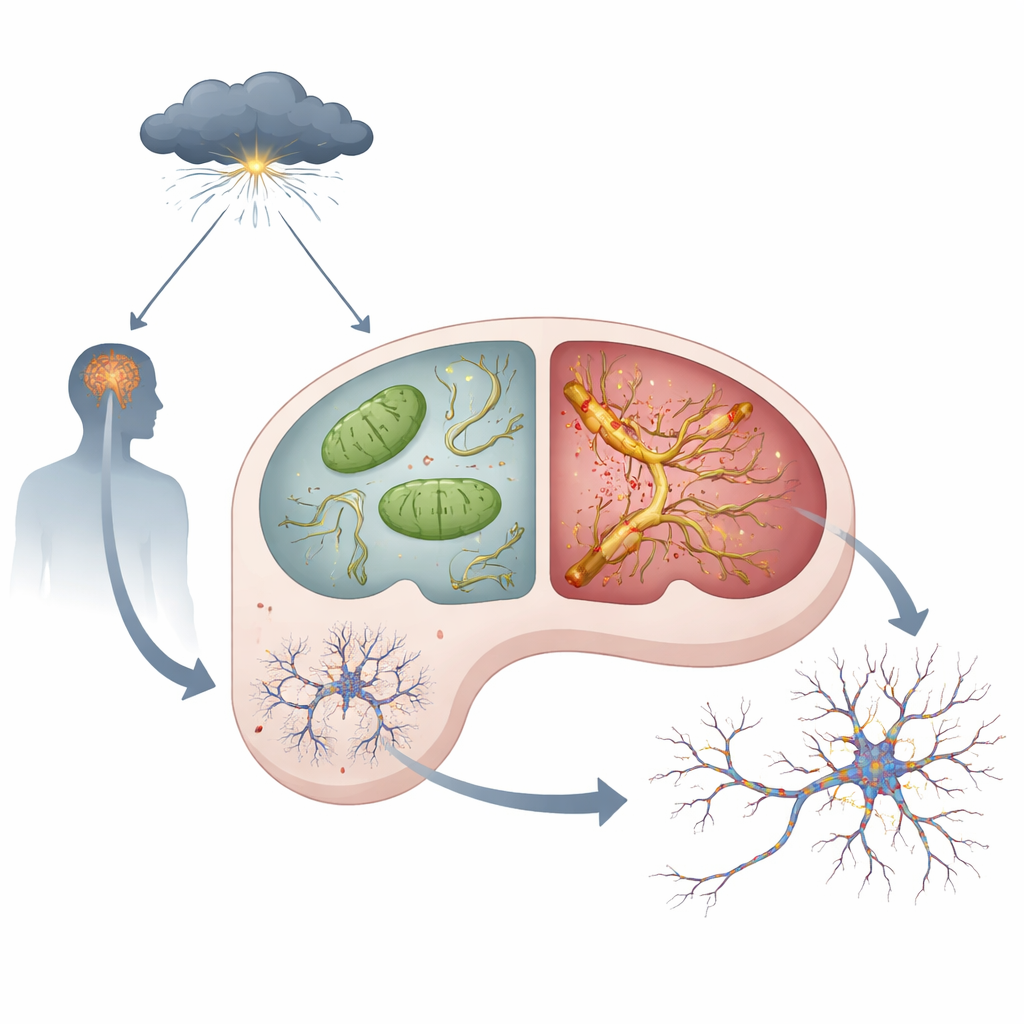
هرمونات الإجهاد، محطات طاقة معطوبة، وتاو السام
داخل كل خلية عصبية توجد الميتوكوندريا، محطات طاقة صغرى تولّد الطاقة اللازمة للتفكير والتذكر. وجد الفريق أنه حتى في ظروف الهدوء، أظهرت فئران APOE4 علامات مشاكل ميтоكوندرية في الحُصين: المزيد من نواتج الأكسدة التفاعلية، نشاط أضعف لمجمع حاسم لتوليد الطاقة، ومستويات أقل من ATP، عملة طاقة الخلية. عندما عولجت الحيوانات بجرعات عالية من هرمون إجهاد صناعي يحاكي الإجهاد المزمن، ساءت هذه المشاكل في فئران APOE4 مقارنةً بفئران APOE3. في الوقت نفسه، بدأ بروتين يُدعى تاو — الذي يساعد عادةً في تثبيت «المسارات» الداخلية للخلية — يتراكم، ويخضع لتعديلات مفرطة، ويتكتل، وينتشر من خلية عصبية إلى أخرى. كانت تغيّرات تاو هذه، المعروفة غالبًا باعتلال تاو، أقوى وانتشارها أوسع في أدمغة APOE4 المعرضة لهرمونات الإجهاد.
إشارات إجهاد مفرطة النشاط في أدمغة معرضة
فحصت الدراسة أيضًا مدى استجابة خلايا الدماغ لإشارات الإجهاد. تعمل الجلوكوكورتيكويدات عبر مستقبلات تكون عادة في سيتوبلازم الخلية وتنتقل إلى النواة والميتوكوندريا عند تنشيطها. في فئران APOE4، كانت هذه المستقبلات بالفعل أكثر نشاطًا في الحالة الأساسية وانتقلت بسهولة أكبر إلى النواة والميتوكوندريا، رغم أن مستويات الهرمونات في الدم كانت مشابهة لتلك في حيوانات APOE3. داعمًا لذلك، أظهرت حيوانات وخلايا APOE4 مستويات أعلى من بروتينات مُساعِدة تعزز تنشيط المستقبلات، وأنماط تعبير جيني تتوافق مع إشارات هرمونات إجهاد أقوى. في زراعة الخلايا، كانت جرعات منخفضة جدًا من هرمون الإجهاد التي كان لها أثر ضئيل على خلايا APOE3 كافية لإتلاف الميتوكوندريا وتحفيز تراكم وإفراز تاو في خلايا APOE4، مما يُظهر أن هذه الخلفية الجينية تخفض عتبة الضرر المرتبط بالإجهاد.
مسام حرج في الميتوكوندريا وطريقة محتملة للتدخل
بتعمق أكبر، ركز الباحثون على «المسام النفاذي الانتقالي الميتوكوندري» (mPTP)، قناة يمكن أن تفتح في الغشاء الداخلي للميتوكوندريا. عندما تفتح هذه المسام، تفقد الميتوكوندريا شحنتها الكهربائية، وتضخ نواتج تفاعل ضارة، ويمكن أن تدفع الخلايا نحو الخلل الوظيفي. في خلايا APOE4، كانت حتى التعرضات المتواضعة لهرمون الإجهاد كافية لرفع مستويات سيكلوفيلين D، منظم رئيسي للمسامات، ولتحفيز فتح المسام. حجب هذه المسام بعقارين مختلفين — أحدهما يتداخل مباشرة مع سيكلوفيلين D والآخر يخفف إنتاج المؤكسدات الميتوكوندرية (mito-apocynin) — حمى خلايا APOE4 من فقدان الطاقة، والزيادة في المؤكسدات التفاعلية، وتغيرات تاو.
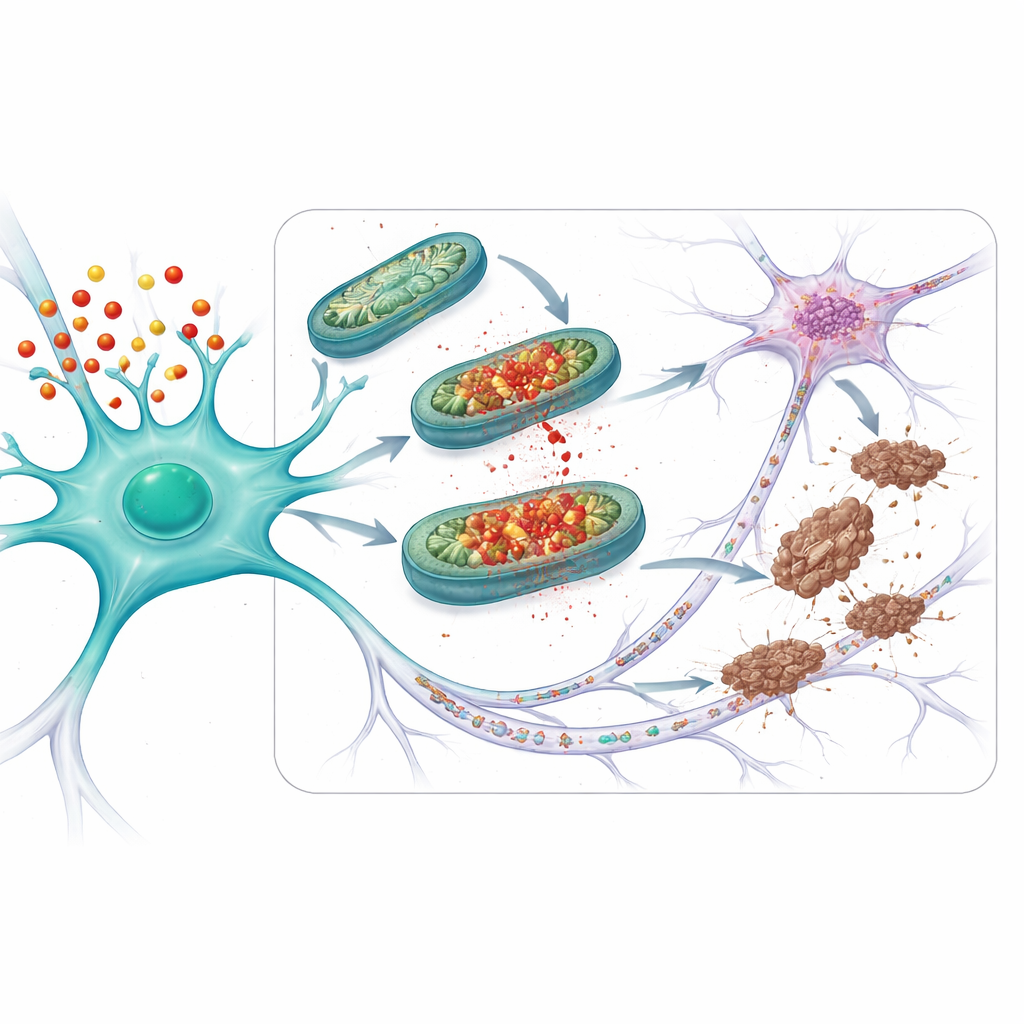
حماية الروابط والدماغ المسن
سأل الفريق بعد ذلك ما إذا كانت هذه الاستراتيجية الوقائية ستفيد في نماذج أقرب إلى المرض. درسوا فئرانًا لم تحمل APOE4 فحسب، بل أنتجت أيضًا شكلًا متحورًا من تاو يميل إلى تكوين تشابكات بسهولة. في هذه الحيوانات، كانت المشاكل الميتوكوندرية، وتاو الشاذ، وفقد المشابك — نقاط الاتصال بين الخلايا العصبية — أسوأ من الفئران ذات نسخة APOE3 الأكثر أمانًا. علاج فئران APOE4 بـ mito-apocynin، بدءًا قبل ظهور أعراض واضحة، قلل من الضرر الميتوكوندري، وتغيرات تاو، وفقدان المشابك. وفي فئران APOE4 الأكبر سنًا ذات مشاكل تاو الناشئة طبيعيًا (حتى من دون تاو المتحور المضاف)، أعادت معالجات قصيرة الأجل بـ mito-apocynin وظيفة الميتوكوندريا، وخففت تاو الشاذ، وقلّلت مدى انتشار تاو بين الخلايا العصبية.
ما معنى هذا للأشخاص المعرضين للخطر
بعبارة بسيطة، تشير هذه الدراسة إلى أن APOE4 يجعل محطات طاقة خلايا الدماغ أكثر هشاشة ومفاتيح استجابتها للإجهاد أكثر سهولة في الانفعال. عندما تُضاف هرمونات الإجهاد المزمن فوق ذلك، يسرع هذا المزيج الشلال الذي يبدأ من الضرر الميتوكوندري ليؤدي إلى تراكم تاو السام، وانتشاره، وفقدان الاتصالات الدماغية. والأهم من ذلك، تُظهر الدراسة أن حجب مسام ميتوكوندرية محددة يمكن أن يقطَع هذا الشلال في نماذج APOE4. ومع أن هناك حاجة إلى الكثير من العمل قبل أن يصل أي علاج إلى المرضى، فقد يصبح استهداف هذه المسام — وإدارة الإجهاد المزمن، خاصة لدى حاملي APOE4 — جزءًا من استراتيجيات مستقبلية لإبطاء أو منع الضرر المرتبط بالزهايمر.
الاستشهاد: Yu, Q., Du, F., Puerta-Alvarado, V. et al. APOE4 exacerbates glucocorticoid stress hormone-induced tau pathology via mitochondrial dysfunction. Cell Death Dis 17, 419 (2026). https://doi.org/10.1038/s41419-026-08543-1
الكلمات المفتاحية: APOE4, الضغط المزمن, الميتوكوندريا, اعتلال تاو, مرض الزهايمر