Clear Sky Science · fr
APOE4 aggrave la pathologie tau induite par les glucocorticoïdes du stress via la dysfonction mitochondriale
Pourquoi les gènes liés au stress et à la mémoire nous concernent tous
Beaucoup de personnes craignent que des périodes prolongées de stress n’augmentent le risque de troubles de la mémoire plus tard dans la vie. Parallèlement, une variante génétique courante appelée APOE4 est connue pour accroître fortement le risque de maladie d’Alzheimer. Cette étude réunit ces deux fils conducteurs en examinant comment les hormones du stress et APOE4 interagissent à l’intérieur des cellules cérébrales, et si cette interaction pourrait indiquer de nouvelles pistes pour protéger le cerveau vieillissant.
Comment un gène de risque courant rencontre le stress quotidien
Les chercheurs se sont concentrés sur APOE4, une version d’une protéine impliquée dans le métabolisme du cholestérol portée par des millions de personnes dans le monde. Ils ont associé ce contexte génétique à une exposition aux glucocorticoïdes, les principales hormones du stress libérées lors d’un stress psychologique chronique. En utilisant des souris génétiquement modifiées pour porter l’APOE humaine 3 (la version plus neutre) ou 4, et des neurones cultivés à partir de leurs cerveaux, ils se sont focalisés sur l’hippocampe, un centre de la mémoire particulièrement sensible au stress et à la maladie d’Alzheimer. Leur objectif était de savoir si APOE4 rend ces neurones plus vulnérables aux effets néfastes des hormones du stress.
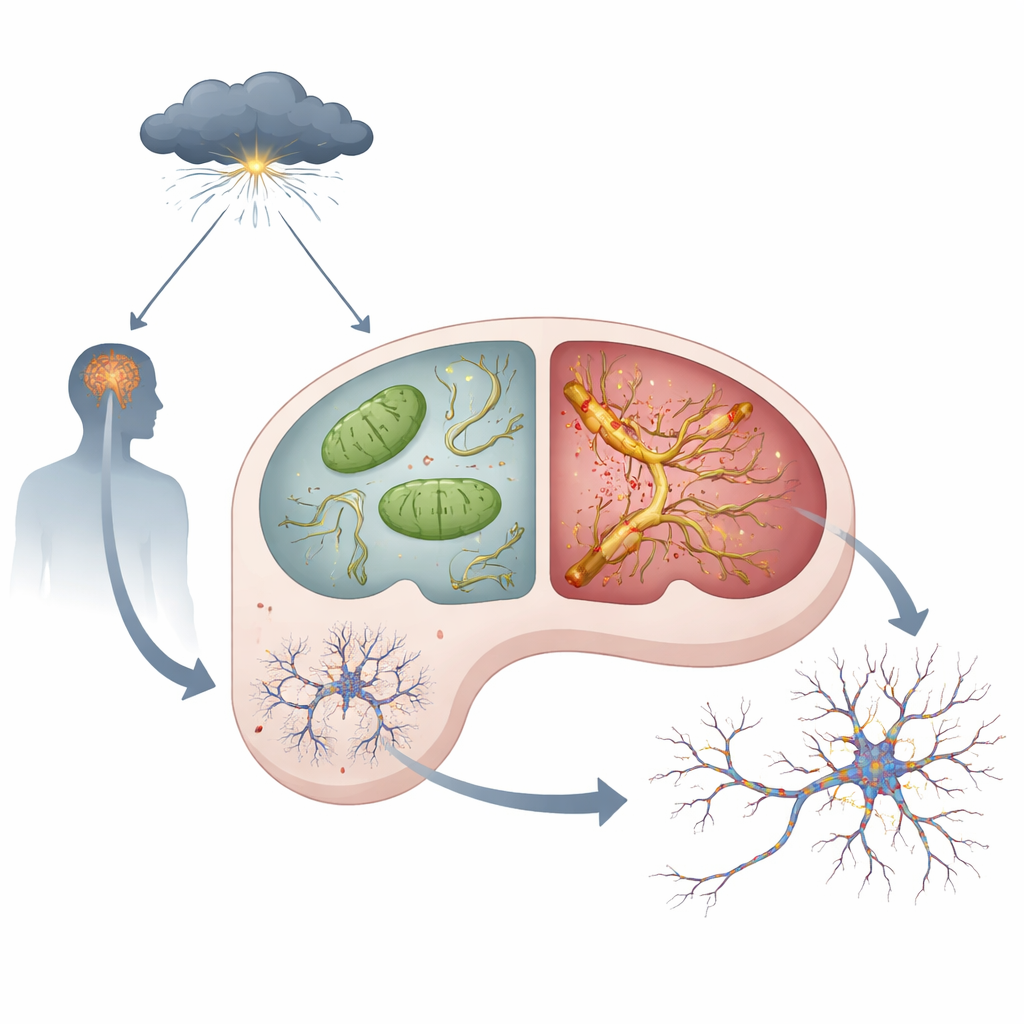
Hormones du stress, centrales énergétiques défaillantes et tau toxique
À l’intérieur de chaque neurone se trouvent les mitochondries, petites centrales qui produisent l’énergie nécessaire à la pensée et à la mémoire. L’équipe a constaté que, même en conditions calmes, les souris APOE4 présentaient des signes de dysfonction mitochondriale dans l’hippocampe : davantage de sous-produits oxydatifs réactifs, une activité plus faible d’un complexe clé de production d’énergie et des niveaux réduits d’ATP, la monnaie énergétique de la cellule. Lorsque les animaux ont été traités par de fortes doses d’une hormone de synthèse mimant le stress chronique, ces problèmes se sont aggravés chez les souris APOE4 par rapport aux souris APOE3. Parallèlement, la protéine tau — qui aide normalement à stabiliser les « rails » internes de la cellule — a commencé à s’accumuler, à être excessivement modifiée, à s’agréger et à se propager de neurone en neurone. Ces altérations de la tau, souvent désignées sous le terme de pathologie tau, étaient bien plus prononcées et étendues dans les cerveaux APOE4 exposés aux hormones du stress.
Signalisation du stress hyperactive dans des cerveaux vulnérables
L’étude a aussi examiné l’intensité de la réponse des cellules cérébrales aux signaux de stress. Les glucocorticoïdes agissent via des récepteurs qui se trouvent normalement dans le cytosol et migrent vers le noyau et les mitochondries une fois activés. Chez les souris APOE4, ces récepteurs étaient déjà plus actifs au repos et migraient plus facilement vers le noyau et les mitochondries, bien que les niveaux hormonaux sanguins globaux soient similaires à ceux des animaux APOE3. En appui, les animaux et les neurones APOE4 présentaient des taux plus élevés de protéines auxiliaires favorisant l’activation des récepteurs, et des profils d’expression génique cohérents avec une signalisation aux glucocorticoïdes renforcée. En culture cellulaire, des très faibles doses d’hormone de stress, peu actives sur les neurones APOE3, suffisaient à endommager les mitochondries et à déclencher l’accumulation et la libération de tau dans les neurones APOE4, montrant que ce contexte génétique abaisse le seuil de dommage lié au stress.
Un pore mitochondrial critique et une voie d’intervention possible
Approfondissant leur analyse, les chercheurs ont ciblé le pore de transition de perméabilité mitochondriale (mPTP), un canal qui peut s’ouvrir dans la membrane interne mitochondriale. Lorsque ce pore s’ouvre, les mitochondries perdent leur potentiel électrique, libèrent des molécules réactives nocives et peuvent pousser la cellule vers la dysfonction. Dans les neurones APOE4, même une exposition modeste aux hormones du stress suffisait à augmenter les niveaux de cyclophiline D, un régulateur clé du pore, et à déclencher son ouverture. Bloquer ce pore avec deux médicaments différents — l’un interférant directement avec la cyclophiline D et l’autre réduisant la production d’oxydants mitochondriaux (mito-apocynine) — a protégé les neurones APOE4 de la perte d’énergie, de l’excès de molécules réactives et des altérations de la tau.
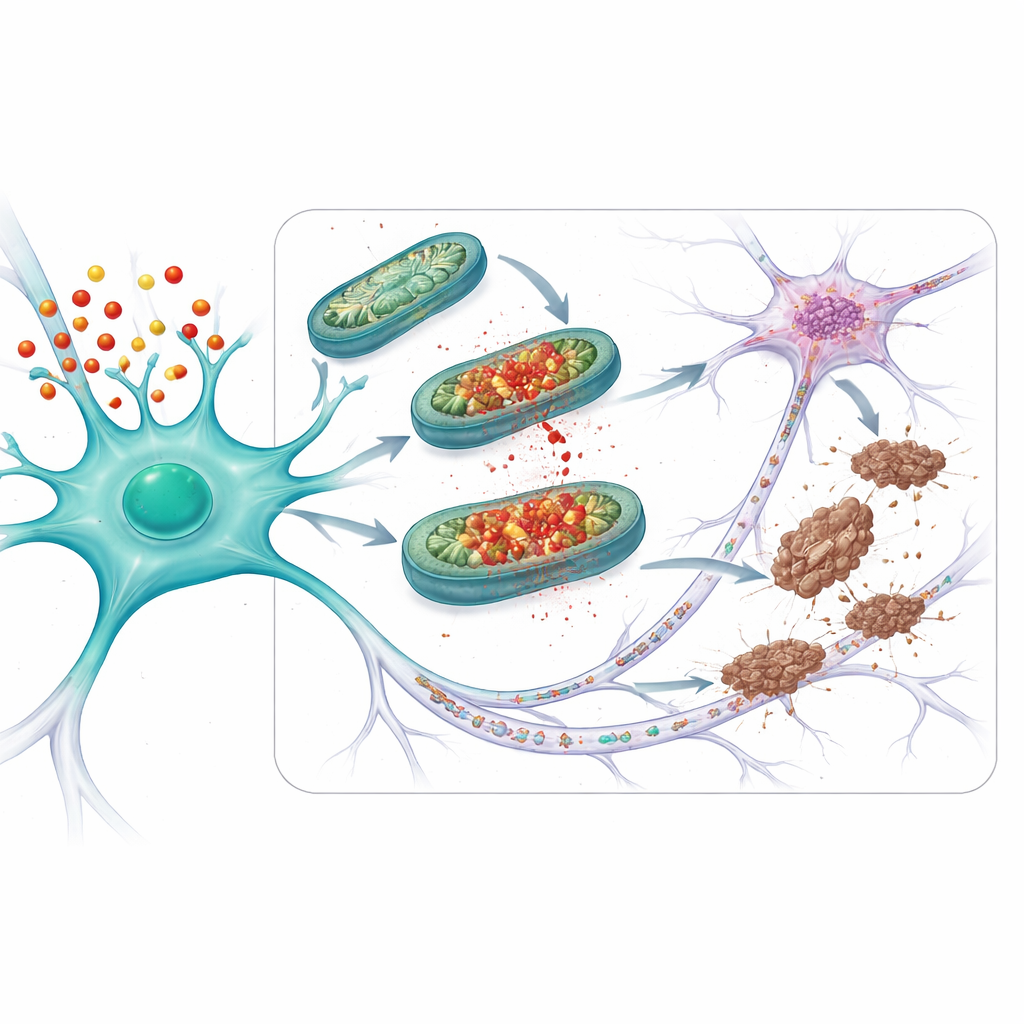
Protéger les connexions et les cerveaux vieillissants
Les chercheurs ont ensuite évalué si cette stratégie protectrice fonctionnait dans des contextes plus proches de la maladie. Ils ont étudié des souris qui, en plus de porter APOE4, produisent une forme mutante de tau qui forme facilement des enchevêtrements. Chez ces animaux, les problèmes mitochondriaux, la tau anormale et la perte de synapses — les points de connexion entre neurones — étaient tous pires que chez les souris portant la version plus sûre APOE3. Le traitement des souris APOE4 par mito-apocynine, débuté avant l’apparition de symptômes évidents, a réduit les dégâts mitochondriaux, les altérations de la tau et la perte de synapses. Chez des souris APOE4 plus âgées présentant des problèmes de tau émergents naturellement (même sans tau mutante ajoutée), un traitement à court terme par mito-apocynine a de même restauré la fonction mitochondriale, réduit la tau anormale et limité la propagation de la tau entre neurones.
Ce que cela signifie pour les personnes à risque
En termes simples, ce travail suggère qu’APOE4 rend les centrales énergétiques des cellules cérébrales plus fragiles et leurs interrupteurs de réponse au stress plus faciles à activer. Lorsqu’on ajoute des hormones du stress chronique, cette combinaison accélère la cascade allant des dommages mitochondriaux à l’accumulation toxique de tau, à sa propagation et à la perte de connexions cérébrales. Surtout, l’étude montre que bloquer un pore mitochondrial spécifique peut interrompre cette cascade dans des modèles APOE4. Bien que beaucoup de travail reste nécessaire avant qu’un traitement n’atteigne les patients, cibler ce pore — et gérer le stress chronique, en particulier chez les porteurs d’APOE4 — pourrait devenir une des stratégies futures pour ralentir ou prévenir les dommages liés à la maladie d’Alzheimer.
Citation: Yu, Q., Du, F., Puerta-Alvarado, V. et al. APOE4 exacerbates glucocorticoid stress hormone-induced tau pathology via mitochondrial dysfunction. Cell Death Dis 17, 419 (2026). https://doi.org/10.1038/s41419-026-08543-1
Mots-clés: APOE4, stress chronique, mitochondries, pathologie tau, maladie d’Alzheimer