Clear Sky Science · ru
APOE4 усугубляет индукцию тау-патологии стрессовым гормоном-глюкокортикоидом через дисфункцию митохондрий
Почему стресс и гены памяти важны для всех нас
Многие опасаются, что длительные периоды стресса могут повысить вероятность развития проблем с памятью в более позднем возрасте. Одновременно известно, что распространённый вариант гена, называемый APOE4, сильно увеличивает риск болезни Альцгеймера. В этом исследовании эти два направления объединяются: учёные спрашивают, как стрессовые гормоны и APOE4 взаимодействуют внутри нервных клеток и может ли это взаимодействие указать на новые способы защиты стареющего мозга.
Как распространённый ген риска встречается с повседневным стрессом
Исследователи сосредоточились на APOE4 — варианте белка, участвующего в обращении холестерина, который носит миллионы людей по всему миру. Они сопоставили этот генетический фон с воздействием глюкокортикоидов — основных стрессовых гормонов, выделяемых при хроническом психологическом давлении. Используя мышей, генетически модифицированных для ношения человеческих APOE3 (более нейтральной версии) или APOE4, а также нейронов, выращенных из их мозга, они внимательно изучали гиппокамп — центр памяти, особенно чувствительный и к стрессу, и к болезни Альцгеймера. Целью было выяснить, делает ли APOE4 эти нейроны более уязвимыми к вредному влиянию стрессовых гормонов.
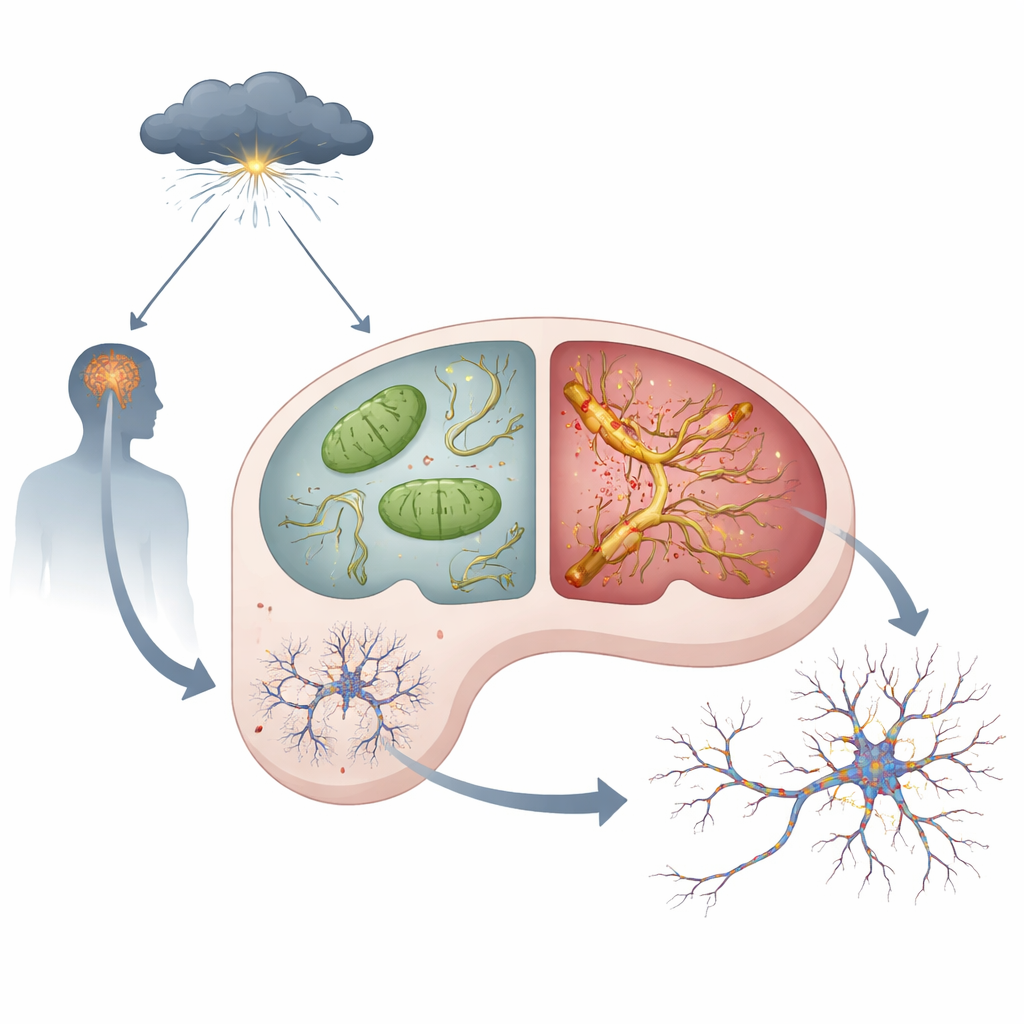
Стрессовые гормоны, повреждённые «электростанции» и токсичный тау
Внутри каждого нейрона находятся митохондрии — крошечные «электростанции», вырабатывающие энергию, необходимую для мышления и запоминания. Команда обнаружила, что даже в спокойных условиях у мышей с APOE4 в гиппокампе проявляются признаки митохондриальных проблем: больше побочных реактивных продуктов, сниженная активность ключевого энергетического комплекса и более низкий уровень АТФ — «денег» клетки. При обработке животных высокими дозами синтетического стрессового гормона, имитирующего хронический стресс, эти нарушения усиливались у мышей с APOE4 сильнее, чем у APOE3. Одновременно белок тау — который обычно стабилизирует внутриклеточные «рельсы» — начал накапливаться, чрезмерно модифицироваться, агрегироваться и распространяться от нейрона к нейрону. Эти изменения тау, часто называемые тау-патологией, были значительно выраженнее и охватывали большую территорию в мозгах APOE4, подвергшихся действию стрессовых гормонов.
Гиперактивная стрессовая сигнализация в уязвимых мозгах
Исследование также оценивало силу ответа клеток мозга на стрессовые сигналы. Глюкокортикоиды действуют через рецепторы, которые обычно находятся в цитоплазме и при активации перемещаются в ядро и митохондрии. У мышей с APOE4 эти рецепторы уже имели повышенную активность в базальном состоянии и легче перемещались в ядро и митохондрии, хотя общий уровень гормонов в крови был сопоставим с животными APOE3. В подтверждение этого у APOE4-животных и нейронов были обнаружены повышенные уровни вспомогательных белков, способствующих активации рецепторов, и профиль экспрессии генов, соответствующий усиленной стресс-гормональной сигнализации. В клеточной культуре очень низкие дозы стрессового гормона, которые почти не влияли на нейроны APOE3, были достаточны, чтобы повредить митохондрии и вызвать накопление и выделение тау в нейронах APOE4, что показывает: этот генетический фон снижает порог вреда от стресса.
Критический пор в митохондриях и возможный путь вмешательства
Углубляясь, исследователи сосредоточились на митохондриальном пороговом канале проницаемости (mPTP) — канале, который может открываться во внутренней мембране митохондрий. При открытии этого порта митохондрии теряют электрический заряд, выкачивают вредные реактивные молекулы и могут направлять клетки к дисфункции. В нейронах APOE4 даже умеренное воздействие стрессового гормона повышало уровень циклофилина D — ключевого регулятора поры — и инициировало её открытие. Блокирование этой поры двумя разными препаратами — одним, который непосредственно вмешивается в функцию циклофилина D, и другим, снижающим митохондриальное образование окислителей (mito-apocynin) — защищало нейроны APOE4 от потери энергии, избытка реактивных молекул и изменений тау.
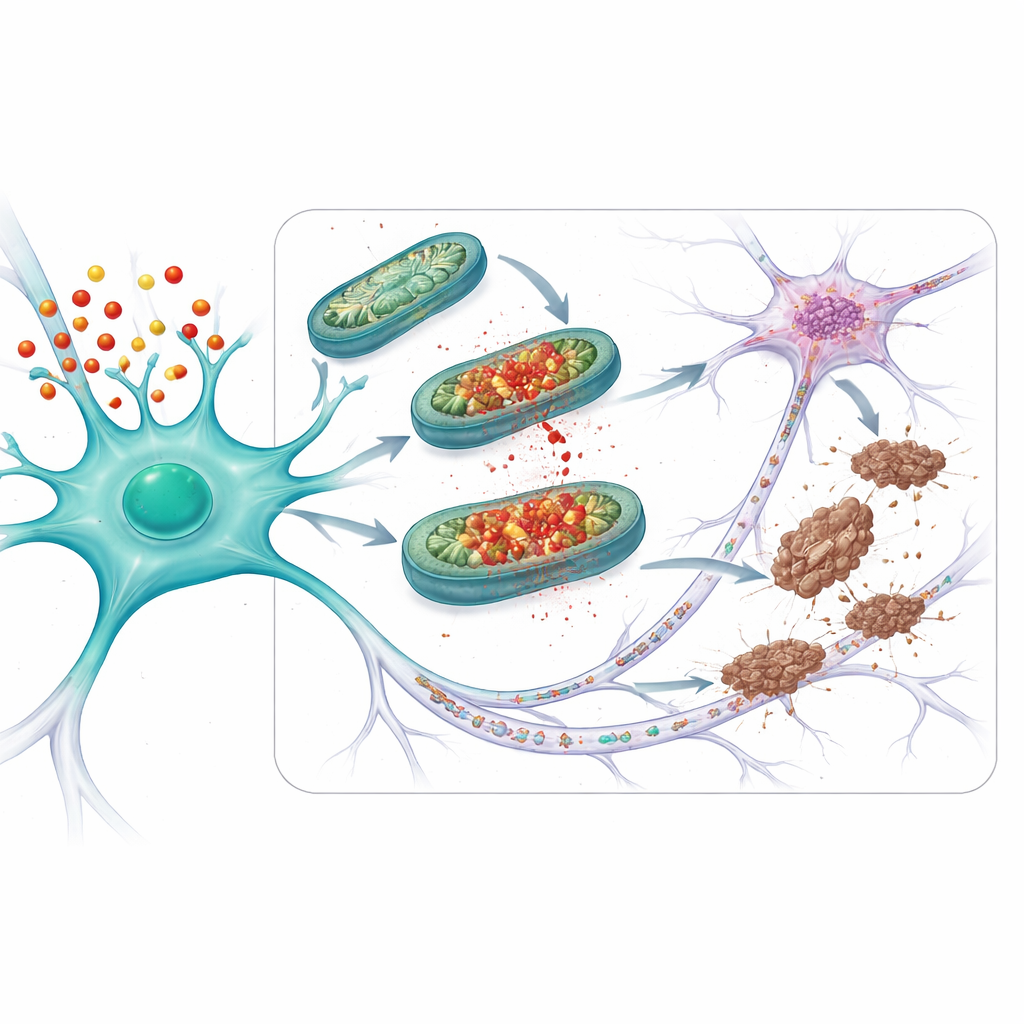
Защита синапсов и стареющих мозгов
Затем команда изучила, поможет ли эта защитная стратегия в условиях, более близких к заболеванию. Они исследовали мышей, которые не только несли APOE4, но и производили мутантную форму тау, склонную к образованию клубков. У этих животных митохондриальные нарушения, патологический тау и потеря синапсов — точек соединения между нейронами — были более выражены, чем у мышей с безопасной версией APOE3. Лечение APOE4-мышей mito-apocynin, начатое до появления явных симптомов, уменьшало митохондриальные повреждения, изменения тау и потерю синапсов. У пожилых APOE4-мышей с естественно возникающими проблемами с тау (даже без дополнительного мутантного тау) краткосрочное лечение mito-apocynin аналогично восстановило функцию митохондрий, снизило аномальный тау и ограничило дальность его распространения между нейронами.
Что это значит для людей с риском
Проще говоря, эта работа указывает, что APOE4 делает «электростанции» клеток мозга более хрупкими, а переключатели стрессовой реакции — более чувствительными. При добавлении хронических стрессовых гормонов такое сочетание ускоряет каскад, ведущий от митохондриального повреждения к накоплению токсичного тау, его распространению и потере нейронных связей. Существенно, что исследование показывает: блокирование определённой митохондриальной поры может прервать этот каскад в моделях APOE4. Хотя до появления терапии для пациентов потребуется ещё много работы, нацеливание на эту пору — и управление хроническим стрессом, особенно у носителей APOE4 — может стать частью будущих стратегий замедления или предотвращения повреждений, связанных с болезнью Альцгеймера.
Цитирование: Yu, Q., Du, F., Puerta-Alvarado, V. et al. APOE4 exacerbates glucocorticoid stress hormone-induced tau pathology via mitochondrial dysfunction. Cell Death Dis 17, 419 (2026). https://doi.org/10.1038/s41419-026-08543-1
Ключевые слова: APOE4, хронический стресс, митохондрии, тау-патология, болезнь Альцгеймера