Clear Sky Science · nl
APOE4 verergert door glucocorticoïde-stresshormonen geïnduceerde tau-pathologie via mitochondriale disfunctie
Waarom stress en geheugen-genen ons allemaal aangaan
Veel mensen vrezen dat langdurige stress hun kans op geheugenproblemen op latere leeftijd vergroot. Tegelijkertijd is een veelvoorkomende genetische variant, APOE4, bekend als een sterke risicofactor voor de ziekte van Alzheimer. Deze studie brengt die twee lijnen samen: hoe interacteren stresshormonen en APOE4 in hersencellen, en wijst die interactie op nieuwe manieren om het ouder wordende brein te beschermen?
Hoe een veelvoorkomend risicogen en alledaagse stress elkaar ontmoeten
De onderzoekers concentreerden zich op APOE4, een variant van een eiwit dat cholesterol reguleert en door miljoenen mensen wereldwijd wordt gedragen. Ze combineerden deze genetische achtergrond met blootstelling aan glucocorticoïden, de belangrijkste stresshormonen die vrijkomen bij chronische psychologische druk. Met muizen die zo waren gemodificeerd dat ze het menselijke APOE3 (de meer neutrale versie) of APOE4 droegen, en met zenuwcellen die uit hun hersenen werden gekweekt, zoomden ze in op de hippocampus, een geheugencentrum dat bijzonder gevoelig is voor zowel stress als de ziekte van Alzheimer. Hun doel was te bepalen of APOE4 deze neuronen kwetsbaarder maakt voor de schadelijke effecten van stresshormonen.
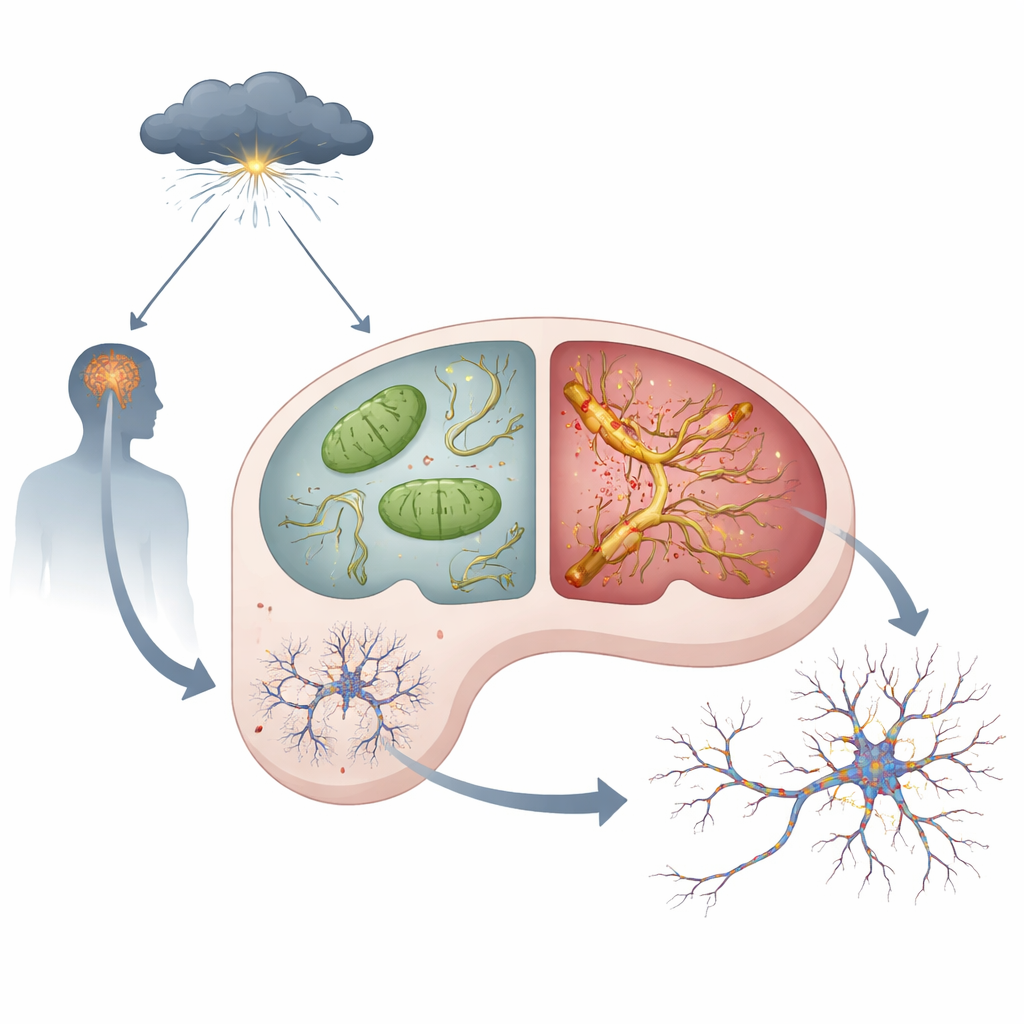
Stresshormonen, defecte energiecentrales en toxische tau
In elke neuron bevinden zich mitochondriën, kleine energiecentrales die de energie leveren die nodig is voor denken en onthouden. Het team ontdekte dat zelfs onder rustige omstandigheden APOE4-muizen tekenen van mitochondriale problemen in de hippocampus vertoonden: meer reactieve zuurstofbijproducten, zwakkere activiteit van een sleutelcomplex voor energieproductie en lagere ATP-niveaus, de energie-eenheid van de cel. Wanneer de dieren werden behandeld met hoge doses van een synthetisch stresshormoon dat chronische stress nabootst, verslechterden deze problemen meer bij APOE4-muizen dan bij APOE3-muizen. Tegelijkertijd begon een eiwit genaamd tau — dat normaal helpt interne „sporen” in de cel te stabiliseren — zich op te stapelen, overmatig te worden gewijzigd, samen te klonteren en van neuron naar neuron te verspreiden. Deze veranderingen in tau, vaak tau-pathologie genoemd, waren veel sterker en verspreidden zich verder in APOE4-hersenen die aan stresshormonen waren blootgesteld.
Overactieve stresssignalen in kwetsbare hersenen
De studie onderzocht ook hoe sterk hersencellen reageerden op stresssignalen. Glucocorticoïden werken via receptoren die normaal in de celvloeistof zitten en bij activatie naar de kern en mitochondriën verplaatsen. Bij APOE4-muizen waren deze receptoren al bij basislijn actiever en verplaatsten ze zich makkelijker naar de kern en mitochondriën, hoewel de totale hormoonniveaus in het bloed vergelijkbaar waren met die van APOE3-dieren. Ondersteunend hierbij toonden APOE4-dieren en neuronen hogere niveaus van helper-eiwitten die receptoractivatie bevorderen, en genexpressiepatronen die overeenkomen met sterkere stresshormoonsignalering. In celkweken waren zeer lage doses stresshormoon die weinig effect hadden op APOE3-neuronen voldoende om mitochondriën te beschadigen en tau-opstapeling en -afgifte te veroorzaken in APOE4-neuronen, wat laat zien dat deze genetische achtergrond de drempel voor stressgerelateerde schade verlaagt.
Een kritisch porie in mitochondriën en een mogelijke interventie
Dieper gravend richtten de onderzoekers zich op de mitochondriale permeabiliteitstransitiepoort (mPTP), een kanaal dat kan openen in het binnenmembraan van mitochondriën. Wanneer deze poort opent, verliezen mitochondriën hun elektrische lading, pompen ze schadelijke reactieve moleculen uit en kunnen ze cellen richting disfunctie duwen. In APOE4-neuronen was zelfs een bescheiden blootstelling aan stresshormoon voldoende om de niveaus van cyclophiline D, een belangrijke regulator van de poort, te verhogen en opening van de poort te veroorzaken. Het blokkeren van deze poort met twee verschillende middelen — één dat direct interfereert met cyclophiline D en een ander dat de mitochondriale oxidantproductie dempt (mito-apocynine) — beschermde APOE4-neuronen tegen energieverlies, overtollige reactieve moleculen en tau-veranderingen.
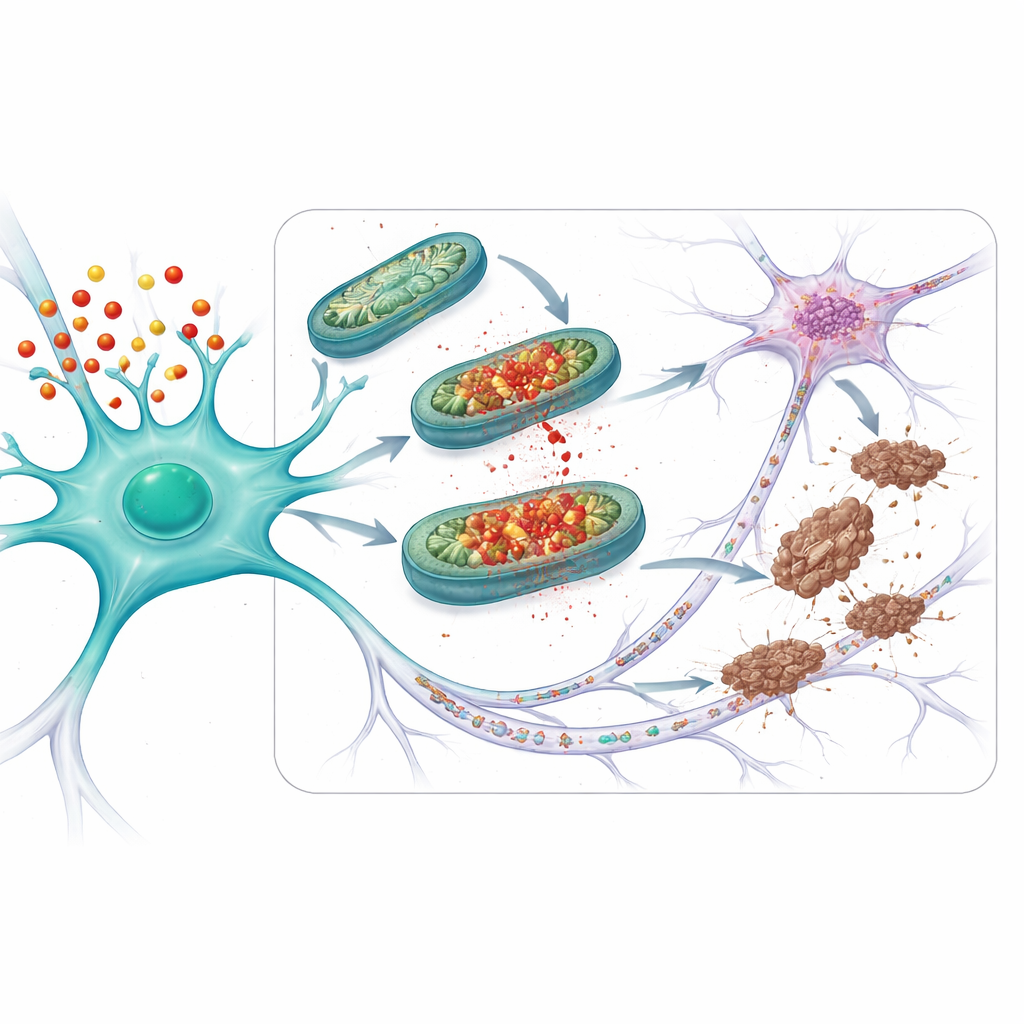
Het beschermen van verbindingen en verouderende hersenen
Het team vroeg zich vervolgens af of deze beschermende strategie ook werkt in meer ziekteachtige omstandigheden. Ze bestudeerden muizen die niet alleen APOE4 droegen, maar ook een gemuteerde vorm van tau produceerden die gemakkelijk kluwens vormt. Bij deze dieren waren mitochondriale problemen, abnormale tau en verlies van synapsen — de verbindingspunten tussen neuronen — allemaal erger dan bij muizen met de veiligere APOE3-versie. Behandeling van APOE4-muizen met mito-apocynine, begonnen voordat duidelijke symptomen verschenen, verminderde mitochondriale schade, tau-veranderingen en synapsverlies. Bij oudere APOE4-muizen met van nature opkomende tau-problemen (zelfs zonder extra gemuteerde tau) herstelde kortdurende behandeling met mito-apocynine op vergelijkbare wijze de mitochondriale functie, verminderde abnormale tau en beperkte hoe ver tau zich tussen neuronen verspreidde.
Wat dit betekent voor mensen met risico
Simpel gezegd suggereert dit werk dat APOE4 de energiecentrales van hersencellen fragieler maakt en hun stress-responschakelaars gevoeliger doet omslaan. Wanneer chronische stresshormonen daarbovenop komen, versnelt die combinatie de cascade die leidt van mitochondriale schade naar toxische tau-opstapeling, verspreiding en verlies van hersenverbindingen. Cruciaal is dat de studie laat zien dat het blokkeren van een specifieke mitochondriale poort deze cascade kan onderbreken in APOE4-modellen. Hoewel er veel meer onderzoek nodig is voordat een behandeling patiënten bereikt, zou het richten op deze poort — en het beheersen van chronische stress, vooral bij APOE4-dragers — deel kunnen worden van toekomstige strategieën om Alzheimer-gerelateerde schade te vertragen of te voorkomen.
Bronvermelding: Yu, Q., Du, F., Puerta-Alvarado, V. et al. APOE4 exacerbates glucocorticoid stress hormone-induced tau pathology via mitochondrial dysfunction. Cell Death Dis 17, 419 (2026). https://doi.org/10.1038/s41419-026-08543-1
Trefwoorden: APOE4, chronische stress, mitochondriën, tau-pathologie, Ziekte van Alzheimer